Identificar los órganos más propensos a desarrollar el síndrome de insuficiencia multiorgánica (MODS) en pacientes con sepsis por peritonitis secundaria. Determinar el valor evolutivo y predictivo de mortalidad del sistema Sequential Organ Failure Assessment (SOFA).
DiseñoEstudio de cohorte observacional prospectivo.
ÁmbitoLa unidad de reanimación (UR) de nuestro centro, un hospital universitario de tercer nivel.
PacientesEstudio prospectivo y observacional sobre 102 pacientes con sepsis de origen abdominal e insuficiencia de al menos un órgano relacionado con la infección. Se registraron las características demográficas, el origen abdominal de la sepsis, la mortalidad a los 28 días y la puntuación SOFA diaria.
ResultadosLa mortalidad a los 28 días fue del 55%. El 53% de los pacientes presentaron fracaso de 2 o más órganos en el primer día de estancia. La puntuación SOFA media diaria fue significativamente mayor en los pacientes fallecidos a partir del cuarto día de estancia. Las variables que se asociaron a una mayor mortalidad de manera estadísticamente significativa fueron: MODS (p=0,000), fallo sistema nervioso central (p=0,000) y puntuación SOFA al cuarto día de estancia (p=0,012). El área bajo la curva ROC expresó una capacidad predictiva de mortalidad el SOFA cuarto día de estancia del 0,703 (IC 95%, 0,538-0,853 y p=0,026. El mejor poder discriminativo se observó para el MODS con área bajo la curva ROC del 0,776 (IC 95%, 0,678-0,874 y p=0,000).
ConclusionesLa evolución en la insuficiencia de órganos determinada por medio de SOFA mostró una alta precisión siendo un buen predictor de mortalidad la puntuación SOFA media cuarto día de estancia. El MODS fue la principal causa de muerte y el fracaso del sistema nervioso central, función renal y sistema respiratorio los factores de riesgo de muerte.
To identify the organs most susceptible to develop multiorgan dysfunction syndrome (MODS) in patients with sepsis due to secondary peritonitis, and to determine the outcome and mortality predicting utility of the SOFA (Sequential Organ Failure Assessment) system.
DesignA prospective, observational cohort study was made.
SettingThe resuscitation unit of a third-level university hospital.
PatientsA prospective, observational cohort study was made of 102 patients with sepsis of abdominal origin and failure of at least one organ related to the infection. The demographic characteristics were documented, along with the abdominal origin of sepsis, mortality after 28 days, and the daily SOFA score.
ResultsThe mortality rate after 28 days was 55%. A total of 53% of the patients presented failure of two or more organs on the first day of admission. The mean daily SOFA score was significantly higher among the patients that died after day 4 of admission. The variables showing a statistically significant correlation to increased mortality were: MODS (P=.000), central nervous system failure (P=.000) and SOFA score on day 4 of admission (P=.012). The area under the ROC curve showed the mortality predicting capacity of the SOFA score on day 4 of admission to be 0.703 (95%CI 0.538-0.853; P=.026). The maximum discriminating capacity was recorded for MODS, with an area under the ROC curve of 0.776 (95%CI 0.678-0.874; P=.000).
ConclusionsOrgan failure outcome as predicted by the SOFA score showed high precision – the mean SOFA score on day 4 of admission being a good mortality predictor. MODS was the main cause of death, while central nervous system, renal and respiratory failure were identified as the mortality risk factors.
La peritonitis secundaria se asocia con una morbimortalidad elevada a pesar de los avances en los cuidados intensivos y en las técnicas quirúrgicas1. Además, una respuesta inflamatoria sistémica inducida por la infección peritoneal puede progresar a shock séptico e insuficiencia multiorgánica, a pesar de un adecuado control quirúrgico y tratamiento antimicrobiano. Se han utilizado diferentes sistemas para la valoración de la afectación multiorgánica y predicción de mortalidad derivada de la infección abdominal con resultados variables2,3. De los distintos sistemas de valoración de la disfunción de órganos (LODS, MODS, SOFA), el que más amplia aceptación parece haber logrado en adultos es el sistema SOFA («Sepsis-related Organ Failure Assessment», o «Sequential Organ Failure Assessment»)4. Se ha demostrado que la insuficiencia de órganos evaluada por medio del sistema SOFA tiene valor predictivo evolutivo y de mortalidad en diferentes grupos de pacientes quirúrgicos5–7. Ferreira et al.8 demostraron cómo el incremento en la puntuación SOFA en las primeras 48h de estancia en pacientes críticos ingresados en la unidad de cuidados intensivos (UCI) predice una tasa de mortalidad mayor del 50%, independiente de la puntuación inicial. El SOFA se trata de un sistema sencillo, diseñado específicamente para la sepsis y para ser evaluado de forma repetida a lo largo de la evolución del enfermo8. Incluye la valoración de la función de 6 órganos o sistemas (aparato respiratorio, hemostasia, función hepática, sistema cardiovascular, sistema nervioso central y función renal), con puntuaciones para cada uno de ellos de 0 a 4, denominándose «disfunción» cuando se asignan 1 o 2 puntos, y «fallo o insuficiencia» de órgano cuando alcanza la puntuación de 3 o 4, proporcionando una puntuación diaria de 0 a 24 puntos. Diversos estudios multicéntricos que utilizaron el sistema SOFA demostraron diferentes valores pronósticos de cada disfunción orgánica y desigual contribución en los resultados en pacientes críticos, siendo el sistema cardiovascular el que tiene mayor importancia pronóstica4,9. En cambio, el grado de disfunción orgánica medida mediante el SOFA ha sido utilizado tan solo en un estudio como predictor de mortalidad hospitalaria en pacientes con peritonitis secundaria10. El objetivo de este estudio es evaluar las consecuencias de la insuficiencia multiorgánica en pacientes con sepsis por peritonitis secundaria y determinar el valor evolutivo y predictivo de mortalidad del sistema SOFA en estos pacientes tras su ingreso en la unidad de reanimación (UR).
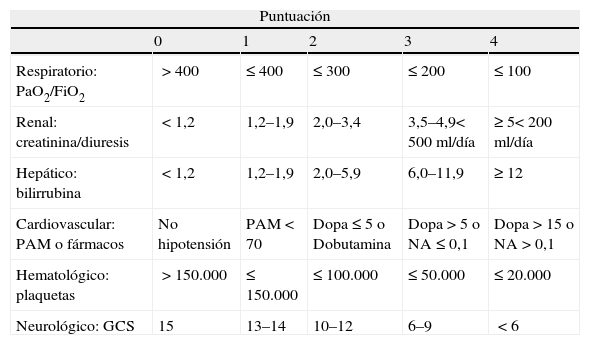
Pacientes y métodosTras la aprobación del Comité de Ética e Investigación Clínica, se realizó un estudio de cohorte observacional prospectivo en la UR de nuestro hospital en el periodo de tiempo comprendido entre el 1 de enero de 2007 y el 31 de diciembre de 2009. Se incluyeron en el estudio a 102 pacientes, de ambos sexos, con el diagnóstico de sepsis grave por peritonitis secundaria. Se consideró sepsis grave como sepsis e insuficiencia de al menos un órgano o sistema relacionado con la infección y síndrome de disfunción multiorgánica (MODS) como la insuficiencia grave, reversible o no, de más de un sistema orgánico vital. La disfunción de órganos (aparato respiratorio, hemostasia, función hepática, sistema cardiovascular, sistema nervioso central y función renal) fue evaluada por medio del sistema SOFA (tabla 1)9. Se consideró disfunción de órgano cuando la puntuación era igual o mayor de 1, registrando diariamente el valor más anormal dentro de la escala de disfunción de 0 a 4, asumiendo en este estudio la insuficiencia orgánica la puntuación 3-4 de la escala SOFA. La puntuación SOFA fue calculada diariamente por medio de la suma de las peores puntuaciones de cada uno de los órganos y sistemas incluidos en SOFA.
Sistema de valoración multiorgánica SOFA (Sequential Organ Failure Assessment)
| Puntuación | |||||
| 0 | 1 | 2 | 3 | 4 | |
| Respiratorio: PaO2/FiO2 | >400 | ≤ 400 | ≤ 300 | ≤ 200 | ≤100 |
| Renal: creatinina/diuresis | <1,2 | 1,2–1,9 | 2,0–3,4 | 3,5–4,9<500 ml/día | ≥5<200 ml/día |
| Hepático: bilirrubina | <1,2 | 1,2–1,9 | 2,0–5,9 | 6,0–11,9 | ≥ 12 |
| Cardiovascular: PAM o fármacos | No hipotensión | PAM<70 | Dopa ≤ 5 o Dobutamina | Dopa>5 o NA ≤ 0,1 | Dopa>15 o NA>0,1 |
| Hematológico: plaquetas | >150.000 | ≤150.000 | ≤100.000 | ≤50.000 | ≤20.000 |
| Neurológico: GCS | 15 | 13–14 | 10–12 | 6–9 | <6 |
Cardiovascular: PAM (presión arterial media). Fármacos vasoactivos administrados durante>1 h; Dopa: dopamina; NA: noradrenalina (dosis en μg/kg/min); Hepático: bilirrubina en mg/dL; Neurológico: GCS (Glasgow Coma Score); Renal: creatinina en mg/dL. Puntos 3-4 en caso de fracaso renal funcional u oligoanuria; Respiratorio: PaO2/FiO2 en mmHg. Puntos 3-4 solo se valoran si precisa ventilación mecánica.
La gravedad de la enfermedad de los pacientes ingresados fue evaluada por medio del sistema SAPS II (Simplified Acuate Physiology Score) durante las primeras 24h de estancia en la UR. El SAPS II es la suma de los puntos asignados a cada una de las 17 variables incluidas en el sistema (12 variables fisiológicas, edad, tipo de ingreso, y 3 enfermedades de base), siendo la puntuación más elevada representación de enfermedad más grave y de mayor mortalidad11.
Se registraron las siguientes variables: características demográficas de los pacientes, origen abdominal de la sepsis, mortalidad a los 28 días y la estancia en la UR. Los pacientes fueron distribuidos en 2 grupos según la supervivencia a los 28 días: supervivientes (n=43) o fallecidos (n=59).
Se creó una base de datos en el programa SPSS 17.0. Las variables cuantitativas con distribución normal se expresaron como media±desviación estándar (DE) y las variables de distribución no-normal (edad, días de estancia y puntuación SAP II) como mediana y el rango intercuartil 25-75. La puntuación SOFA entre grupos se analizó mediante ANOVA. Las variables categóricas fueron expresadas como porcentajes y se analizaron por medio de la prueba de Chi cuadrado. Se consideraron diferencias significativas con un valor de p<0,05.
El poder predictivo de riesgo de muerte de la puntuación SOFA fue contrastado por el área bajo la curva Receiver Operating Characteristic (ROC). El área bajo la curva ROC resume la relación entre la sensibilidad (número de verdaderos positivos) y 1-especificidad (número de falsos positivos) para todos los valores posibles de puntuación SOFA, así como la mayor capacidad de mayor riesgo de muerte a los pacientes que fallecen. Las curvas de supervivencia se estimaron utilizando el método de Kaplan-Meier. Los pacientes ingresados en la UR con el diagnóstico de sepsis grave se estratificaron en subgrupos de acuerdo con el número de disfunciones orgánicas. Los tiempos de supervivencia se midieron a partir de la fecha de ingreso en la UR hasta 28 días de estancia hospitalaria. Se realizó el estudio univariante de las variables en las que se demostró diferencias significativas entre supervivientes y no supervivientes. Adicionalmente, se realizó un análisis de regresión logística multivariada mediante el procedimiento de forward stepwise para poder evaluar las variables asociadas de manera independiente con la mortalidad a los 28 días como una variable dependiente. Los odds ratio con un intervalo de confianza de 95% fueron utilizados para estimar la asociación entre las variables independientes y la mortalidad.
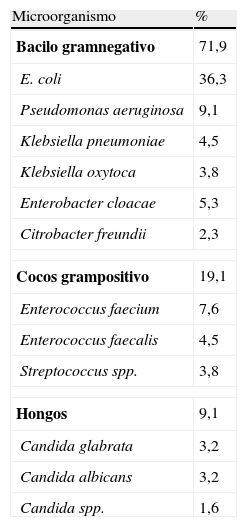
ResultadosLas causas que provocaron la peritonitis secundaria en nuestro estudio fueron perforación de intestino grueso por necrosis de la pared intestinal por neoplasia (31,3%), peritonitis postoperatoria por fuga de anastomosis (23,5%), colecistitis supurativa y/o peritonitis biliar (15,6%), perforación del tracto gastrointestinal (12,7%), traslocación de bacterias por obstrucción intestinal e isquemia mesentérica (10,7%) y pelviperitonitis (5,9%). El 16,7% de los pacientes fueron reintervenidos durante su estancia en la UR principalmente por peritonitis generalizada, dehiscencia de suturas y absceso intraabdominal. En la tabla 2 se muestra la frecuencia de los diferentes microorganismos aislados en cultivo de líquido peritoneal y resistencias a antimicrobianos.
Frecuencia de microorganismos aislados en cultivo de líquido peritoneal y resistencia a antimicrobianos
| Microorganismo | % |
| Bacilo gramnegativo | 71,9 |
| E. coli | 36,3 |
| Pseudomonas aeruginosa | 9,1 |
| Klebsiella pneumoniae | 4,5 |
| Klebsiella oxytoca | 3,8 |
| Enterobacter cloacae | 5,3 |
| Citrobacter freundii | 2,3 |
| Cocos grampositivo | 19,1 |
| Enterococcus faecium | 7,6 |
| Enterococcus faecalis | 4,5 |
| Streptococcus spp. | 3,8 |
| Hongos | 9,1 |
| Candida glabrata | 3,2 |
| Candida albicans | 3,2 |
| Candida spp. | 1,6 |
| Resistencia a antimicrobianos | % |
| Amoxicilina/Clavulánico | 43,2 |
| Quinolonas | 35,1 |
| Cefalosporinas 2.a | 31,3 |
| Cefalosporinas 3.a | 11,2 |
| Piperacilina/Tazobactam | 14,2 |
| Aminoglucósidos | 12,6 |
La mediana de edad fue de 74 (cuartiles 25-75, 63-80 años) años, con un 61% de varones y 39% de mujeres. La mediana de edad fue significativamente mayor en los pacientes fallecidos que en los supervivientes (75 [cuartiles 25-75, 67-80] años y 69 [cuartiles 25-75, 58-78] años, respectivamente; p=0,020). La mediana de la puntuación SAPS II fue de 48 (cuartiles 25-75, 41-54) puntos y la mediana de la estancia en la UR fue 10 (cuartiles 25-75, 5-18) días. La estancia en la UR fue significativamente mayor en los supervivientes que en los pacientes fallecidos (14 [cuartiles 25-75, 9-28] días y 7 [cuartiles 25-75, 3-16] días, respectivamente; p=0,004]), y la puntuación SAPS II mayor en los pacientes fallecidos que en los supervivientes (51 [cuartiles 25-75, 45-55] y 45 [cuartiles 25-75, 38-51], respectivamente; p=0,020).
La mortalidad a las 48h de estancia en la UR fue del 17% y a los 28 días del 55%. El 53% de los pacientes presentaron fracaso de 2 o más órganos en el primer día de estancia con insuficiencia cardiovascular y respiratoria como más frecuentes (87 y 51%, respectivamente). El 90% de los pacientes presentaron fracaso de 2 o más órganos durante la estancia completa en la UR, siendo la insuficiencia cardiovascular la más frecuente (97%), seguida del aparato respiratorio (76%), función renal (56%), sistema nervioso central (51%), hemostasia (28%) y función hepática (11%). El 73,5% de los pacientes incluidos en el estudio necesitaron ventilación mecánica mostrando una mortalidad significativamente mayor que los pacientes no ventilados mecánicamente (66,7 y 25,9%, respectivamente; p=0,000). El 37,3% de los pacientes sometidos a ventilación mecánica desarrollaron neumonía.
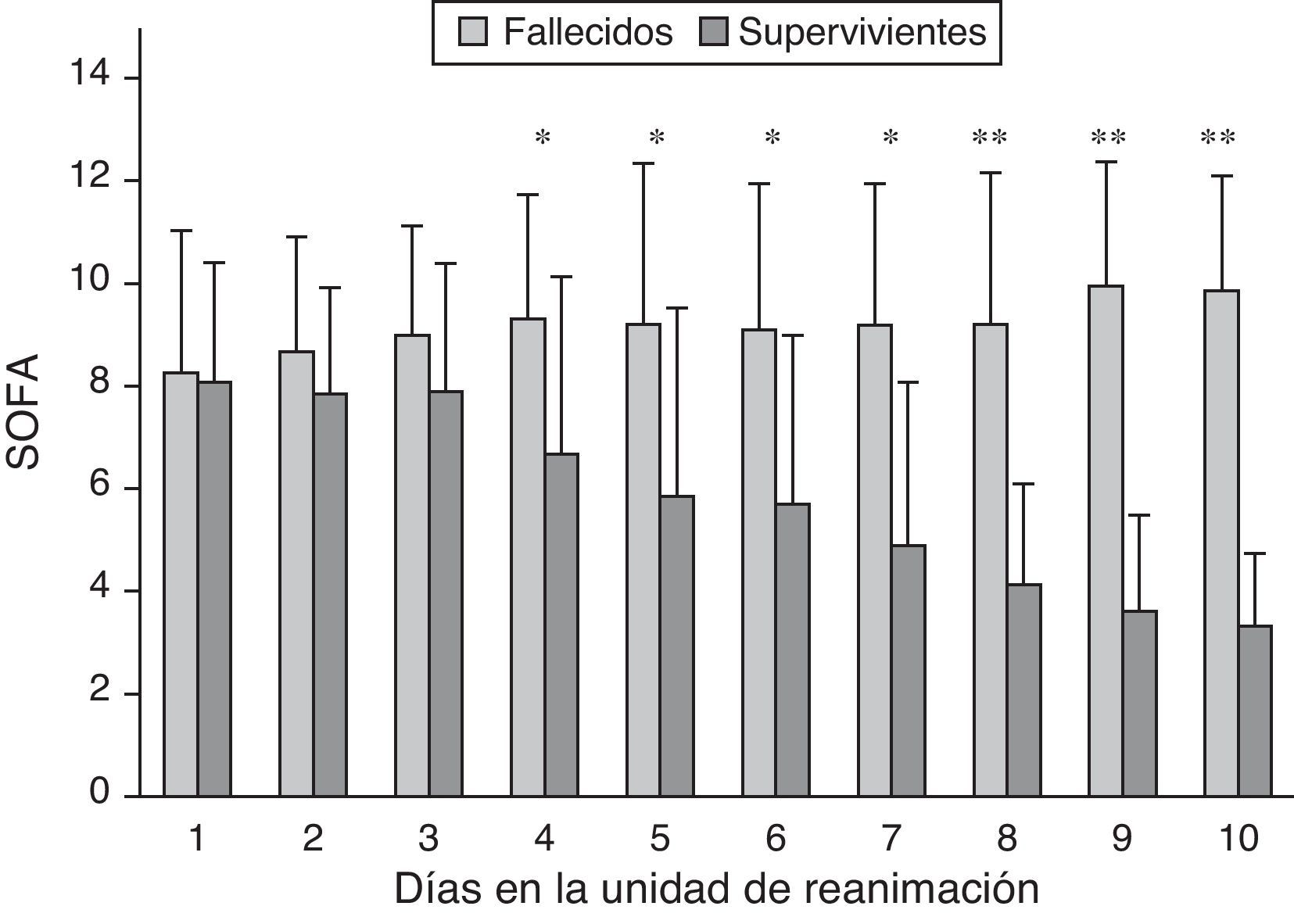
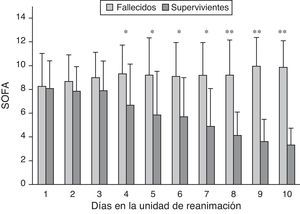
La puntuación SOFA media diaria fue mantenida y significativamente mayor en los pacientes fallecidos que en los supervivientes a partir del cuarto día de estancia en la UR. En los supervivientes la disfunción de órganos se redujo gradualmente a partir del cuarto día de estancia según muestra la puntuación SOFA media registrada diariamente durante los primeros 10 días de estancia (fig. 1).
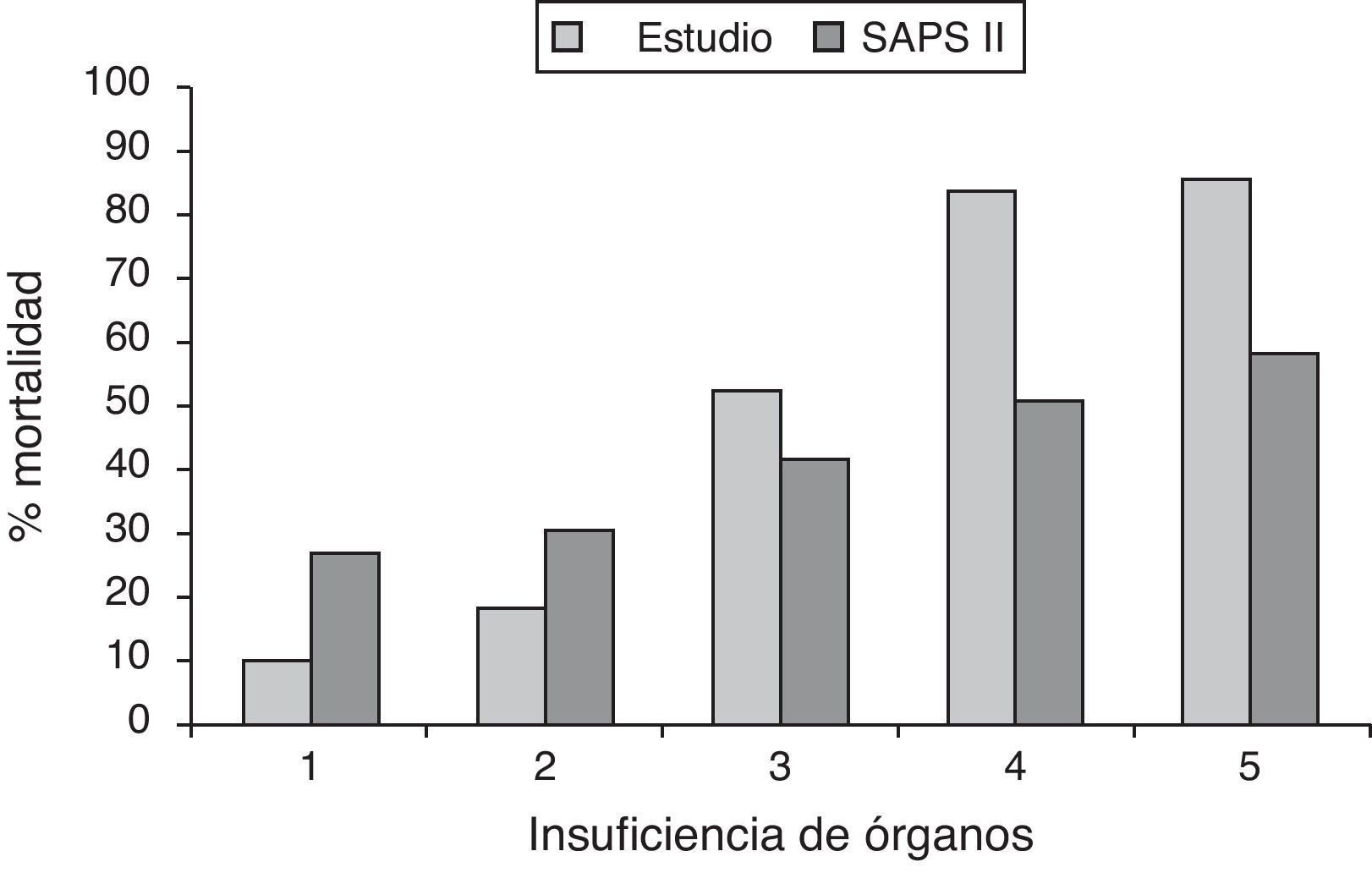
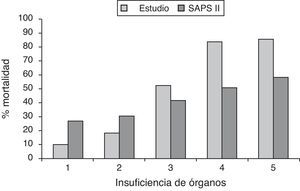
La figura 2 muestra la mortalidad según el número de órganos con insuficiencia comparada con la predicción de mortalidad según el SAPS II. Los resultados obtenidos muestran una mayor asociación de muerte con el fracaso multiorgánico (p=0,000) que con la gravedad al ingreso por SAPS II (p=0,016).
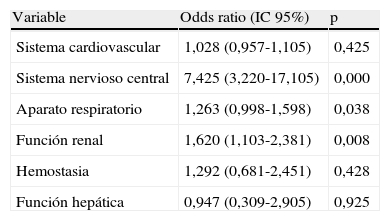
En el análisis univariante, las variables que se asociaron a una mayor mortalidad de manera estadísticamente significativa fueron: SAPS II (p=0,023), MODS (p=0,000), fallo sistema nervioso central (p=0,000) y puntuación SOFA correspondiente al cuarto día de estancia en la UR (p=0,012). Sin embargo, al efectuar el análisis multivariante, solo siguen manteniendo significación en relación con la mortalidad a los 28 días el SAPS II, SOFA cuarto día de estancia y el MODS. El análisis de regresión logística determinó que el fallo de sistema nervioso central (p=0,000), función renal (p=0,008) y sistema respiratorio (0,038) contribuyeron de manera significativa a la mortalidad a los 28 días (tabla 3).
Contribución a la mortalidad de la insuficiencia de órgano para cada uno de los 6 componentes de SOFA en pacientes con sepsis por peritonitis secundaria durante la estancia en la UR
| Variable | Odds ratio (IC 95%) | p |
| Sistema cardiovascular | 1,028 (0,957-1,105) | 0,425 |
| Sistema nervioso central | 7,425 (3,220-17,105) | 0,000 |
| Aparato respiratorio | 1,263 (0,998-1,598) | 0,038 |
| Función renal | 1,620 (1,103-2,381) | 0,008 |
| Hemostasia | 1,292 (0,681-2,451) | 0,428 |
| Función hepática | 0,947 (0,309-2,905) | 0,925 |
SOFA: Sequential Organ Failure Assessment; UR: unidad de Reanimación.
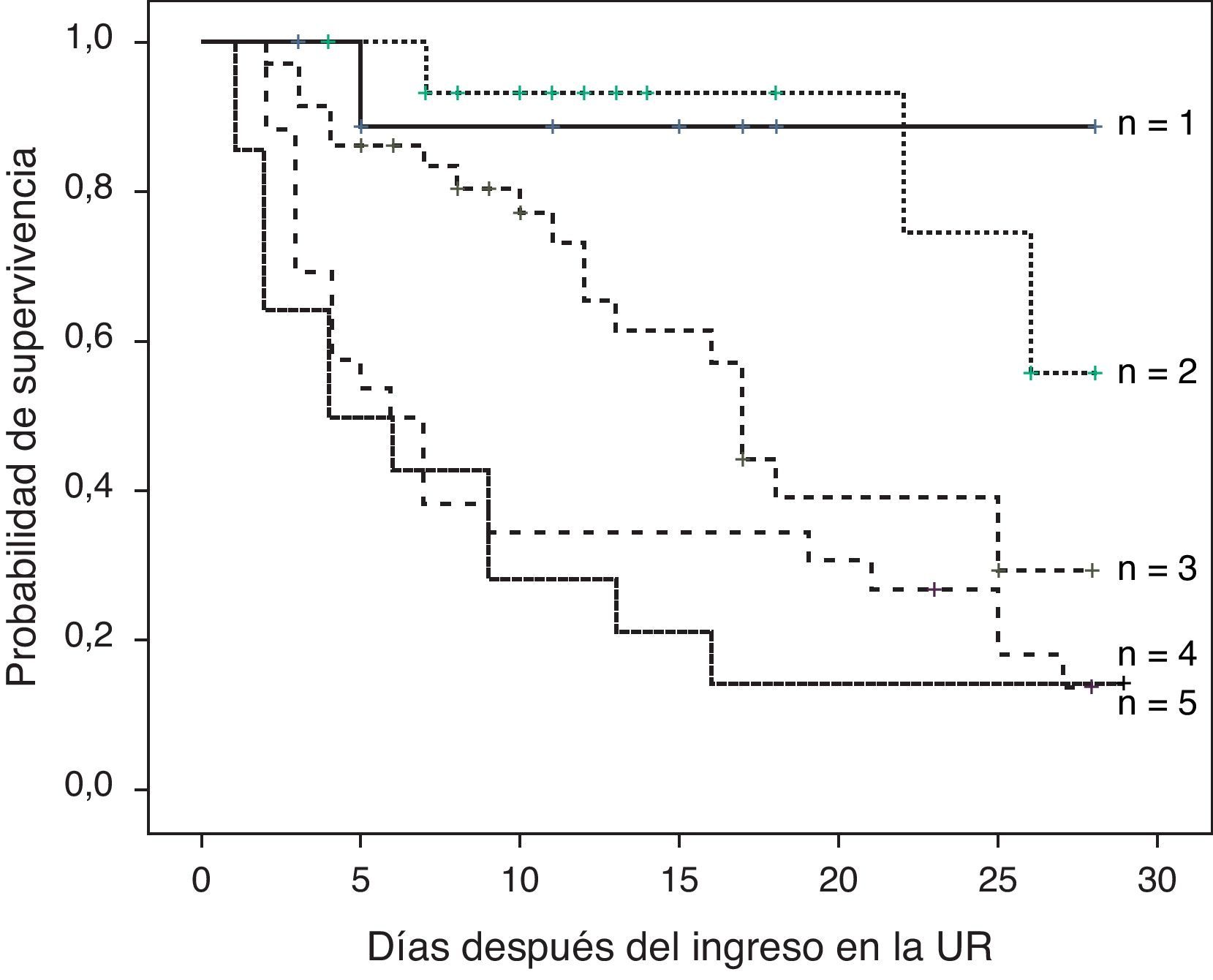
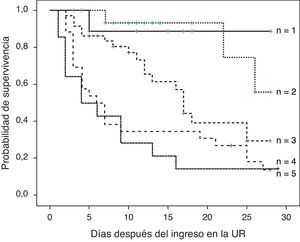
El análisis de supervivencia de Kaplan-Meier demostró que los subgrupos de pacientes con insuficiencia de 3 o más órganos tenían una tasa de supervivencia menor que los pacientes con insuficiencia de uno o 2 órganos (fig. 3).
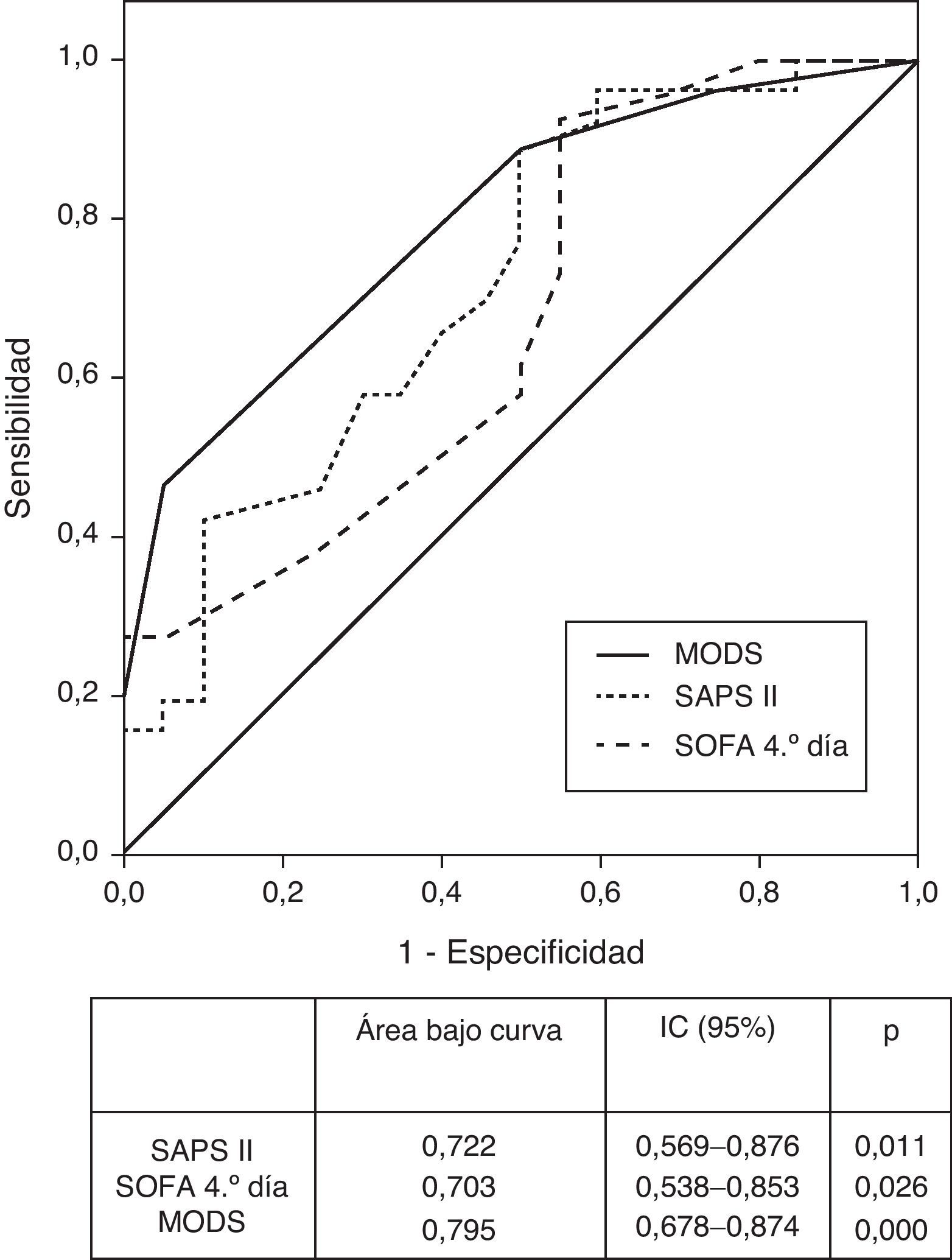
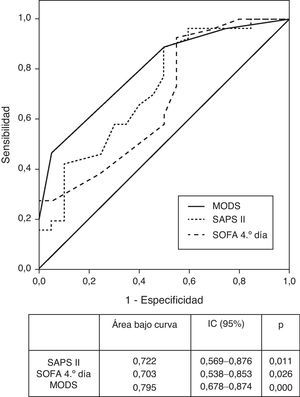
En la figura 4 se muestra el poder predictivo de riesgo de muerte, donde el área bajo la curva ROC expresa una capacidad predictiva de mortalidad del SOFA cuarto día de estancia del 0,703 (IC 95%, 0,538-0,853 y p=0,026); esta capacidad predictiva se incrementa con el aumento de la estancia, siendo al 10.° día del 0,871 (IC 95%, 0,746-0,996 y p=0,001). Cuando se consideró la puntuación SAPS II, el área bajo la curva ROC fue del 0,722 (IC 95%, 0,569-0,876 y p=0,011) y el mejor poder discriminativo se observó para el MODS con área bajo la curva ROC del 0,776 (IC 95%, 0,678-0,874 y p=0,000) (fig. 4).
DiscusiónLa peritonitis secundaria es una complicación grave frecuente en la UCI y en la UR. En un estudio multicéntrico europeo sobre sepsis en UCI, en el 22% de los pacientes la causa del estado séptico fue la infección intraabdominal12. Coincidiendo con otros autores13, en nuestro estudio la perforación de intestino grueso por tumor o dehiscencia de suturas fue la causa más frecuente de peritonitis secundaria y sepsis grave seguida en este estudio de la colecistitis aguda, perforación gastroduodenal, isquemia mesentérica y apendicitis aguda perforada. La infección de la cavidad peritoneal se produce por una flora polimicrobiana procedente de la luz intestinal constituida por gérmenes aerobios, anaerobios y hongos que desencadenan una respuesta inflamatoria local que incluye la expresión de citocinas proinflamatorias y reclutamiento de los macrófagos y neutrófilos en el lugar de infección14. La disfunción de órganos en los pacientes con peritonitis secundaria sería la expresión sistémica de los mediadores pro y antiinflamatorios que provocan cambios en la microcirculación y en la utilización celular de oxígeno10. Según estudios previos, las escalas de evaluación fisiológica como APACHE II, o sistemas de evaluación específica como el índice de peritonitis de Mannheim han sido de gran utilidad para establecer la gravedad de la enfermedad y el pronóstico en pacientes con sepsis grave de origen abdominal3,15,16. Sin embargo, ninguno de estos sistemas de evaluación de la gravedad valora el estado de salud previo del paciente con sepsis grave. El sistema APACHE II ha sido criticado como sistema de evaluación de la gravedad debido a que las variables fisiológicas que se correlacionan con la gravedad de la enfermedad pueden estar modificadas por el tratamiento de resucitación realizado en la sala de urgencias o en el quirófano antes de su ingreso en la UR. Asimismo, en un estudio reciente se ha demostrado una buena correlación entre el índice de peritonitis de Mannheim con el pronóstico de las peritonitis secundarias por perforación de colon17; sin embargo, según diversos autores no sucedería lo mismo con la peritonitis secundaria de otra etiología10,18. Tras una revisión sistemática, Minne et al. encontraron que la combinación de un sistema de evaluación de la gravedad en las primera 24 h del ingreso (APACHE II o SAPS II) y durante el curso del tratamiento de la enfermedad (SOFA) permiten una mejor discriminación entre mortalidad y supervivientes en pacientes sépticos que la utilización aislada o conjunta de los sistemas APACHE II y SAPS II19.
Según diversos autores, la puntuación SOFA durante los primeros días de ingreso en la UCI es un buen predictor evolutivo y de mortalidad, independiente de la puntuación inicial, en pacientes críticos. Del mismo modo, la puntuación máxima en la escala SOFA durante la estancia en UCI o UR es igualmente reflejo de un MODS significativamente relacionado con la mortalidad4,8–10. Un estudio multicéntrico demostró que puntuaciones máximas SOFA mayores de 15 se corresponden con una mortalidad superior al 90%, con una sensibilidad del 30,7%, una especificidad del 98,9% y una correcta clasificación del 84,2%4.
En nuestro estudio utilizamos los sistemas de valoración de la gravedad SAPS II y SOFA para predecir el riesgo de muerte en pacientes con sepsis grave por peritonitis secundaria ingresados en la UR. Los resultados obtenidos demuestran que los cambios en la severidad de la disfunción de órganos están estrechamente relacionados con la mortalidad, así como el aumento del SOFA diario refleja el empeoramiento de la función de los órganos durante la sepsis grave, sobre todo en los pacientes que fallecen. Asimismo, la puntuación SOFA al cuarto día de estancia fue mejor predictor de mortalidad que el SOFA en el primer día, proporcionado información pronóstica adicional la puntuación SOFA registrada diariamente y comparada con el registro inicial. Coincidiendo con otros autores, la contribución de cada órgano en la puntuación SOFA acumulada no fue similar, siendo la más notable la insuficiencia cardiovascular seguida del sistema respiratorio, función renal y sistema nervioso central4,20.
En nuestra población de pacientes la puntuación SOFA al cuarto día de estancia tiene una capacidad de discriminación significativa para agrupar a los pacientes con riesgo de fallecer, con valores de área bajo la curva ROC que indica buena exactitud. Asimismo, en el estudio de Ferreira et al.8 se comprueba cómo el incremento en la puntuación SOFA de las primeras 48h, reflejo de mala respuesta al tratamiento inicial, predice una mortalidad de al menos del 50%, independiente de la puntuación inicial. Igualmente, Vosylius et al.20 observaron que la puntuación SOFA al tercer día de estancia en UCI en pacientes con sepsis grave era mejor predictor de mortalidad que la insuficiencia orgánica aislada. De la misma manera, los resultados de este estudio son similares a publicaciones anteriores que reconocen al MODS como predictor de mortalidad, como muestra el valor de área bajo la curva ROC (buena exactitud), lo que indica que la mortalidad en nuestra serie guarda relación directa con el número de órganos afectados4.
En este estudio, el análisis de regresión logística multivariado reveló que el fallo del sistema nervioso central, función renal y sistema respiratorio se asociaron de forma independiente con la mortalidad a los 28 días. En los pacientes con sepsis grave se produce una reacción sistémica masiva al inicio de la enfermedad con vasodilatación profunda y desarrollo de un fracaso cardiovascular y un porcentaje elevado de pacientes con inflamación persistente fallecen rápidamente debido a MODS21. El MODS en los pacientes con sepsis grave por peritonitis secundaria se caracterizó por una incidencia de fracaso cardiovascular del 87% en el primer día de estancia y el desarrollo de una disfunción secuencial de los órganos vitales con afectación significativa del sistema nervioso central, función renal y respiratoria en los pacientes fallecidos.
La mortalidad a los 28 días observada en nuestra serie de pacientes fue elevada, pero dentro de los rangos publicados por otros autores22–24. Al igual que en la gran mayoría de las series publicadas sobre mortalidad en sepsis grave, la principal causa de muerte en nuestros pacientes fue la insuficiencia multiorgánica23,25. La relación entre la mortalidad y el número de insuficiencia de órganos en el momento del diagnóstico de sepsis grave y la progresión hacia el fracaso multiorgánico ha sido demostrada en diferentes estudios23,24. En el análisis multivariante comprobamos que el pronóstico de estos pacientes está claramente relacionado con la puntuación SOFA media al cuarto día de estancia en la UR, pero también con el nivel de gravedad sistémica (SAPS II) y el fracaso multiorgánico.
En resumen, en nuestra población de pacientes, la mortalidad a los 28 días alcanzó hasta el 55%, siendo el fracaso multiorgánico la principal causa de muerte. La evolución en la disfunción de órganos tras el ingreso en la UR recogida por medio de la puntuación SOFA media diaria mostró una alta precisión sobre la insuficiencia múltiple de órganos en los pacientes con sepsis grave de origen abdominal, siendo un buen predictor de mortalidad la puntuación SOFA media en el cuarto día de estancia. El fracaso del sistema nervioso central, función renal y sistema respiratorio fueron los factores de riesgo de mortalidad en este estudio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.