Evaluar la eficacia del entrenamiento muscular respiratorio en el destete de la ventilación mecánica y en la fuerza muscular respiratoria en pacientes en ventilación mecánica.
DiseñoEnsayo clínico controlado aleatorizado de grupos paralelos, doble ciego. Ámbito: unidad de cuidados intensivos de una clínica de iv nivel de la ciudad de Cali.
PacientesCiento veintiséis pacientes en ventilación mecánica por 48horas o más.
IntervencionesEl grupo experimental recibió todos los días un programa de entrenamiento muscular respiratorio con treshold, ajustado al 50% de la presión inspiratoria máxima adicional al cuidado estándar; el convencional recibió el cuidado estándar de fisioterapia respiratoria.
Variables de interés principalDestete de la ventilación mecánica. Otras variables evaluadas: fuerza muscular respiratoria, requerimiento de ventilación mecánica no invasiva y la frecuencia de reintubación.
AnálisisAnálisis por intención a tratar con todas las variables evaluadas y estratificado por condición de sepsis.
ResultadosNo se presentaron diferencias estadísticamente significativas en la mediana de tiempo de destete de la VM entre los grupos ni en la probabilidad de extubación entre los grupos (HR: 0,82; IC 95%: 0,55-1,20; p=0,29). La presión inspiratoria máxima se incrementó en el grupo experimental en promedio 9,43 (17.48) cmH2O y en el convencional 5,92 (11,90) cmH2O (p=0,48). La diferencia entre los promedios del cambio en la presión inspiratoria máxima fue 0,46 (p=0,83 IC 95%: –3,85 a –4,78).
ConclusionesEl entrenamiento muscular respiratorio no demostró eficacia en la disminución del periodo del destete de la VM ni en el incremento de la fuerza muscular respiratoria en la población estudiada. Estudio registrado en ClinicalTrials.gov (NCT02469064).
To evaluate the efficacy of respiratory muscular training in the weaning of mechanical ventilation and respiratory muscle strength in patients on mechanical ventilation of 48hours or more.
DesignRandomized controlled trial of parallel groups, double-blind. Ambit: Intensive Care Unit of a IV level clinic in the city of Cali.
Patients126 patients in mechanical ventilation for 48hours or more.
InterventionsThe experimental group received daily a respiratory muscle training program with treshold, adjusted to 50% of maximal inspiratory pressure, additional to standard care, conventional received standard care of respiratory physiotherapy.
Main interest variablesweaning of mechanical ventilation. Other variables evaluated: respiratory muscle strength, requirement of non-invasive mechanical ventilation and frequency of reintubation.
Analysisintention-to-treat analysis was performed with all variables evaluated and analysis stratified by sepsis condition.
ResultsThere were no statistically significant differences in the median weaning time of the MV between the groups or in the probability of extubation between groups (HR: 0.82 95% CI: 0.55-1.20 P=.29). The maximum inspiratory pressure was increased in the experimental group on average 9.43 (17.48) cmsH20 and in the conventional 5.92 (11.90) cmsH20 (P=.48). The difference between the means of change in maximal inspiratory pressure was 0.46 (P=.83 95%CI –3.85 to –4.78).
Conclusionsrespiratory muscle training did not demonstrate efficacy in the reduction of the weaning period of mechanical ventilation nor in the increase of respiratory muscle strength in the study population. Registered study at ClinicalTrials.gov (NCT02469064).
Aproximadamente el 35% de los pacientes que ingresan en unidades de cuidados intensivos (UCI) requieren ventilación mecánica (VM); una minoría de estos pacientes (20% a 30%) presenta dificultades en el destete, y de ellos cerca del 50% requiere VM por 7 días o más, así aproximadamente el 15% de los pacientes que ingresan en una UCI requiere VM prolongada1–3.
La VM prolongada expone a los pacientes a un mayor riesgo de neumonía asociada a la VM, isquemia traqueal, daño pulmonar y disfunción muscular diafragmática; la aparición de estas complicaciones incrementa el riesgo de mortalidad1,4–12. Adicionalmente, los pacientes que presentan dificultades en el destete consumen aproximadamente el 40% de los recursos de una UCI2,7,13.
La sepsis, condición presente en aproximadamente un 10,8% de los pacientes que ingresan en una UCI14, ha sido considerada como un factor determinante en el destete de la VM y en la fuerza de la musculatura respiratoria15–18. Charles Bolton et al. fueron los primeros en sugerirlo18, y posteriormente estudios retrospectivos y prospectivos han confirmado esta observación15,17.
Entre las estrategias terapéuticas empleadas para mejorar la fuerza muscular respiratoria en los pacientes con VM y facilitar el destete se ha considerado el entrenamiento muscular respiratorio (EMR). Esta técnica tiene como objetivo mejorar la fuerza y la resistencia de los músculos respiratorios. Son pocas las investigaciones que evalúan el EMR en pacientes con VM como técnica para facilitar el destete19–25.
A la fecha de realización de este estudio 4 ensayos clínicos habían evaluado la eficacia del EMR en términos del tiempo del destete de la VM22,26–28, solo 2 de ellos han reportado diferencias significativas en este tiempo y concluyen que la EMR lo disminuye28,29, mientras que los otros estudios no confirman tal hallazgo. Estos estudios difieren en la metodología empleada, en la técnica de EMR implementada y en las poblaciones estudiadas, adicionalmente presentan tamaños de muestra pequeños y ausencia de análisis multivariado.
Dado que en el ámbito colombiano no se han evaluado los efectos del EMR en los pacientes en VM, y que la evidencia internacional es contradictoria e inespecífica, este estudio tuvo como objetivo evaluar la eficacia del EMR en el destete de la VM y la fuerza muscular inspiratoria en pacientes sometidos a VM por 48 o más horas.
MetodologíaEnsayo clínico controlado aleatorizado de grupos paralelos, doble ciego. Criterios de inclusión: pacientes de 18 y más años con requerimiento de VM mayor o igual a 48horas que fueron hospitalizados en una UCI de 4.° nivel de una institución de salud de la ciudad de Cali, que hubieran manifestado la voluntad de participar en el estudio por medio de la firma del consentimiento informado; pacientes con primer evento de requerimiento de VM; intubados dentro de la institución de salud o en centros periféricos y remitidos hasta 12horas después de la intubación; PaO2>60mmHg con una FiO2≤0,5; PEEP<8cmH2O; RASS entre –1 y 0 y con presión arterial media mayor de 60mmHg en ausencia de soporte vasopresor o con requerimiento mínimo (dobutamina o dopamina<5 mcg/kg/min o epinefrina<1mcg/kg/min). Criterios de exclusión: pacientes con enfermedad neuromuscular progresiva; lesión del sistema nervioso central; lesión medular por encima de T5; enfermedad esquelética de la caja torácica o de la columna vertebral; pacientes que hubiesen recibido soporte ventilatorio domiciliario previo a la hospitalización; presencia excesiva de secreciones; traqueostomía o intubación nasotraqueal; mujeres en estado de gestación y pacientes infectados con gérmenes multirresistentes.
La investigación recibió la aprobación 022-013 del Comité de ética de la Universidad del Valle y 030-2014 del Comité de ética de la institución de salud donde se realizó el estudio.
El grupo control recibió el cuidado convencional de fisioterapia respiratoria en UCI, el cual consistía en fisioterapia respiratoria, terapia física y manejo de la VM. El grupo experimental recibió como tratamiento adicional un programa de EMR realizado con Threshold IMT (entrenador muscular respiratorio: Threshold IMT; Respironics Inc; Murrysville, PA, EE. UU.) todos los días 2 veces al día. Se realizaron 3 series de 6 a 10 repeticiones cada una, con 2minutos de descanso entre cada serie. La carga inicial de entrenamiento fue ajustada considerando el 50% de la presión inspiratoria máxima (Pimáx)29,30, y fue realizado por 4 fisioterapeutas, con dedicación exclusiva para el desarrollo del proyecto y con entrenamiento previo al proceso de recolección, quienes siguieron las directrices del manual operativo estandarizado diseñado previamente por los investigadores
La fuerza muscular respiratoria fue medida a través de la Pimáx de acuerdo con los protocolos descritos por la American Toracic Society y la European Respiratory Society; con un manovacuómetro digital Carefusión31 se realizaron mediciones de confiabilidad intra e interevaluador previo al proceso de recolección. La medición de la Pimáx se realizó en ambos grupos.
El destete de la VM fue definido como el periodo comprendido entre el inicio de VM en presión soporte (PS) con un nivel de PS<10cmH2O hasta la extubación. Para evaluar la fuerza muscular respiratoria se midió el cambio en la Pimáx. Se consideró destete fallido de la VM como el requerimiento de reintubación o muerte durante las primeras 48horas postextubación
Desenlace primario: destete de la VM. Desenlances secundarios: fuerza muscular respiratoria, frecuencia de destete fallido de la VM y requerimiento de VM no invasiva (VMNI) en cada grupo de tratamiento.
Para el cálculo del tamaño de muestra se tomó como variable respuesta el tiempo de destete de la VM, con una desviación estándar de 52,8horas y una diferencia esperada de 24horas en el tiempo de destete de la VM a favor del grupo experimental, según los datos del ensayo clínico controlado realizado por Condessa et al.26, un 10% de drop out, un poder del 80% y un error tipo alfa del 5% se requirieron 63 pacientes en cada grupo.
Se realizó una aleatorización estratificada por condición de sepsis, definida por la presencia de uno o más de los siguientes signos: fiebre (temperatura>38,3°C), hipotermia (temperatura<36°C), taquicardia (frecuencia cardiaca>90lpm), taquipnea (frecuencia respiratoria>40rpm), leucocitosis (leucocitos>12.000/μl), leucopenia (leucocitos<4.000/μl), estado mental alterado en pacientes con signos sugestivos de infección32. Posteriormente se realizó aleatorización por bloques no fijos, de tamaños variables de 4 y 6 individuos. La aleatorización se realizó en el programa Random allocation software for parallel group randomized trials, previo al ingreso del primer paciente. Dos fisioterapeutas realizaron la asignación de tratamiento. Las combinaciones de la intervención fueron organizadas por una persona externa en sobres cerrados de diferente color según la condición de la sepsis. Los sobres fueron numerados en la superficie exterior y se mantuvieron en 2 cajas selladas; estas se abrieron después de obtener el consentimiento informado.
Se realizó enmascaramiento del investigador principal y del equipo de trabajo de UCI. Para ello el proceso de recolección de datos y de implementación de la intervención estuvo a cargo de los 4 fisioterapeutas que hicieron parte del trabajo de campo, excluyendo al investigador principal, quienes realizaban las mediciones de la Pimáx y la implementación de la intervención en un tiempo definido previamente, por lo tanto la intervención en los 2 grupo tuvo la misma duración; adicionalmente la intervención se realizó con las cortinas de los cubículos de la UCI cerradas y el Threshold se mantuvo todo el tiempo guardado en una caja opaca sellada.
Análisis estadísticoSe realizó un análisis por intención a tratar y se construyeron modelos múltiples finales para cada una de las variables evaluadas.
La selección de las variables de los modelos finales se realizó seleccionando de cada modelo simple aquellas con valor p<0,2533, y para ello se utilizó el método de eliminación de variables (stepwise).Cada vez que se retiró una variable se sometió el modelo a la realización del lrtest. Con las variables que permanecieron en el modelo se evaluó la presencia de confusión y de interacción33.
El análisis univariado de las horas de destete de la VM se realizó con la prueba de Mann-Whitney. El análisis univariado de la probabilidad de extubación se realizó con análisis de sobrevivida (Kaplan-Meier), y la prueba de log rank; el análisis multivariado se realizó con regresión de COX33. Se evaluó el ajuste del modelo final obteniendo los residuales de Cox-Snell con la representación gráfica. La diferencia en el promedio de la Pimáx final entre los grupos fue analizada a través de la prueba «t», la diferencia en el promedio de la Pimáx al interior de cada grupo fue analizada a través de la prueba «t» pareada, para ello el cambio en la Pimáx al interior de cada grupo se consideró como la diferencia en el promedio Pimáx final y la Pimáx inicial. El análisis multivariado de cambio en la Pimáx (Pimáx inicial-Pimáx final) se realizó con regresión lineal. Se determinó la razón de oportunidades (OR) de destete fallido de la VM y de requerimiento de VMNI, el análisis multivariado de estas 2 variables se realizó mediante regresión logística. Se comparó el tiempo de requerimiento de VMNI entre los grupos través de la prueba Mann Withney.
ResultadosA continuación se muestran los resultados relacionados con la muestra total.
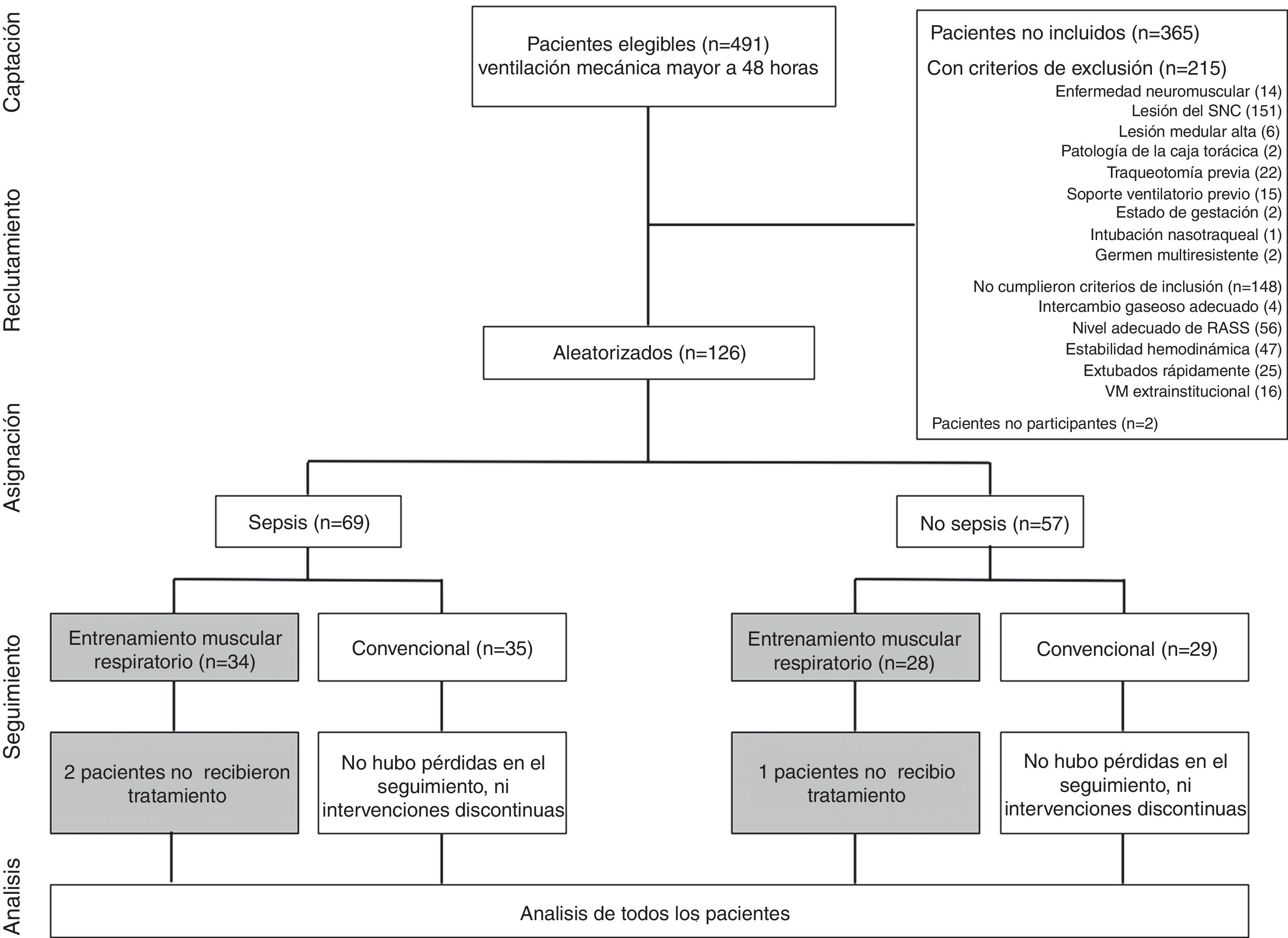
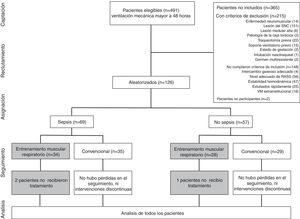
Características de los pacientes incluidos en el estudioLa figura 1 muestra el reclutamiento, la aleatorización y el flujo de participantes por grupo. Durante 7 meses 491 pacientes requirieron VM durante un periodo igual o mayor a 48horas; de estos, 215 presentaron criterios de exclusión, 148 no cumplieron criterios de inclusión: 2 pacientes decidieron no participar.
Se aleatorizaron 126 pacientes, 3 de ellos no cumplieron el protocolo al ser asignados al tratamiento experimental y recibir tratamiento convencional. Ningún paciente solicitó ser retirado del estudio y no se presentaron efectos adversos.
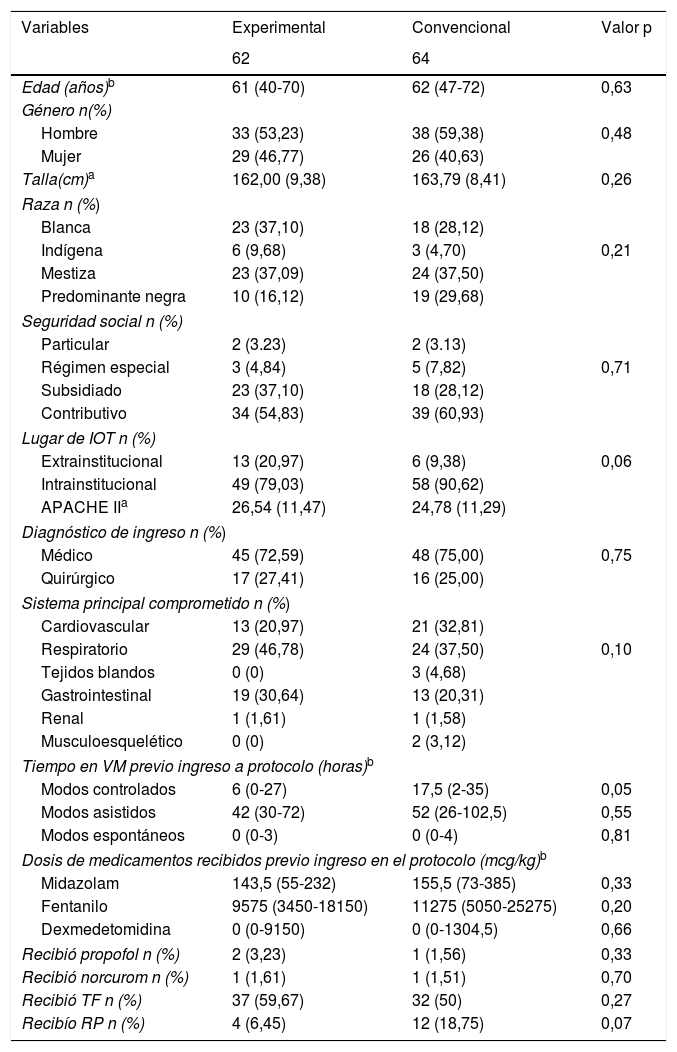
Las características de los pacientes en la línea de base de acuerdo al tratamiento asignado se presentan en la tabla 1.
Características de ingreso de los participantes según el tratamiento asignado
| Variables | Experimental | Convencional | Valor p |
|---|---|---|---|
| 62 | 64 | ||
| Edad (años)b | 61 (40-70) | 62 (47-72) | 0,63 |
| Género n(%) | |||
| Hombre | 33 (53,23) | 38 (59,38) | 0,48 |
| Mujer | 29 (46,77) | 26 (40,63) | |
| Talla(cm)a | 162,00 (9,38) | 163,79 (8,41) | 0,26 |
| Raza n (%) | |||
| Blanca | 23 (37,10) | 18 (28,12) | |
| Indígena | 6 (9,68) | 3 (4,70) | 0,21 |
| Mestiza | 23 (37,09) | 24 (37,50) | |
| Predominante negra | 10 (16,12) | 19 (29,68) | |
| Seguridad social n (%) | |||
| Particular | 2 (3.23) | 2 (3.13) | |
| Régimen especial | 3 (4,84) | 5 (7,82) | 0,71 |
| Subsidiado | 23 (37,10) | 18 (28,12) | |
| Contributivo | 34 (54,83) | 39 (60,93) | |
| Lugar de IOT n (%) | |||
| Extrainstitucional | 13 (20,97) | 6 (9,38) | 0,06 |
| Intrainstitucional | 49 (79,03) | 58 (90,62) | |
| APACHE IIa | 26,54 (11,47) | 24,78 (11,29) | |
| Diagnóstico de ingreso n (%) | |||
| Médico | 45 (72,59) | 48 (75,00) | 0,75 |
| Quirúrgico | 17 (27,41) | 16 (25,00) | |
| Sistema principal comprometido n (%) | |||
| Cardiovascular | 13 (20,97) | 21 (32,81) | |
| Respiratorio | 29 (46,78) | 24 (37,50) | 0,10 |
| Tejidos blandos | 0 (0) | 3 (4,68) | |
| Gastrointestinal | 19 (30,64) | 13 (20,31) | |
| Renal | 1 (1,61) | 1 (1,58) | |
| Musculoesquelético | 0 (0) | 2 (3,12) | |
| Tiempo en VM previo ingreso a protocolo (horas)b | |||
| Modos controlados | 6 (0-27) | 17,5 (2-35) | 0,05 |
| Modos asistidos | 42 (30-72) | 52 (26-102,5) | 0,55 |
| Modos espontáneos | 0 (0-3) | 0 (0-4) | 0,81 |
| Dosis de medicamentos recibidos previo ingreso en el protocolo (mcg/kg)b | |||
| Midazolam | 143,5 (55-232) | 155,5 (73-385) | 0,33 |
| Fentanilo | 9575 (3450-18150) | 11275 (5050-25275) | 0,20 |
| Dexmedetomidina | 0 (0-9150) | 0 (0-1304,5) | 0,66 |
| Recibió propofol n (%) | 2 (3,23) | 1 (1,56) | 0,33 |
| Recibió norcurom n (%) | 1 (1,61) | 1 (1,51) | 0,70 |
| Recibió TF n (%) | 37 (59,67) | 32 (50) | 0,27 |
| Recibío RP n (%) | 4 (6,45) | 12 (18,75) | 0,07 |
IOT: intubación orotraqueal; RP: rehabilitación pulmonar; TF: terapia física; VM: ventilación mecánica.
El promedio de edad fue de 57,49años (Me: 62, rango: 18 – 88), la talla promedio fue 162,90cm (Me: 163, rango: 145-185). Del total de participantes 71 fueron hombres y 55 mujeres, 107 pacientes fueron intubados a nivel intrainstitucional y 19 a nivel extrainstitucional, 93 pacientes ingresaron en la UCI con diagnóstico médico y 33 con diagnóstico quirúrgico; el tiempo promedio de VM previo al ingreso al protocolo fue 86,53 horas (Me: 66,5, rango: 49-314), el promedio de dosis de midazolam recibido previo al ingreso al protocolo fue 277,73mcg/kg (Me: 153, rango: 0-5200), el promedio de dosis de fentanilo recibido fue de 16113 mcg/kg (Me: 10075, rango: 0-153800), 3 y 2 pacientes recibieron goteo de propofol y norcurom previo al ingreso en el protocolo respectivamente, 69 pacientes recibieron terapia física y 16 recibieron rehabilitación pulmonar durante el seguimiento.
No se presentaron diferencias en las características clínicas y sociodemográficas entre los 2 pacientes que decidieron no participar y los pacientes ingresados en el estudio.
Destete de la ventilación mecánicaUn paciente del grupo de experimental no alcanzó a ser destetado de la VM por evolucionar con shock séptico; durante el seguimiento 3 pacientes necesitaron traqueostomía sin haber iniciado el destete de la VM, 2 de ellos pertenecían al grupo experimental y uno al grupo convencional.
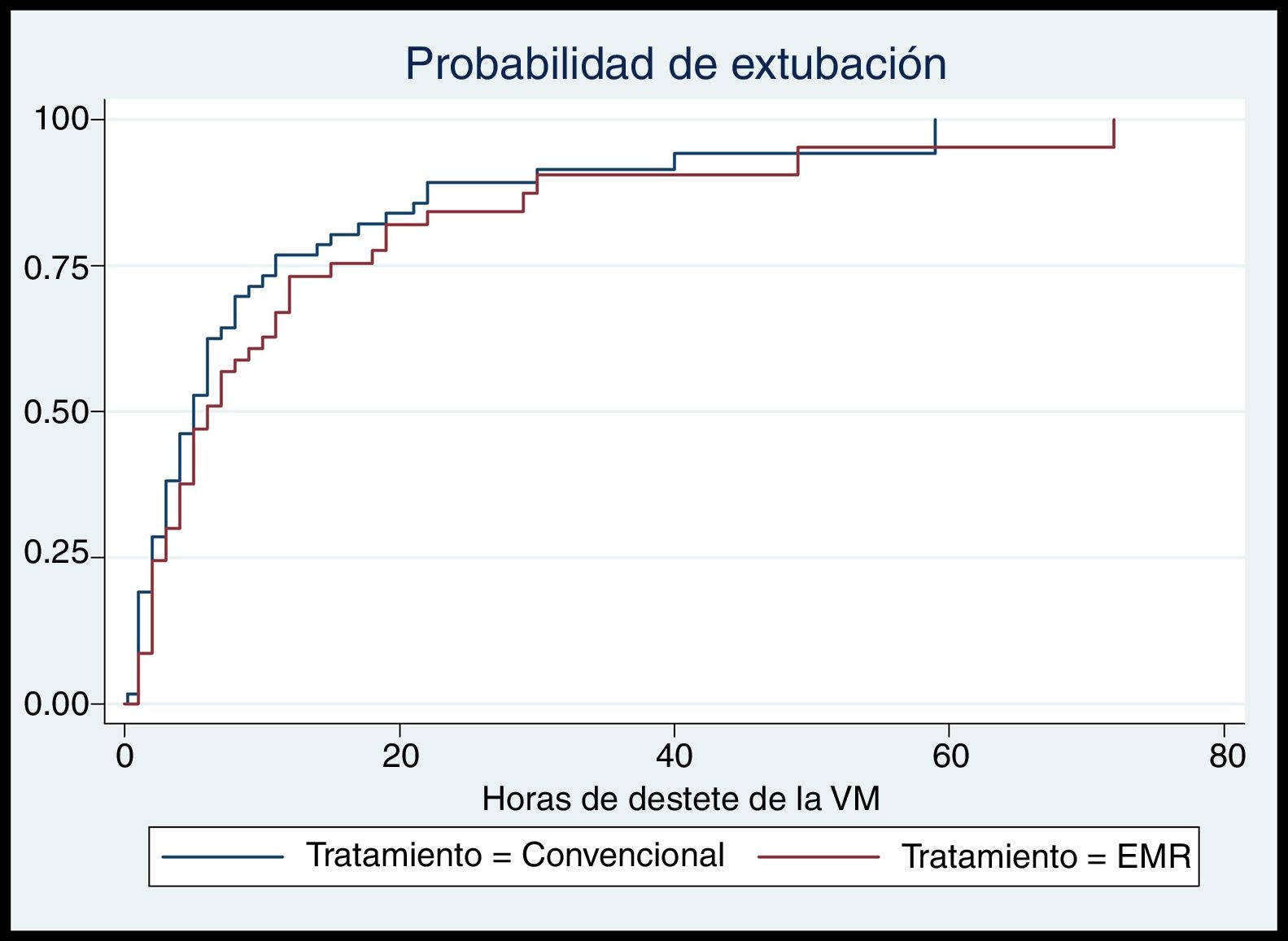
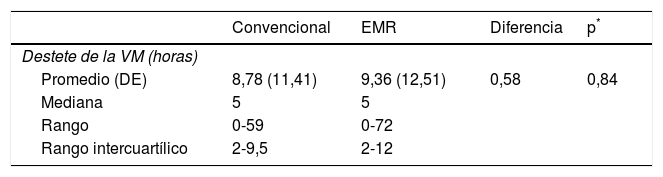
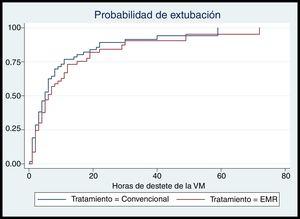
El tiempo del destete de la VM tuvo una duración promedio en el grupo convencional de 8,78 (11,41) horas, en el experimental la duración promedio fue de 9,36 (12,51) horas, en ambos grupos la mediana de destete de la VM fue de 5horas; en el grupo convencional el rango intercuartílico fue 2-9,5horas, en el grupo experimental fue de 2 a 12horas. No se presentaron diferencias estadísticamente significativas en la mediana de tiempo de destete de la VM entre los grupos (tabla 2). Tampoco se presentaron diferencias estadísticamente significativas en la probabilidad de extubación a lo largo del seguimiento según el tratamiento administrado (RP: 0,82; test de log rank=1,12, p=0,29) (fig. 2).
Tiempo de destete de la ventilación mecánica según el tratamiento administrado
| Convencional | EMR | Diferencia | p* | |
|---|---|---|---|---|
| Destete de la VM (horas) | ||||
| Promedio (DE) | 8,78 (11,41) | 9,36 (12,51) | 0,58 | 0,84 |
| Mediana | 5 | 5 | ||
| Rango | 0-59 | 0-72 | ||
| Rango intercuartílico | 2-9,5 | 2-12 | ||
EMR: entrenamiento muscular respiratorio; VM: ventilación mecánica.
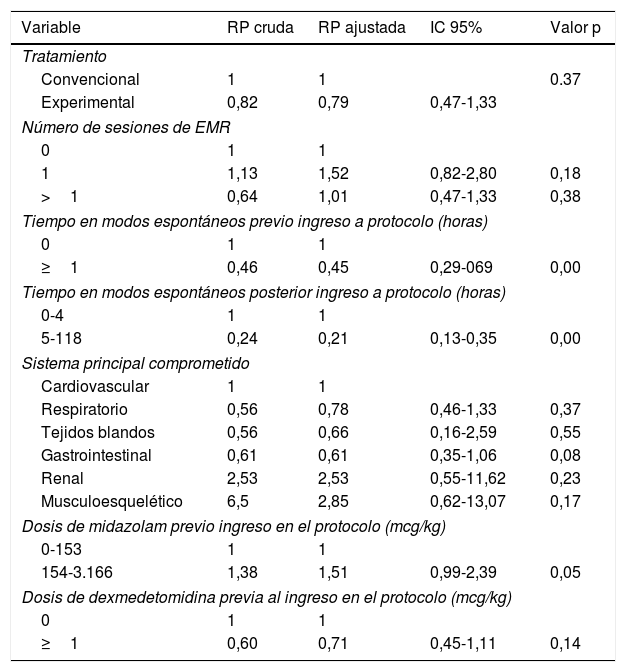
La tabla 3 presenta las razones de peligro crudas y ajustadas de extubación.
Razón de peligro cruda y ajustada de extubación
| Variable | RP cruda | RP ajustada | IC 95% | Valor p |
|---|---|---|---|---|
| Tratamiento | ||||
| Convencional | 1 | 1 | 0.37 | |
| Experimental | 0,82 | 0,79 | 0,47-1,33 | |
| Número de sesiones de EMR | ||||
| 0 | 1 | 1 | ||
| 1 | 1,13 | 1,52 | 0,82-2,80 | 0,18 |
| >1 | 0,64 | 1,01 | 0,47-1,33 | 0,38 |
| Tiempo en modos espontáneos previo ingreso a protocolo (horas) | ||||
| 0 | 1 | 1 | ||
| ≥1 | 0,46 | 0,45 | 0,29-069 | 0,00 |
| Tiempo en modos espontáneos posterior ingreso a protocolo (horas) | ||||
| 0-4 | 1 | 1 | ||
| 5-118 | 0,24 | 0,21 | 0,13-0,35 | 0,00 |
| Sistema principal comprometido | ||||
| Cardiovascular | 1 | 1 | ||
| Respiratorio | 0,56 | 0,78 | 0,46-1,33 | 0,37 |
| Tejidos blandos | 0,56 | 0,66 | 0,16-2,59 | 0,55 |
| Gastrointestinal | 0,61 | 0,61 | 0,35-1,06 | 0,08 |
| Renal | 2,53 | 2,53 | 0,55-11,62 | 0,23 |
| Musculoesquelético | 6,5 | 2,85 | 0,62-13,07 | 0,17 |
| Dosis de midazolam previo ingreso en el protocolo (mcg/kg) | ||||
| 0-153 | 1 | 1 | ||
| 154-3.166 | 1,38 | 1,51 | 0,99-2,39 | 0,05 |
| Dosis de dexmedetomidina previa al ingreso en el protocolo (mcg/kg) | ||||
| 0 | 1 | 1 | ||
| ≥1 | 0,60 | 0,71 | 0,45-1,11 | 0,14 |
EMR: entrenamiento muscular respiratorio.
Los análisis univariado y multivariado mostraron que un prolongado tiempo de destete de la VM se asoció con el tiempo en VM en modos espontáneos previo (≥1h) y posterior (5-118h) al ingreso en el protocolo.
Cambio en la presión inspiratoria máximaVeinticuatro pacientes no alcanzaron una medición de la Pimáx final, de ellos 14 pertenecían al grupo experimental y 10 al grupo convencional; este resultado se analizó en 102 pacientes.
La tabla 4 describe el cambio en la Pimáx al interior de cada grupo y la diferencia de cambio en la Pimáx entre los grupos. Se presentaron diferencias estadísticamente significativas entre Pimáx final y Pimáx inicial al interior de cada grupo (p<0,05), así en el grupo experimental la Pimáx se incrementó 9,43cmH2O, y en el convencional se incrementó 5,92cmH2O. No se presentaron diferencias estadísticamente significativas entre los promedio de cambios en la Pimáx entre los grupos (p=0,48).
Cambio en la presión inspiratoria máxima según el tratamiento asignado
| Parámetro | Cambio en la Pimáx al interior de cada grupo | Diferencia entre grupos | ||||
|---|---|---|---|---|---|---|
| Media (DE) | Experimental N=48 | p | Convencional N=54 | p | N=48 | p |
| 9,43 (17,48) | 0,00a | 5,92 (11,90) | 0,001a | 3,51 (14,78) | 0,48b | |
Pimáx. Presión inspiratoria máxima.
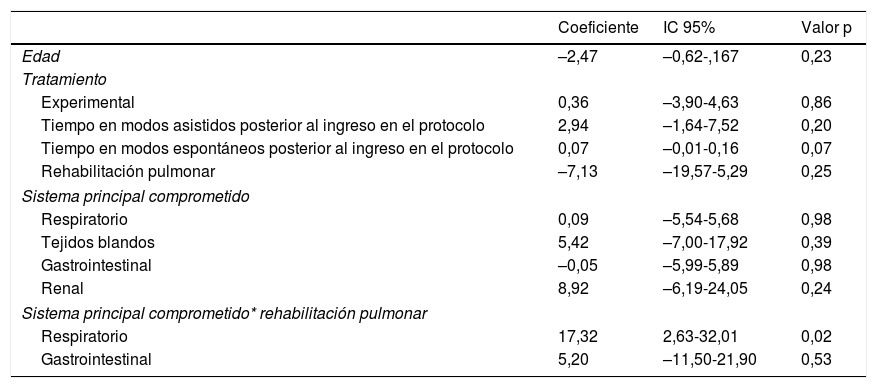
No se encontró asociación entre el promedio del cambio en la Pimáx y el tratamiento asignado. El modelo final mostró que un incremento significativo de la Pimáx se encontraba asociado con la interacción entre el sistema principal comprometido y rehabilitación pulmonar (p<0,05) (tabla 5).
Modelo múltiple final cambio en la presión inspiratoria máxima
| Coeficiente | IC 95% | Valor p | |
|---|---|---|---|
| Edad | –2,47 | –0,62-,167 | 0,23 |
| Tratamiento | |||
| Experimental | 0,36 | –3,90-4,63 | 0,86 |
| Tiempo en modos asistidos posterior al ingreso en el protocolo | 2,94 | –1,64-7,52 | 0,20 |
| Tiempo en modos espontáneos posterior al ingreso en el protocolo | 0,07 | –0,01-0,16 | 0,07 |
| Rehabilitación pulmonar | –7,13 | –19,57-5,29 | 0,25 |
| Sistema principal comprometido | |||
| Respiratorio | 0,09 | –5,54-5,68 | 0,98 |
| Tejidos blandos | 5,42 | –7,00-17,92 | 0,39 |
| Gastrointestinal | –0,05 | –5,99-5,89 | 0,98 |
| Renal | 8,92 | –6,19-24,05 | 0,24 |
| Sistema principal comprometido* rehabilitación pulmonar | |||
| Respiratorio | 17,32 | 2,63-32,01 | 0,02 |
| Gastrointestinal | 5,20 | –11,50-21,90 | 0,53 |
Del grupo experimental 15 pacientes (24,19%) presentaron destete fallido de la VM y del grupo convencional 16 (25%); estas diferencias no fueron significativas (p=0,54).
El análisis univariado y multivariado mostró que el destete fallido de la VM se asoció con la puntuación del APACHE (0-24) y el tiempo en VM en modos espontáneos (≥1) posterior al ingreso en el protocolo (p<0,05). No se encontró asociación entre la oportunidad de destete fallido y el tratamiento asignado.
Requerimiento de ventilación mecánica no invasivaEn el grupo experimental 33 pacientes (64,71%) recibieron manejo con VMNI, con una mediana de duración de 5 (4-13) horas; en el grupo convencional 38 pacientes (64,41%) recibieron manejo con VMNI, con una mediana de duración de 7,5 (4-11) horas; estas diferencias no fueron significativas (p>0,05).
En el análisis univariado y multivariado no se encontró asociación entre la oportunidad de requerimiento de VMNI y el tratamiento asignado.
DiscusiónA nivel nacional este es el primer ECC que investiga la eficacia del EMR en pacientes en VM mayor o igual a 48horas en el destete de la VM y la fuerza muscular respiratoria con enmascaramiento de los investigadores, del personal clínico y con una estimación del tamaño de la muestra basado en el tiempo de destete de la VM, al ser considerado el indicador más útil para los pacientes y el personal clínico. Los resultados no mostraron diferencias significativas en el tiempo de destete de la VM entre los grupos. El análisis de sobrevida mostró que la probabilidad de extubación no está asociada con el tratamiento administrado.
Los pacientes del grupo experimental (n=62) recibieron de una a 14 sesiones de EMR; el 50% de ellos recibió de 3 a 14 sesiones de EMR, esto debido al periodo corto de VM que los pacientes recibieron una vez que cumplían los criterios de inclusión. Algunos estudios han mostrado que es necesario como mínimo 10 días de entrenamiento muscular para incrementar la fuerza de la musculatura de las extremidades con una repercusión clínica importante34. El comportamiento de la musculatura inspiratoria es similar: se ha descrito que se requiere alrededor de 14 días de EMR para generar cambios significativos en la fuerza muscular, como proliferación de las fibras musculares tipo i y ii de los músculos intercostales, e incremento de la perfusión muscular inspiratoria30,35. Probablemente los pacientes no recibieron el número requerido de sesiones de EMR para generar cambios clínicos significativos.
Se encontró asociación entre un prolongado destete de la VM y tiempo en VM en modos espontáneos previo y posterior al ingreso en el protocolo. La VM en modos espontáneos ha sido sugerida como una estrategia terapéutica para prevenir la disfunción muscular respiratoria, y así disminuir el tiempo de VM36–38. Sin embargo, solo los modos parciales (asistidos/espontáneos) con bajos niveles de asistencia previenen la disfunción muscular respiratoria, y en ese sentido permiten acelerar el destete de la VM, mientras que los altos niveles de asistencia en las modalidades ventilatorias parciales (asistidos/espontáneos) son igualmente perjudiciales a la VM controlada y producen así disfunción muscular diafragmática, mayor número de asincronías ventilatorias y prolongación del tiempo de destete38–40. En este estudio el tiempo de VM en presión soporte por niveles específicos de presión no fue cuantificado; sin embargo, dada la definición operativa de periodo de destete de la VM el tiempo promedio de VM en presión soporte (11,1±18h en el grupo convencional, 17,26±34,92h en el grupo experimental) y el tiempo promedio de destete de la VM (8,78±11,41h en el grupo convencional 9,36±12,51 horas en el grupo experimental) se asume que los pacientes recibieron VM con niveles de presión soporte por encima de 10cmH2O, explicando así los hallazgos encontrados.
Cuatro ensayos clínicos han evaluado la eficacia del EMR en términos de tiempo de destete de la VM22,26–28; hasta el momento solo 2 de ellos han reportado diferencias estadísticamente significativas en el tiempo de destete de la VM a favor del grupo experimental27,28. Las conclusiones de estos estudios se ven limitadas por el pequeño tamaño de la muestra, la ausencia de enmascaramiento del grupo encargado de intervenir a los pacientes, de una definición precisa del tiempo de destete de la VM y de análisis multivariados.
Con relación al cambio en la Pimáx los resultados no mostraron diferencias significativas en la mediana de cambio en la Pimáx entre los grupos. En el modelo de regresión lineal final de cambio en la Pimáx la variable de interacción sistema respiratorio comprometido y rehabilitación pulmonar muestra significación estadística (p de interacción=0,01; IC 95%: 4,25-34,4), esto puede estar relacionado con intervenciones específicas de la rehabilitación pulmonar que pueden influir con cambios en la fuerza de la musculatura respiratoria y que actúan preferiblemente en los pacientes con enfermedad respiratoria, pacientes en los cuales la indicación de rehabilitación pulmonar se hace más evidente36.
Cuatro4 ECC han reportado resultados de Pimáx20,22,26–28, 3 de ellos reportaron diferencias significativas en el cambio en la Pimáx entre los grupos a favor del grupo experimental20,26,28. Las diferencias en los resultados entre los estudios pueden deberse a las diferencias en los protocolos de EMR y a diferencias en las características de la población de estudio.
El protocolo de EMR realizado por Caruso et al. se realizó a través de ajustes de la sensibilidad del ventilador22. Los otros estudios usaron el dispositivo Threshold, pero con diferentes niveles de carga20,26–28. La presente investigación utilizó un nivel de carga del 50% de la Pimáx, la cual, de forma similar al estudio de Condessa et al., era evaluada a través de mediciones de la Pimáx realizadas diariamente. Este nivel de carga corresponde al más alto hasta ahora reportado en los ECC19; sin embargo, no se encontraron diferencias significativas en el cambio en la Pimáx entre los grupos, lo cual pudo estar relacionado con la frecuencia de sesiones de EMR recibidas por los pacientes del grupo experimental, la cual no fue suficiente para generar cambios clínicos significativos.
La oportunidad de destete fallido no se asoció con el tratamiento administrado (OR: 0,96, p=0,95; IC 95%: 0,36-2,56). El fallo en el destete de la VM es un evento multifactorial en el cual se involucran condiciones como la integridad respiratoria y cardiovascular, la competencia neuromuscular, las condiciones psicológicas y el estado nutricional entre otros factores41; todas estas condiciones no fueron evaluadas en la presente investigación, dadas las dificultades de medición en las UCI. Del grupo experimental 15 pacientes (24,19%) presentaron destete fallido de la VM, del grupo convencional 16 (25%) presentaron este evento (p=0,54). La incidencia de destete fallido ha sido reportada con valores que van del 26% al 42%41–46, por lo que los resultados del presente estudio se asemejan a lo reportado.
El requerimiento de VMNI no se asoció con el tratamiento administrado. No se presentaron diferencias estadísticamente significativas en la mediana de requerimiento de VMNI entre los grupos. Esteban et al. reportan que el 10% de los pacientes que son extubados requiere manejo con VMNI postextubación4, así la proporción de pacientes que requirieron VMNI en el presente estudio fue mayor a lo reportado en la literatura, lo cual puede estar relacionado con protocolos de manejo a nivel institucional.
Las fortalezas metodológicas del estudio están relacionadas con las estrategias implementadas para disminuir la posibilidad de sesgos de selección y de información, y para controlar factores de confusión, tales como el doble enmascaramiento, el control de calidad realizado a los instrumentos de medición y los procesos de recolección de información y el análisis de la información. La validez externa es alta, ya que todos los pacientes que cumplieron con los criterios de inclusión fueron aleatorizados e incluidos en el estudio, y adicionalmente al ser la intervención evaluada realizada en el ámbito intrahospitalario. La adherencia al tratamiento se garantizó en la mayoría de los pacientes, así 123 pacientes finalizaron el seguimiento hasta alcanzar el punto final principal definido. Las características de los pacientes que decidieron no participar no difirieron de las características de los pacientes incluidos, evidenciando así la ausencia de sesgo de selección.
Hasta la fecha este es el estudio con mayor tamaño de muestra (n=126) y el único que ha realizado análisis de supervivencia a través de regresión de Cox, logrando así incluir en el análisis a los pacientes censurados e identificando las variables que influyen en el desenlace principal evaluado.
La limitación principal del estudio fue el corto periodo de EMR. Esto en relación con las características de la población elegible y con los protocolos institucionales de manejo ventilatorio, puesto que una vez que los pacientes cumplían con los criterios de inclusión iniciaban el proceso de destete de la VM, y por lo tanto se extubaron tempranamente, lo que sugiere la ausencia de disfunción muscular respiratoria asociada a la VM y no dependencia a la VM. Así, se asume que los pacientes que probablemente se beneficien son aquellos en los cuales la disfunción muscular respiratoria sea evidente.
Esta investigación es un marco de referencia a nivel nacional y local. Dado que los resultados no evidencian eficacia del EMR en el destete de la VM y en la fuerza muscular respiratoria, no es posible recomendar la intervención mencionada en esta población.
Los resultados demostraron la relación negativa entre el tiempo de VM en modos espontáneos con nivel alto de asistencia ventilatoria y el destete de la VM, lo cual sugiere la incursión de modalidades ventilatorias espontáneas con niveles de presión soporte menor a 10cmH2O.
A pesar de no existir resultados con significación estadística, desde la perspectiva clínica es plausible considerar que podría existir un potencial beneficio del EMR como estrategia de prevención de la disfunción muscular respiratoria asociada a la VM en los pacientes con enfermedad de origen respiratorio que simultáneamente reciban rehabilitación pulmonar; esto considerando que en este estudio este grupo de pacientes incrementó la fuerza muscular respiratoria.
Se recomiendan futuras investigaciones en las que se incluyan pacientes con destete difícil y con VM prolongada, en los cuales la disfunción muscular respiratoria se hace evidente, y evaluarse el resultado del EMR con mayor tiempo de seguimiento. Dado que esta población representa una minoría de los pacientes que requieren VM en elinterior de la UCI en la institución de interés de este estudio, la factibilidad de esta investigación se hace posible a nivel multicéntrico.
ConclusionesAl evaluar la eficacia del EMR no se presentaron diferencias estadísticamente significativas en el periodo de destete de la VM y en el cambio en la fuerza muscular respiratoria entre el grupo experimental y el grupo control.
El tiempo en VM en modos espontáneos con niveles altos de asistencia ventilatoria prolongan el destete de la VM en pacientes con requerimiento de VM mayor a 48horas. En este sentido es necesario considerar la utilidad de la intervención oportuna de los pacientes cuyo sistema principal comprometido es el respiratorio para incrementar la fuerza muscular respiratoria.
No se presentaron diferencias estadísticamente significativas en la oportunidad de destete fallido de la VM y de requerimiento de VMNI entre los pacientes pertenecientes al grupo experimental y grupo control.
FinanciaciónInvestigación financiada por la Vicerrectora de Investigación de la Universidad del Valle.
AutoríaConcepto/idea/diseño de investigación: L.M. Sandoval, I.C. Casas, E.C. Wilches, A.F. García
Escritura: L.M. Sandoval, I.C. Casas, E.C. Wilches, A. F. García
Coordinación de la recopilación y análisis de datos: L.M. Sandoval, I.C. Casas
Gestión de proyectos: L.M. Sandoval, E.C. Wilches, A.F. García
Adquisición de fondos: L.M. Sandoval, E.C. Wilches, A.F. García
Revisión del manuscrito antes de la presentación: M. Sandoval, I.C. Casas, E.C. Wilches, A.F. García
Conflicto de interesesNinguno declarado.
A la Fundación Valle del Líli, por permitir que el proyecto se llevara a cabo en sus instalaciones.