Pocos estudios han evaluado el impacto en el diagnóstico y tratamiento de la ecocardiografía transtorácica básica en los pacientes postoperados de cirugía cardíaca. El objetivo de nuestro estudio fue valorar el impacto de la ecocardiografía transtorácica básica en el manejo diagnóstico y terapéutico de estos pacientes.
DiseñoDurante 18 meses se estudiaron prospectivamente todos los pacientes postoperados de cirugía cardíaca que ingresaron en el Servicio de Medicina Intensiva de un hospital universitario. Se realizó una valoración clínica a todos ellos para establecer un diagnóstico y un tratamiento inicial. Se realizó una ecocardiografía transtorácica básica para valoración diagnóstica, que se comparó con la valoración clínica. En caso de discrepancia, se valoró cambiar el tratamiento en función a la ecocardiografía y se evaluó la respuesta terapéutica. Se realizó un análisis descriptivo de los hallazgos.
ResultadosSe incluyeron 136 pacientes y se realizaron 203 ecocardiografías. La ecocardiografía transtorácica difería del diagnóstico inicial en 101 (49,8%) ecocardiografías. En 56 de estas (55,44%) se obtuvo un diagnóstico alternativo, lo que comportó un cambio en el tratamiento en 30pacientes (53,6%). Encontramos mejoría clínica significativa en 26 de estos pacientes (86,76%) en los siguientes 30-60min.
ConclusionesLa ecocardiografía transtorácica básica es útil en el manejo diagnóstico y terapéutico de los pacientes postoperados de cirugía cardíaca. En la mitad de las ecocardiografías realizadas no se pudo confirmar el diagnóstico clínico. En la mayoría de los pacientes en que observamos cambio en el diagnóstico debido a la ecocardiografía, se observó mejoría clínica tras el cambio de tratamiento.
Few studies have evaluated the impact in diagnosis and therapeutic management of basic transthoracic echocardiography in postoperated cardiac surgery. The aim of our study was to evaluate the impact of basic transthoracic echocardiography in the management of this kind of patients.
DesignOver an 18-month period, we prospectively studied all patients admitted to a university hospital Intensive Care Unit following heart surgery. We evaluated clinically all of them to establish a diagnosis and an initial treatment. We performed basic transthoracic echocardiography for a diagnosis evaluation that was compared with clinical diagnosis. If they differed, we assessed to change treatment and evaluate the therapeutic response. We performed a descriptive analysis.
ResultsWe included 136 patients and performed 203 echocardiographies. Transthoracic echocardiography differed of initial diagnosis in 101 (49.8%) echocardiographies. In 56 of these echocardiographies (55.44%), we could give an alternative diagnosis with a change in the treatment in 30patients (53,6%). We found clinical improvement in 26 patients (86.76%) in the following 30-60minutes.
ConclusionsBasic transthoracic echocardiography is useful in diagnostic and therapeutic management of postoperative cardiac surgery patients. We could not confirm the clinical diagnosis in half of the performed echocardiographies. In most patients in whom we observe a change in the diagnosis due to echocardiography, we observed a clinical improvement after changing the treatment.
La ecocardiografía transtorácica es una modalidad de imagen no invasiva muy útil en la valoración de los pacientes críticos. Esta técnica proporciona a pie de cama y en tiempo real una imagen dinámica del corazón y ofrece, además, información morfológica y funcional. A menudo los datos aportados por la ecocardiografía permiten identificar las causas de shock y proporcionan una guía útil para evaluar el tratamiento instaurado. Algunos estudios han demostrado que la ecocardiografía puede aportar información que conduce a modificar de forma significativa el tratamiento de hasta el 52% de los enfermos críticos, y por ello algunos grupos han desarrollado protocolos de ecocardiografía transtorácica para optimizar el tratamiento de estos pacientes1-20.
Aunque se han realizado estudios que evalúan la utilidad de la ecocardiografía transesofágica realizada por intensivistas en los pacientes críticos21,22, existen muy pocos estudios que valoren la aplicabilidad y el impacto de la ecocardiografía transtorácica básica dirigida a objetivos concretos en el manejo diagnóstico y terapéutico de los pacientes postoperados de cirugía cardíaca1,23-25. Recientemente, nuestro grupo ha publicado un estudio donde se observa que se puede realizar una ecocardiografía transtorácica básica en la mayoría de pacientes postoperados de cirugía cardíaca obteniendo datos interpretables26.
El objetivo de nuestro estudio fue evaluar de forma prospectiva el impacto de la ecocardiografía transtorácica básica dirigida a objetivos concretos en el diagnóstico y tratamiento de los pacientes postoperados de cirugía cardíaca.
Material y métodosSelección de pacientesEl estudio se realizó en el Servicio de Medicina Intensiva de un hospital general universitario, dotado de 16 camas polivalentes, en el que ingresan 100 pacientes postoperados de cirugía cardíaca al año.
Se incluyeron todos los pacientes mayores de 18años sometidos a cirugía cardíaca que ingresaron consecutivamente en la UCI entre noviembre de 2014 y abril de 2016, si estaba disponible en presencia física un intensivista con formación ecocardiográfica básica acreditada.
El protocolo de estudio fue revisado y aprobado por el Comité Ético de Investigación Clínica del hospital. Todos los pacientes incluidos en el estudio firmaron su consentimiento informado para su participación.
Características clínicasEn el momento del ingreso se registraron los datos demográficos generales, el motivo de ingreso, las principales comorbilidades, los índices de gravedad (APACHEII, EuroSCORE) y los datos hemodinámicos y ecocardiográficos previos a la cirugía, si estaban disponibles.
Se realizó una valoración clínica y hemodinámica del paciente para establecer un diagnóstico inicial por parte de uno de los seis intensivistas del servicio según la práctica clínica habitual en el postoperado de cirugía cardíaca: hipovolemia, disfunción ventricular izquierda, disfunción ventricular derecha, disfunción biventricular, vasoplejía, insuficiencia mitral masiva o taponamiento, y se pautó un tratamiento en función de ese diagnóstico.
Ecocardiografía básicaTras la valoración clínica inicial y dentro de las primeras 8h de ingreso, otro intensivista con formación en ecocardiografía básica realizó una ecocardiografía transtorácica básica. En el momento de la exploración se recogió la presencia de ventilación mecánica, el uso de fármacos vasoactivos y los parámetros hemodinámicos (frecuencia cardíaca, presión arterial, saturación venosa central, niveles de lactato).
Se repitió un examen ecocardiográfico diariamente si existían signos de hipoperfusión tisular (hipotensión arterial, signos de mala perfusión periférica, lactatos elevados, oliguria). El ecocardiografista desconocía la orientación diagnóstica inicial.
El análisis ecocardiográfico consistió en una valoración sistemática de las proyecciones paraesternal eje largo y eje corto, apical cuatro cámaras, subcostal cuatro cámaras con visualización de la vena cava inferior. Para cada ventana acústica se graduó la dificultad de obtención de la imagen como alta o baja. Todas las exploraciones se realizaron con la sonda de ecocardiograma M5S-D de 1,5-4,6MHz del ecógrafo Vivid-e de General Electrics, disponible las 24h en la UCI de nuestro centro.
Los datos ecocardiográficos analizados fueron:
- 1)
Ventrículo izquierdo: tamaño visual que se definía como normal o dilatado, función sistólica visual clasificada como normal (≥50%) o deprimida (<50%) y patrón de contracción homogéneo o heterogéneo.
- 2)
Ventrículo derecho: tamaño visual clasificado como normal o dilatado y función sistólica visual (normal o deprimida).
- 3)
Válvulas: presencia de insuficiencia mitral masiva.
- 4)
Vena cava inferior: clasificada como normal, dilatada o no visualizada.
- 5)
Líquido pericárdico con o sin taponamiento cardíaco clasificado como presente o ausente.
Los patrones ecocardiográficos se definieron como5,6,27:
- -
Hipovolemia grave: ventrículos hiperdinámicos y pequeños, con obliteración de la cavidad del ventrículo izquierdo (kissing walls) y vena cava inferior pequeña con gran variación con los movimientos respiratorios (en ventilación mecánica, vena cava inferior <1,5cm con colapso >50%; en ventilación espontánea, vena cava inferior <1cm con colapso >50%).
- -
Fallo de ventrículo izquierdo: reducción de la movilidad global del ventrículo izquierdo, patrón de contractilidad heterogénea que sugeriría isquemia miocárdica o dilatación de la cavidad del ventrículo izquierdo que sugeriría enfermedad cardíaca crónica.
- -
Fallo de ventrículo derecho: dilatación del ventrículo derecho y movimiento paradójico del tabique interventricular, que en el paciente crítico se asocia básicamente al síndrome de distrés respiratorio agudo o a un tromboembolismo pulmonar grave. La dilatación del ventrículo derecho aislada es sugestiva de infarto del ventrículo derecho. Otros hallazgos asociados pueden ser una vena cava inferior dilatada y sin colapso.
- -
Taponamiento: presencia de derrame pericárdico con colapso diastólico de aurícula y ventrículo derechos, vena cava inferior dilatada y sin colapso respiratorio en respiración espontánea.
- -
Insuficiencia mitral masiva aguda: ventrículo izquierdo de tamaño normal (lo que indica valvulopatía aguda), función sistólica del ventrículo izquierdo normal o hiperdinámica por sobrecarga de volumen del ventrículo izquierdo y flujo regurgitante masivo en Doppler color.
Todas las exploraciones fueron registradas digitalmente y valoradas posteriormente por un intensivista con grado avanzado en ecocardiografía transtorácica (A.O.), quien valoró la calidad de las imágenes obtenidas como óptima (identificación completa de los bordes endocárdicos del ventrículo izquierdo), subóptima (identificación de >50% de los bordes endocárdicos del ventrículo izquierdo) o mala (identificación de <50% de los bordes endocárdicos del ventrículo izquierdo o imposibilidad de visualización). Se utilizaron en el análisis solo las ecocardiografías óptimas y subóptimas. Se determinó el porcentaje de casos en los que la ecocardiografía confirmó la sospecha diagnóstica inicial. En el caso de no confirmar el diagnóstico inicial, se determinó el porcentaje de casos en los que la ecocardiografía ofrecía un diagnóstico alternativo y el porcentaje de cambio en el tratamiento. Finalmente se analizó la mejoría clínica de los diferentes cambios terapéuticos.
En caso de duda en los hallazgos ecocardiográficos, se realizó una segunda valoración ecocardiográfica por un cardiólogo experto en ecocardiografía avanzada.
Análisis estadísticoSe realizó un estudio descriptivo en el cual analizamos el porcentaje de mejoría clínica debido a la optimización del tratamiento. Las variables continuas se expresaron en medianas y desviaciones estándar, o en porcentajes.
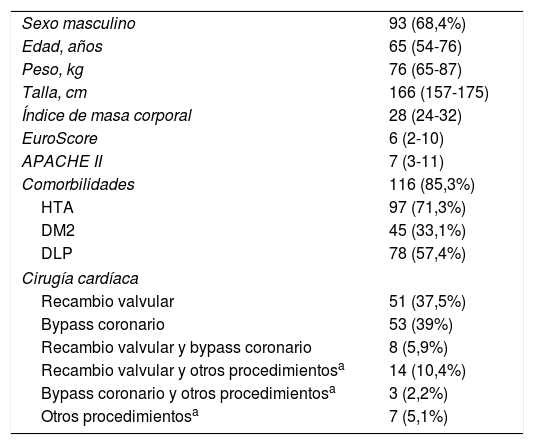
ResultadosCaracterísticas de los pacientesSe incluyeron en el estudio un total de 136 pacientes postoperados de cirugía cardíaca entre noviembre de 2014 y abril de 2016, de forma consecutiva, realizándose un total de 203 ecocardiografías. No se excluyó a ningún paciente durante el período de estudio. Los datos demográficos y clínicos se describen en la tabla 1.
Datos demográficos, clínicos e índices predictores de gravedad
| Sexo masculino | 93 (68,4%) |
| Edad, años | 65 (54-76) |
| Peso, kg | 76 (65-87) |
| Talla, cm | 166 (157-175) |
| Índice de masa corporal | 28 (24-32) |
| EuroScore | 6 (2-10) |
| APACHE II | 7 (3-11) |
| Comorbilidades | 116 (85,3%) |
| HTA | 97 (71,3%) |
| DM2 | 45 (33,1%) |
| DLP | 78 (57,4%) |
| Cirugía cardíaca | |
| Recambio valvular | 51 (37,5%) |
| Bypass coronario | 53 (39%) |
| Recambio valvular y bypass coronario | 8 (5,9%) |
| Recambio valvular y otros procedimientosa | 14 (10,4%) |
| Bypass coronario y otros procedimientosa | 3 (2,2%) |
| Otros procedimientosa | 7 (5,1%) |
DLP: dislipemia; DM2: diabetes mellitus tipo 2; HTA: hipertensión arterial.
Las cifras expresan promedio (desviación estándar) o frecuencia (porcentaje).
Respecto al tipo de cirugía realizada, la mayoría fueron recambios valvulares aislados (51 pacientes; 37,5%) o asociados a otros procedimientos (22 pacientes; 16,3%). Se realizaron 64 cirugías de revascularización coronaria (47,1%) aisladas o asociadas a otros procedimientos. En 7 pacientes (5,1%) se realizó otro tipo de cirugía.
De las sustituciones valvulares realizadas, 49 (67,12%) fueron biológicas, 21 (28,77%) mecánicas y 3 (4,11%) fueron anuloplastias. Hubo 54 (39,7%) recambios valvulares aórticos, 17 (12,5%) recambios valvulares mitrales, 4 (2,94%) anuloplastias mitrales y 15 (11,03%) anuloplastias tricuspídeas.
Todos los pacientes disponían de una ecocardiografía transtorácica previa a la cirugía, realizada por un cardiólogo durante el mismo ingreso o de forma ambulatoria unos días antes. En esta se observó que la mayoría de los pacientes presentaban un ventrículo izquierdo no hipertrófico (72 pacientes; 52,94%), no dilatado (115 pacientes; 84,56%) con una fracción de eyección calculada por Simpson 4C normal (127 pacientes; 93,38%). Respecto al ventrículo derecho, en la mayoría de los pacientes no estaba dilatado (131 pacientes; 96,32%) y presentaba una función normal en todos los casos. La vena cava inferior en la mayoría de los casos no estaba dilatada (128 pacientes; 94,11%).
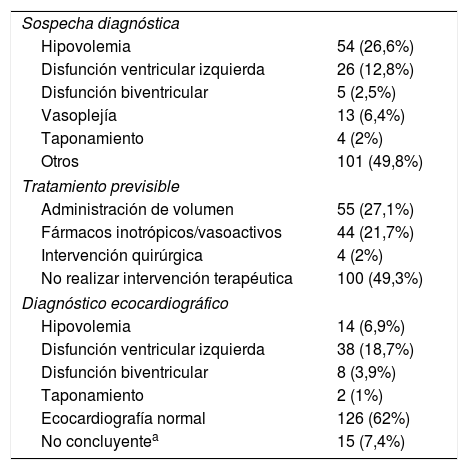
Ecocardiografía posquirúrgicaSe realizaron un total de 203 ecocardiografías transtorácicas, distribuidas de la siguiente forma: en 97 pacientes (71,3%) solo se realizó una ecocardiografía, en 19 pacientes (14%) se realizaron 2 ecocardiografías, en 14 pacientes (10,3%) se realizaron 3 ecocardiografías, en 4 pacientes (2,9%) se realizaron 4 ecocardiografías y en 2 pacientes (1,5%) se realizaron 5 ecocardiografías. En la tabla 2 se muestran los datos clínicos en el momento de realizar la ecocardiografía. El principal motivo para realizar la primera ecocardiografía fue la inestabilidad hemodinámica (74 ecocardiografías; 54,4%) y la principal sospecha diagnóstica inicial fue hipovolemia (54 casos; 26,6%). Las otras 62 ecocardiografías (45,6%) se realizaron con otra sospecha diagnóstica o como control. Las ecocardiografías realizadas en los siguientes días fueron por inestabilidad hemodinámica. Respecto al tratamiento inicial previsto por la clínica, en la mayoría de los casos (100 casos; 49,3%) no era previsible realizar ninguna intervención. En la tabla 3 se muestran las sospechas diagnósticas, el tratamiento previsto antes de realizar la ecocardiografía y el diagnóstico ecocardiográfico.
Datos clínicos en el momento de la ecocardiografía
| Ritmo cardíaco (pacientes) | |
| Sinusal | 148 (72,9%) |
| Fibrilación auricular | 34 (16,7%) |
| Bloqueo AV | 1 (0,5%) |
| Marcapasos | 20 (9,9%) |
| Frecuencia cardíaca, lpm | 80 (66-94) |
| Presión arterial media, mmHg | 79 (68-90) |
| Presión venosa central, mmHg | 10(6-14) |
| Saturación venosa central, % | 63 (53-73) |
| Lactato, mg/dl | 15 (6-24) |
| Ventilación mecánica | 51 (25,1%) |
| Fármacos vasoactivos | 125 (61,6%) |
| Noradrenalina | 52 (25,6%) |
| Nitroglicerina | 44 (21,7%) |
| Dopamina | 6 (3%) |
| Dobutamina | 45 (22,2%) |
| Milrinona | 1 (0,5%) |
| Catéter de arteria pulmonar | 42 (20,7%) |
Las cifras expresan promedio (desviación estándar) o frecuencia (porcentaje).
Sospecha diagnóstica y tratamiento previsible antes de la ecocardiografía y diagnóstico ecocardiográfico
| Sospecha diagnóstica | |
| Hipovolemia | 54 (26,6%) |
| Disfunción ventricular izquierda | 26 (12,8%) |
| Disfunción biventricular | 5 (2,5%) |
| Vasoplejía | 13 (6,4%) |
| Taponamiento | 4 (2%) |
| Otros | 101 (49,8%) |
| Tratamiento previsible | |
| Administración de volumen | 55 (27,1%) |
| Fármacos inotrópicos/vasoactivos | 44 (21,7%) |
| Intervención quirúrgica | 4 (2%) |
| No realizar intervención terapéutica | 100 (49,3%) |
| Diagnóstico ecocardiográfico | |
| Hipovolemia | 14 (6,9%) |
| Disfunción ventricular izquierda | 38 (18,7%) |
| Disfunción biventricular | 8 (3,9%) |
| Taponamiento | 2 (1%) |
| Ecocardiografía normal | 126 (62%) |
| No concluyentea | 15 (7,4%) |
Las cifras expresan promedio ±desviación estándar o frecuencia (porcentaje).
La mayoría de las ecocardiografías se realizaron en decúbito supino (197 pacientes; 97%) y el ecocardiografista estuvo una media de 14,46±2,16min por ecocardiografía. Se valoraron los grados de dificultad y la calidad de imagen para cada uno de los planos, encontrándose que en la mayoría de los casos la dificultad fue baja en todos los planos y la calidad de imagen fue óptima o subóptima en la mayoría de los casos. La peor calidad de imagen la encontramos en el plano subcostal para observar la vena cava inferior. Analizando la calidad de imagen de cada plano, encontramos que en el plano paraesternal eje largo había 85 ecocardiografías (41,9%) con calidad óptima, 81 (39,9%) con calidad subóptima y 37 (18,2%) con mala calidad. Para el plano paraesternal eje corto había 80 ecocardiografías (39,4%) con calidad óptima, 82 (40,4%) con calidad subóptima y 41 (20,2%) con mala calidad. Para el plano apical cuatro cámaras había 135 ecocardiografías (66,5%) con calidad óptima, 42 (20,7%) con calidad subóptima y 26 (12,8%) con mala calidad. Para el plano subcostal había 122 ecocardiografías (60,1%) con calidad óptima, 29 (14,3%) con calidad subóptima y 52 (25,6%) con mala calidad. Para la visualización de la vena cava inferior había 116 ecocardiografías (57,1%) con calidad óptima, 19 (9,4%) con calidad subóptima y 68 (33,5%) con mala calidad. Todas las ecocardiografías realizadas tenían algún plano con calidad óptima o subóptima, lo que permitió realizar una valoración ecocardiográfica en todos los casos.
Analizando los distintos parámetros ecocardiográficos, encontramos que el ventrículo izquierdo presentaba un tamaño normal (175 casos; 86,2%) con una función ventricular normal (151 casos; 74,4%) pero con una contractilidad heterogénea en la mayoría de los casos (111 casos; 54,7%). Tan solo 12 pacientes (5,9%) presentaban kissing walls. El ventrículo derecho presentaba un tamaño normal y una función normal en la mayoría de los casos (184 casos; 90,6%). En 60 casos (29,6%) se observó la presencia de líquido pericárdico, pero tan solo 2 pacientes (1,5%) presentaban signos de taponamiento, motivo por el cual fueron reintervenidos.
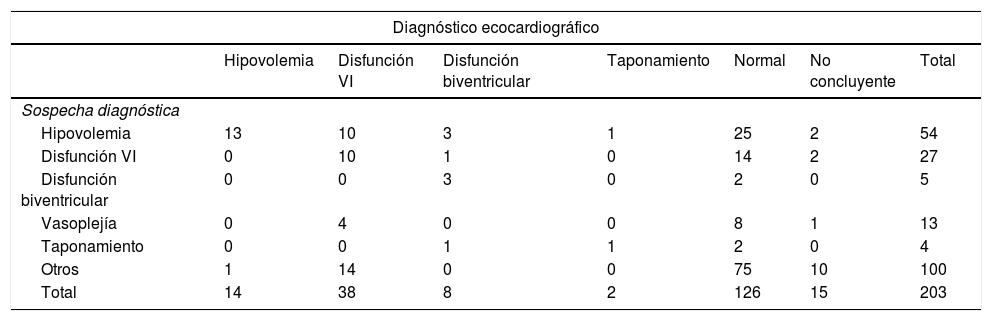
La tabla 4 compara las sospechas diagnósticas por la clínica con los resultados ecocardiográficos, pudiéndose observar las discrepancias diagnósticas. Globalmente, se obtuvo que el diagnóstico ecocardiográfico no difería de la sospecha diagnóstica en 102 casos (50,2%). En la mitad de los casos (101 casos, 49,8%) la ecocardiografía difería del diagnóstico clínico. De estos 101 casos, en 45 de ellos (44,6%) la ecocardiografía era normal, por lo que no podía ofrecer un diagnóstico alternativo. En 56 casos (55,4%) la ecocardiografía ofrecía un diagnóstico alternativo al de sospecha clínica, y de estos pacientes, se realizaron cambios en el tratamiento en 30 de ellos (53,6%). Los cambios realizados mayoritariamente fueron el inicio de fármacos inotrópicos (14 casos, 25%). Se analizó si los cambios se realizaron en la primera ecocardiografía o bien en las sucesivas. Se encontró que en un porcentaje elevado de casos en los que se producía un cambio de diagnóstico (34 casos, 60,71%), este se realizaba en la primera ecocardiografía y comportaba un cambio en la actitud terapéutica en 22 casos (64,71%). En los otros 22 casos con discrepancia diagnóstica respeto a la clínica, los cambios se produjeron en las ecocardiografías posteriores. Todos los cambios realizados se pueden observar en la tabla 5.
Comparación de diagnósticos clínicos con diagnósticos ecocardiográficos
| Diagnóstico ecocardiográfico | |||||||
|---|---|---|---|---|---|---|---|
| Hipovolemia | Disfunción VI | Disfunción biventricular | Taponamiento | Normal | No concluyente | Total | |
| Sospecha diagnóstica | |||||||
| Hipovolemia | 13 | 10 | 3 | 1 | 25 | 2 | 54 |
| Disfunción VI | 0 | 10 | 1 | 0 | 14 | 2 | 27 |
| Disfunción biventricular | 0 | 0 | 3 | 0 | 2 | 0 | 5 |
| Vasoplejía | 0 | 4 | 0 | 0 | 8 | 1 | 13 |
| Taponamiento | 0 | 0 | 1 | 1 | 2 | 0 | 4 |
| Otros | 1 | 14 | 0 | 0 | 75 | 10 | 100 |
| Total | 14 | 38 | 8 | 2 | 126 | 15 | 203 |
VI: ventrículo izquierdo.
Cambios en el tratamiento debidos a la ecocardiografía
| Administración de volumen | 1 (3,33%) |
| Inicio fármacos inotrópicos/vasoactivos | 14 (46,67%) |
| Intervención quirúrgica | 1 (3,33%) |
| Otrosa | 14 (46,67%) |
Las cifras expresan frecuencia (porcentaje).
En un caso con duda diagnóstica se contactó con el servicio de cardiología, que realizó una nueva ecocardiografía que confirmaba nuestra sospecha ecocardiográfica (derrame pericárdico severo con signos de taponamiento), por lo que se contactó con cirugía cardíaca, que decidió reintervención quirúrgica, con mejoría clínica.
De los 30 casos en los que se cambió el tratamiento debido al diagnóstico ecocardiográfico, en 26 de ellos (86,67%) se observó mejoría clínica significativa con mejoría de los parámetros hemodinámicos (presión arterial, saturación venosa central, aumento de diuresis, disminución de los requerimientos de fármacos inotrópicos y vasoactivos) en los siguientes 30-60min. Al analizar los cambios realizados en el tratamiento se observó que en 14 pacientes (46,7%) se iniciaron fármacos inotrópicos o vasoactivos, en otros 14 pacientes (46,7%) se realizó otro tipo de intervención, como finalizar la administración de volumen o la retirada de fármacos inotrópicos. En un paciente (3,3%) se administró volumen y otro paciente (3,3%) requirió reintervención quirúrgica por taponamiento. En 4 pacientes (13,33%) no se observó una clara mejoría debido al ajuste de tratamiento. En dos de los casos se habían iniciado fármacos inotrópicos o vasoactivos (uno de ellos con mala tolerancia a la dobutamina por taquicardización, y otro obtuvo escasa mejoría hemodinámica tras la administración de dobutamina). En otro caso, ante la presencia de bradicardia, se decidió aumentar la frecuencia cardíaca mediante estimulación por marcapasos, a pesar de lo cual no mejoraron los parámetros de hipoperfusión tisular. Por último, en el cuarto caso la sospecha clínica fue hipovolemia con ecocardiografía normal, por lo que se decidió no administrar volumen, pero no se evidenció un cambio clínico significativo.
DiscusiónUna vez demostrada la factibilidad de la ecocardiografía básica en las situaciones más extremas tras una cirugía cardíaca26, era importante estudiar el impacto de la ecocardiografía básica en el manejo del paciente postoperado de cirugía cardíaca. En nuestro estudio encontramos que la ecocardiografía no confirmaba el diagnóstico de sospecha clínica en casi la mitad de los casos. Por otro lado, la ecocardiografía aporta un diagnóstico alternativo en más del 50% de estos casos. Además, los clínicos pudieron realizar un cambio terapéutico en función del resultado de la ecocardiografía en 30 casos (14,8% del total de pacientes y 53,6% con cambio diagnóstico). Este porcentaje se encuentra en el rango bajo de los hallazgos de otros estudios, puesto que el cambio puede alcanzar hasta un 52%1,21,24,28. Esto puede deberse a que se trata de pacientes con características distintas. En el caso de los estudios previos, se incluyeron pacientes medicoquirúrgicos en los que pueden verse afectaciones cardíacas no previsibles por el cuadro clínico inicial. Sin embargo, todos nuestros pacientes son postoperados de cirugía cardíaca y, en consecuencia, las causas fundamentales del shock son más fáciles de sospechar por la clínica. En algunos casos la sospecha clínica fue de hipovolemia, pero con ecocardiografía básica solo podemos detectar la presencia de hipovolemia grave. Otros estudios realizados en pacientes de cirugía cardíaca aportan datos similares al impacto del uso de la ecocardiografía transesofágica29-31, aunque dichos estudios fueron realizados durante la intervención, induciendo cambios en la actitud durante la cirugía. En nuestro caso usamos la ecocardiografía transtorácica básica, técnica totalmente no invasiva, en el postoperatorio inmediato.
Heiberg et al.25 realizaron un metaanálisis de 15 estudios en el que se evaluó el uso de la ecocardiografía transtorácica y transesofágica en el postoperado de cirugía cardíaca, y concluyeron que la ecocardiografía se utilizaba de manera creciente en el postoperado de cirugía cardíaca y que su uso inducía a un cambio significativo en el diagnóstico y el tratamiento de estos pacientes, aunque dichos estudios no se diseñaron para valorar la evolución de los pacientes. De los estudios incluidos en este metaanálisis, 7 analizaban el uso de la ecocardiografía transtorácica2,32-37, y encontraron cambios en el diagnóstico y manejo que oscilaban entre el 10 y el 52%, por lo que nuestro estudio se encuentra dentro de este rango. De manera llamativa, el tratamiento instaurado tras la ecocardiografía consiguió una mejoría clínica en el 86,67% de nuestros pacientes, lo que confirma la utilidad clínica de la ecocardiografía en los pacientes postoperados de cirugía cardíaca.
En nuestro caso llama la atención que el 74% de las ecocardiografías mostraban una fracción de eyección del ventrículo izquierdo (FEVI) normal y el 90% mostraban una fracción de eyección del ventrículo derecho (FEVD) dentro de la normalidad. Esto podría deberse a que en la mayoría de nuestros pacientes la FEVI y la FEVD prequirúrgicas eran normales en 125 pacientes (92%) y en todos los casos, respectivamente, lo que podría justificar que en el postoperatorio estas estuvieran preservadas. Aun así, encontramos que el inicio de fármacos vasoactivos debido al diagnóstico ecocardiográfico fue el cambio de tratamiento más frecuente, comportando mejoría clínica del paciente.
Así pues, nuestro estudio demuestra que existe un cambio de hasta el 50% en el diagnóstico de los pacientes sometidos a cirugía cardíaca debido a la ecocardiografía. De estos, en más de la mitad de los casos se decide cambiar el tratamiento debido a la ecocardiografía, y esto comporta una mejoría clínica en la gran mayoría de pacientes. Aun así, en caso de duda se debe realizar una ecocardiografía avanzada por parte de un intensivista formado para ello, o por un cardiólogo, cuando así se estime necesario.
Nuestro estudio posee algunas limitaciones. Se trata de un estudio realizado en un solo centro, con un mismo equipo quirúrgico, por lo que no podemos extrapolar nuestros resultados a otros centros. Todas las cirugías cardíacas fueron programadas en pacientes clínicamente estables, por lo que las posibles complicaciones en el postoperatorio eran más bajas. Algunos pacientes ya presentaban disfunción ventricular en la ecocardiografía prequirúrgica, por lo que, en la posquirúrgica, esta disfunción se seguía observando por ecocardiografía, sin que ello comportase una repercusión clínica. Así mismo, la ecocardiografía básica solo es capaz de detectar la hipovolemia grave, con lo cual algunos pacientes podrían presentar hipovolemia sin que esta pueda detectarse con la realización de una ecocardiografía básica. Estas circunstancias pueden haber influido en el hecho de haber encontrado un nivel bajo de cambio en el diagnóstico ecocardiográfico respecto al clínico.
ConclusionesLa ecocardiografía transtorácica básica es útil en el manejo diagnóstico y terapéutico de los pacientes postoperados de cirugía cardíaca. En la mayoría de los pacientes en quienes se realizó un cambio en el diagnóstico según los hallazgos obtenidos en la ecocardiografía, se observó una mejoría clínica tras el cambio de tratamiento.
FinanciaciónNo hubo financiación.
AutoríaConcepción y diseño: Dra. Olga Moreno, Dra. Ana Ochagavía, Dr. Antonio Artigas, Dr. Francisco Baigorri.
Adquisición, análisis e interpretación: Dra. Olga Moreno, Dra. Ana Ochagavía, Dra. Sandra Barbadillo, Dra. Roser Tomás, Dra. Maria Dolores Bosque, Dra. Cristina Fortià.
Redacción del manuscrito: Dra. Olga Moreno, Dra. Ana Ochagavía, Dr. Antonio Artigas, Dr. Francisco Baigorri.
Conflicto de interesesLos autores no tienen conflicto de intereses.
Los autores están agradecidos a Cristina Mora, Cristina Espinal, María Luisa Martínez, Susana Millan y Eva Torrents (Hospital Universitari General de Catalunya) por su contribución en la recolección de datos.