Presentamos el caso de un paciente que presenta una parada respiratoria secundaria a angioedema que requirió intubación orotraqueal e ingreso en la unidad de cuidados intensivos. La baja frecuencia de este tipo de casos así como la sorprendente respuesta a inhibidores de la bradicinina ha motivado la publicación del presente caso clínico, previo consentimiento y autorización del paciente implicado.
Se trata de un varón de 70 años sin reacciones alérgicas conocidas, fumador y con hepatopatía crónica de origen enólico (hipertensión portal y varices esofágicas grado III/IV) en tratamiento con propranolol, hiperplasia benigna de próstata y carcinoma epidermoide infiltrante de pared posterior de orofaringe irresecable por lo que recibe quimioterapia y radioterapia. Tras finalizar los ciclos de quimioterapia se objetiva persistencia de tejido tumoral a nivel ganglionar y de cavum (T3N3), siendo positiva la biopsia para tejido tumoral en cavum.
Se decide realización de cirugía de rescate, que consiste en vaciamiento ganglionar cervical derecho con ligadura de la vena yugular derecha. Dos semanas después se realiza vaciamiento ganglionar cervical izquierdo sin ligadura de la vena yugular izquierda quedando únicamente pendiente de realizar radioterapia centrada en la región del cavum.
Veinticuatro horas tras el postoperatorio de vaciamiento cervical izquierdo el paciente presenta parada respiratoria en el contexto de broncoaspiración. Se realizan 4 minutos de masaje cardiaco y aspiración de secreciones con recuperación completa. Se reevalúa al paciente a las 4 horas permaneciendo estable hemodinámica y respiratoriamente.
Pasadas 12 oras de dicho episodio se produce nueva parada respiratoria. A la llegada del Servicio de Medicina Intensiva el paciente se encuentra respirando de forma espontánea aunque con aumento del trabajo respiratorio, cianosis facial y 55% de saturación de oxígeno en sangre por lo que se decide aislamiento de vía respiratoria con tubo endotraqueal, objetivándose durante la maniobra un importante edema a nivel orofaríngeo y laríngeo que dejaba un margen suficiente para el paso del tubo endotraqueal, no requiriendo de otras medidas complementarias para la intubación.
El paciente ingresa en la Unidad de Cuidados Intensivos, en ventilación mecánica y con necesidad de aminas vasoactivas. Se inicia antibioterapia con piperacilina y tazobactam. La TAC craneal no presenta hallazgos significativos y la TAC torácica muestra cambios edematosos generalizados en partes blandas con colecciones subcutáneas en espacio cervical anterior bajo. La vena yugular izquierda se encontraba permeable aunque de aspecto filiforme en algunas segmentos. No se observaban alteraciones parenquimatosas a nivel pulmonar de nueva aparición y el paciente no había recibido fármacos inhibidores de la enzima convertidora de angiotensina en ningún momento.
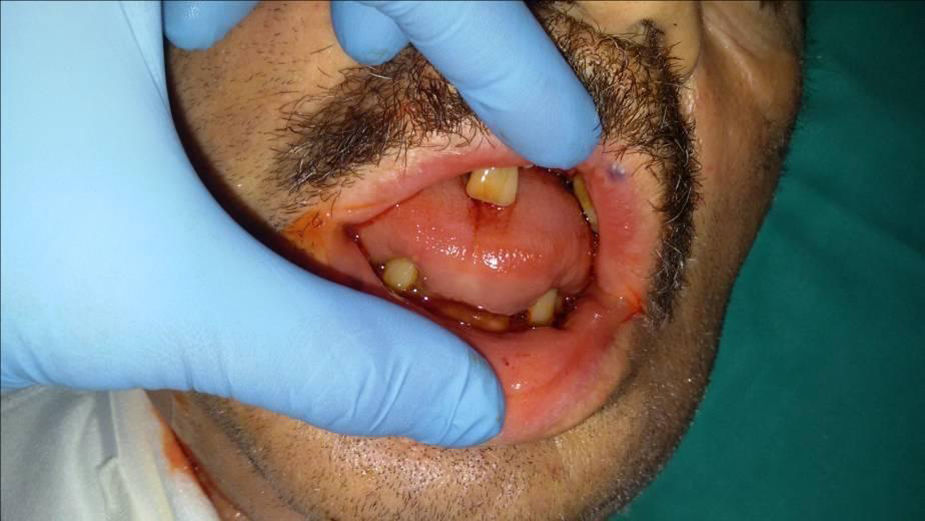
De forma progresiva y en las próximas horas a la intubación el paciente comienza con edema en la región facial, abarcando labios, lengua y región cervical anterior (fig. 1). Ante la sospecha de angioedema secundario a reacción mastocitaria se inició el tratamiento con corticoides (a dosis de 1mg/kg peso) y antihistamínicos (dexclorfeniramina 20mg/24h).
La analítica muestra hemograma y bioquímica rigurosamente normales salvo creatinina 1,32mg/dl y urea 50mg/dl, siendo los niveles de triptasa normales: 3,03mcg/l (<12mcg/l), TSH 2,3mIU/l y T4L 0,76μg/dl. Se solicitaron asimismo niveles de complemento que no llegaron hasta 24 h más tarde, siendo normales los niveles de C1q: 19,95mg/dl (12–25mg/dl), C3: 101mg/dl (75-135mg/dl), C4: 31,30mg/dl (14-60mg/dl) y elevados los niveles de C1 inhibidor: 36,70mg/dl (16-33mg/dl). No se pudo medir la actividad de C1 inhibidor ni los anticuerpos anti-C1 inhibidor dada la falta de medios técnicos disponibles.
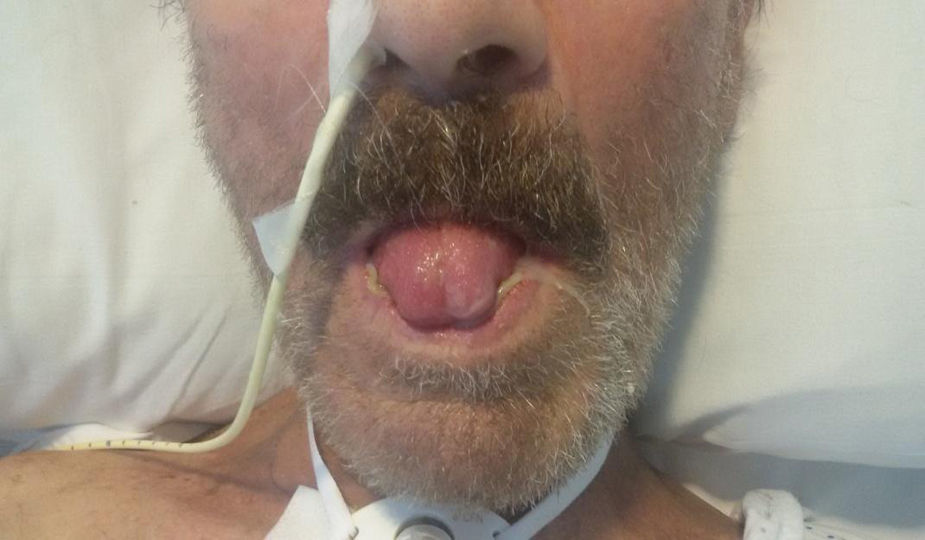
Ante la falta de respuesta tras la instauración del tratamiento corticoideo y antihistamínico, se sospecha la posibilidad de angioedema mediado por bradicinina y se inicia tratamiento con icatibant (antagonista del receptor de bradicinina B2), pautándose 30mg por vía subcutánea en dos dosis separadas entre sí 8 horas. El resultado de dicho tratamiento fue la mejoría notable del edema facial en las siguientes 24 horas (fig. 2). En el momento de instauración de dicho tratamiento no se disponía de los niveles del complemento solicitados, luego dicho tratamiento se instauró fuera de ficha técnica previo consentimiento de los familiares dado que el paciente se encontraba en ventilación mecánica.
Aunque a día de hoy se desconoce a ciencia cierta la etiopatogenia del angioedema, se han descrito dos mecanismos implicados en su producción: por un lado se distingue el angioedema mediado por mastocitos y por otro lado el mediado por bradicinina1.
Clínicamente se caracterizan por la inflamación subcutánea o submucosa secundaria a extravasación de líquido hacia el intersticio del tejido conectivo, afectando generalmente a la cara, labios, boca, úvula, etc. siendo el compromiso respiratorio una urgencia vital1.
El angioedema mediado por mastocitos se asocia generalmente a urticaria, flushing, prurito, broncoespasmo y/o hipotensión. Los niveles de triptasa suelen elevarse y el tratamiento de base es la epinefrina1. Es importante destacar el valor diagnóstico de la triptasa dado que su elevación sugiere degranulación de mastocitos y/o basófilos y por ende apoya el diagnóstico de anafilaxia aunque no se haya determinado la sensibilidad y especificidad de la misma2.
El angioedema mediado por bradicinina no suele presentar dicha clínica asociada, desarrollándose en 24-36 horas y resolviéndose en 2-4 días. Implican la participación de la vía del complemento, la vía de las cininasas y la vía de la coagulación, resultando por ende de su activación la inflamación, el angioedema y la situación de hipercoagulabilidad respectivamente3–6.
Existen varios tipos de angiodema mediados por bradicinina que se pueden distinguir entre ellos por los niveles de C1 inhibidor, la actividad de C1 inhibidor, los niveles de C1q, C3 y C4, test genéticos, serología u otras pruebas complementarias4,5.
En el angioedema hereditario (HAE) está implicado directamente el C1 inhibidor ya sea por déficit del mismo (HAE tipo I), disfuncionalidad del mismo (HAE tipo II) o HAE con función de C1 inhibidor normal (previamente denominado HAE tipo III, en la actualidad HAE-nC1INH)7. Los dos primeros cursan con un patrón de herencia autosómico dominante. Mientras que HAE I y HAE II cursan con niveles bajos de C1 inhibidor, HAE III cursa con niveles normales del mismo y suele estar asociado a mutaciones en el factor XII de la coagulación, produciendo clínica en la edad adulta6–8.
Por otro lado, se ha descrito angioedema mediado por inhibidores de la enzima convertidora de angiotensina3 y angioedema mediado por déficit adquirido de C1 inhibidor. Este último suele ser estimulado por trauma o estrés psicológico y típicamente se autolimita en los 5 primeros días, aunque es obligatorio el despistaje de síndrome linfoproliferativo, neoplasia o enfermedad autoinmune subyacente dada su elevada asociación1.
Para el tratamiento de estos cuadros los tratamientos más efectivos probados son el C1 inhibidor recombinante, el icatibant y el ecallantide (inhibidor de la calicreína no comercializado en España). En cuanto a los dos primeros, están autorizados por la Agencia Española de Medicamentos y Productos Sanitarios para el tratamiento sintomático de crisis agudas en pacientes con HAE con déficit de C1 inhibidor (HAE I y II)1. En el caso del icatibant, se ha descrito efectividad en su uso fuera de indicación para el tratamiento de ataques agudos de angioedema refractarios a C1 inhibidor recombinante, HAE III y del angioedema mediado por inhibidores de la enzima convertidora de angiotensina9–11.
El patrón analítico del complemento podría ser compatible con un HAE III, en relación con la presencia de anticuerpos anti-C1 inhibidor, un angioedema hereditario, en relación con la presencia de anticuerpos como síndrome paraneoplásico del carcinoma epidermoide del paciente o en caso de no encontrar evidencia de lo previo se calificaría como un angioedema idiopático7.
En el diagnóstico diferencial se podría considerar el mixedema (que se descarta dada la ausencia de otras alteraciones analíticas y la velocidad de instauración del cuadro). La mejoría del cuadro al introducir inhibidores de los receptores de bradicinina y las alteraciones del complemento objetivadas suponen un criterio diagnóstico de angioedema mediado por bradicinina de tipo HAE-nC1INH7 como manifestación de un síndrome paraneoplásico o secundario a manipulación quirúrgica traumática (realizada 24 horas antes) de la vía aérea superior, ambas causas descritas como posibles etiologías del angioedema mediado por bradicinina1.
FinanciaciónLos autores declaran no tener financiación externa para este estudio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Agradecemos la ayuda inestimable del Servicio de Urgencias de Adultos y del Servicio de Medicina Intensiva del Hospital Universitario La Paz, Madrid.