Comparar la discriminación y calibración de la escala modificada de Bruselas con el sistema Simplified Acute Physiology Score version 3 (SAPS-3) como predictor de mortalidad.
DiseñoCohorte prospectiva.
ÁmbitoUnidad de Cuidados Intensivos Respiratorios (UCIR) del Hospital General de México.
PacientesDe 285 ingresos en la UCIR en 2012, se incluyeron 251 pacientes, con una edad media de 48,4±17,1 años; de ellos, 132 fueron hombres (52,8%).
Intervenciones Ninguna.
Variables de interésDemográficas, SAPS-3 y escala modificada de Bruselas del primer día de estancia en UCIR.
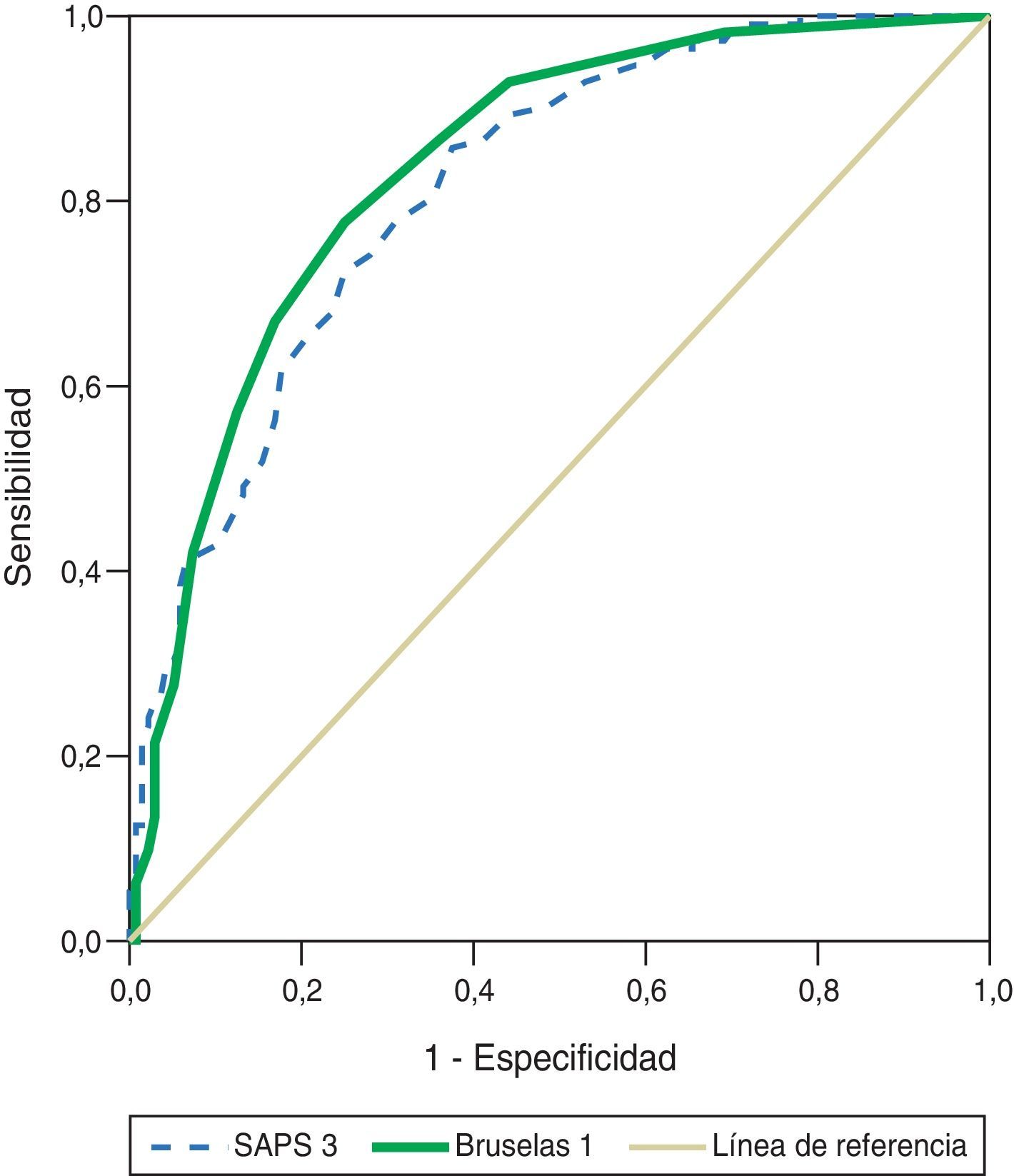
ResultadosEl valor de la escala de Bruselas modificada del día 1 fue 4,7±3,8, y de SAPS-3, 54,7±17,8. El área ROC para la escala de Bruselas modificada del día 1 fue 0,837±0,025 (IC 95% 0,787 a 0,887), y para SAPS-3, de 0,813±0,027 (IC 95% 0,761 a 0,865), con prueba de bondad de ajuste de Hosmer-Lemeshow de 5.885 (p=0,660) y 4.026 (p=0,855), respectivamente.
ConclusionesLa escala modificada de Bruselas en el día 1 tiene una discriminación y calibración excelentes para predecir la mortalidad de los pacientes en la UCIR, comparables a las del modelo SAPS-3.
To compare discrimination and calibration of the modified Brussels score with the Simplified Acute Physiology Score version 3 (SAPS-3) in predicting mortality.
DesignA prospective cohort study was carried out.
SettingThe Respiratory Intensive Care Unit (RICU) of Mexico General Hospital.
PatientsA total of 251 patients out of 285 admissions to the RICU in 2012 were included. The mean age was 48.4±17.1 years, and 132 of the patients were men (52.8%).
InterventionsNone.
Variables of interestDemographic data, SAPS-3 score upon admission and the modified Brussels score on the day 1 of stay in the RICU.
ResultsOn day 1, the modified Brussels and SAPS-3 scores were 4.7±3.8 and 54.7±17.8, respectively. Areas under the ROC curve for the modified Brussels score on day 1 and the SAPS-3 were 0.837±0.025 (95% CI 0.787-0.887) and 0.813±0.027 (95% CI 0.761-0.865), respectively. Hosmer-Lemeshow goodness-of-fit values were 5,885 (P=.660) and 4,026 (P=.855), respectively.
ConclusionsThe modified Brussels score on day 1 offers excellent discrimination and calibration in predicting mortality in the RICU, comparable to that of the SAPS-3.
La disfunción orgánica múltiple es quizá el evento final más frecuente en los pacientes que fallecen en la Unidad de Terapia Intensiva (UTI)1. Si bien es considerada consecuencia de un daño que condicionó una enfermedad grave, su aparición y progresión en la UTI son indicativas de evolución de la enfermedad y de mal pronóstico2. Se han desarrollado muchos sistemas de puntuación que evalúan el grado de disfunción orgánica. El primero fue la escala de disfunción orgánica Multiple Organ Dysfunction Score, que, por su limitación en la variable de cálculo de falla cardiovascular, fue paulatinamente abandonada. La escala de Bruselas3, que surgió posteriormente y trató de resolver este problema, también resultó subóptima4, y fue sustituida por la escala Sequential Organ Failure Assessment (SOFA)5, que inicialmente se usó en pacientes con sepsis y posteriormente se generalizó a todo paciente crítico. La escala SOFA en la actualidad es la más usada, junto con el modelo de regresión logística Logistic Organ Dysfunction Score6.
Un estudio multicéntrico mexicano que comparó las 4 escalas de evaluación de la disfunción multiorgánica reportó que todas ellas tienen excelente discriminación, pero solo la escala modificada de Bruselas demostró buena calibración (tabla 1)7. Adicionalmente, el puntaje del rubro cardiovascular es más sencillo que el de la escala SOFA, que requiere calcular las dosis de medicamentos cardiovasculares5. Por estas razones, ha sido empleada en otros estudios nacionales8,9.
Escala modificada de Bruselas
| Puntaje | 0 | 1 | 2 | 3 | 4 |
|---|---|---|---|---|---|
| Cardiovascular (presión arterial sistólica, mmHg) | >90 | <90, sin aminas vasopresoras | <90, con aminas vasopresoras a cualquier dosis | <90 y pH 7,21-7,30 | <90 y pH<7,20 |
| Pulmonar (PaO2/FiO2) | >400 | 301-400 | 201-300 | 101-200 | <100 |
| Sistema nervioso central (Escala de Coma de Glasgow) | 15 | 13-14 | 10-12 | 6-9 | <5 |
| Coagulación (plaquetas×103/μL) | >120 | 81-120 | 51-80 | 21-50 | <20 |
| Renal (creatinina, mg/dL) | <1,5 | 1,5-1,9 | 2,0-3,4 | 3,5-4,9 | >5 |
| Hepático (bilirrubina total, mg/dL) | <1,2 | 1,2-1,9 | 2,0-5,9 | 6,0-11,9 | >12 |
En nuestra UTI, la escala de Bruselas fue introducida en el año 2009 con una modificación en la variable cardiovascular que permitió facilitar su cálculo7.
El objetivo de este estudio fue evaluar la capacidad predictiva de mortalidad hospitalaria de la escala modificada de Bruselas calificada en el primer día de estancia en la UTI, comparándola con la del modelo Simplified Acute Physiology Score (SAPS-3)10,11.
Material y métodosDiseñoEstudio de cohorte prospectiva.
Pacientes y lugarPacientes que ingresaron a la Unidad de Cuidados Intensivos Respiratorios (UCIR) de 7 camas perteneciente al Servicio de Neumología y Cirugía de Tórax del Hospital General de México, O. D., hospital público escuela. El periodo de estudio fue de 12 meses (desde el 1 de enero al 31 de diciembre de 2012). Se excluyeron los pacientes con datos incompletos en el expediente clínico, los que permanecieron hospitalizados en el momento de realizar el análisis, y aquellos fallecidos en las primeras 24h.
VariablesDemográficas, calificación de SAPS-310,11 con datos de la primera hora de ingreso en la UCIR y cálculo de la mortalidad predicha al egreso hospitalario con el modelo para la región de Centroamérica y Sudamérica, y calificación de la escala modificada de Bruselas calculada con los valores que dieron el mayor puntaje a cada una de sus variables de los primeros 3 días de estancia en la UCIR. Los datos fueron tomados directamente del expediente clínico de los pacientes, de forma prospectiva.
Análisis estadísticoSe usó estadística descriptiva e inferencial. La discriminación y calibración de la escala modificada de Bruselas y de SAPS-3 se realizaron a través del cálculo del área bajo la curva de receptor operativo (ROC) y la prueba de bondad de ajuste, χ2 de Hosmer-Lemeshow, respectivamente, considerando un valor significativo para esta última una p>0,05. Para el análisis entre sobrevivientes y no sobrevivientes en los 3 días se usó la prueba t de Student para muestras independientes, considerando significativo un valor de p<0,05. Se empleó el paquete estadístico SPSS® v. 13 (SPSS, Chicago, IL, EE. UU.).
ÉticaLos comités de investigación y ética del hospital estuvieron enterados del protocolo y no consideraron necesaria la autorización escrita expresa por ser un estudio en el que no se realizó intervención médica ni se obtuvieron muestras biológicas extraordinarias para análisis, fuera de las usuales en la práctica clínica habitual. La confidencialidad de los pacientes que formaron parte del estudio fue garantizada mediante la adjudicación a cada paciente de un código constituido por 3 dígitos que correspondieron al número progresivo de ingreso en la unidad. La hoja de recolección de la información permaneció custodiada por los responsables del estudio.
ResultadosDurante el periodo de estudio ingresaron 285 pacientes en la UCIR, de los cuales fueron incluidos 251, con una edad promedio de 48,4±17,1 años; 132 eran hombres (52,8%). Fueron excluidos 25 pacientes que fallecieron dentro de las primeras 24h de ingreso en la UCIR, 8 pacientes cuya información en el expediente clínico estaba incompleta y un paciente que permanecía hospitalizado en el momento de realizar el análisis.
Las comorbilidades más frecuentes fueron hipertensión arterial en 61 casos (24,3%), diabetes mellitus en 60 (23,9%), alcoholismo en 30 (12,0%) y enfermedad respiratoria crónica en 29 (11,6%). La procedencia de los pacientes incluidos fue: piso de hospitalización 115 (45,8%), quirófano 88 (35,1%) y sala de urgencias 48 (19,1%).
A pesar de tratarse de una UTI monovalente, respiratoria, casi la tercera parte de los ingresos de esta cohorte −83 pacientes (32,9%)− no tenían afección respiratoria e ingresaron por carencia de camas en la UTI general: 43 (51,8%) por enfermedad digestiva, 15 (18,1%) neurológica, 11 (13,3%) cardiovascular y 14 (16,9%) por otras causas.
Al ingreso, 187 pacientes (74,5%) tenían sepsis. De ellos, 131 de origen respiratorio (52,2%) y 30 (12,0%) de adquisición hospitalaria. Del total de pacientes, 210 (83,7%) requirieron antibióticos con una media de 3,1±2,2 (1-11), 147 (58,6%) requirieron ventilación mecánica invasiva por una media de 10,6±12,1 días (1-82 días, mediana 7), apoyo vasopresor 117 casos (46,6%), hemoderivados 77 (30,7%) y hemodiálisis 7 casos (2,8%).
La escala modificada de Bruselas del día 1 fue 4,7±3,8, y la SAPS-3 54,7±17,8, con una mortalidad predicha promedio al egreso hospitalario del 38,8%. La mortalidad observada al egreso hospitalario fue del 45,0%, con una razón de mortalidad estandarizada de 1,16 (IC 95% 0,94-1,37). Los valores promedio de la escala modificada de Bruselas en el segundo y tercer días de estancia fueron 5,4±3,9 y 5,3±3,9, respectivamente. Sesenta pacientes permanecieron menos de 3 días en la UCIR, de los cuales 10 fallecieron en este periodo y los otros 50 fueron egresados de la UCIR vivos.
La estancia media en la UCIR fue de 9,9±11,3 días (1-93 días, mediana 6), y en el hospital, de 24,1±19,8 días (2-144 días, mediana 18).
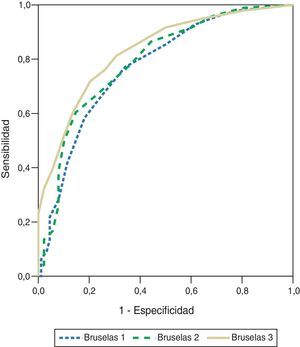
Las áreas bajo la curva ROC de la escala modificada de Bruselas y SAPS-3 fueron 0,837±0,025 (IC 95% 0,787-0,887) y 0,813±0,027 (IC 95% 0,761-0,865), respectivamente (fig. 1). Los valores de χ2H-L para la escala modificada de Bruselas y SAPS-3 fueron 5.885 (p=0,660) y 4.026 (p=0,855), respectivamente.
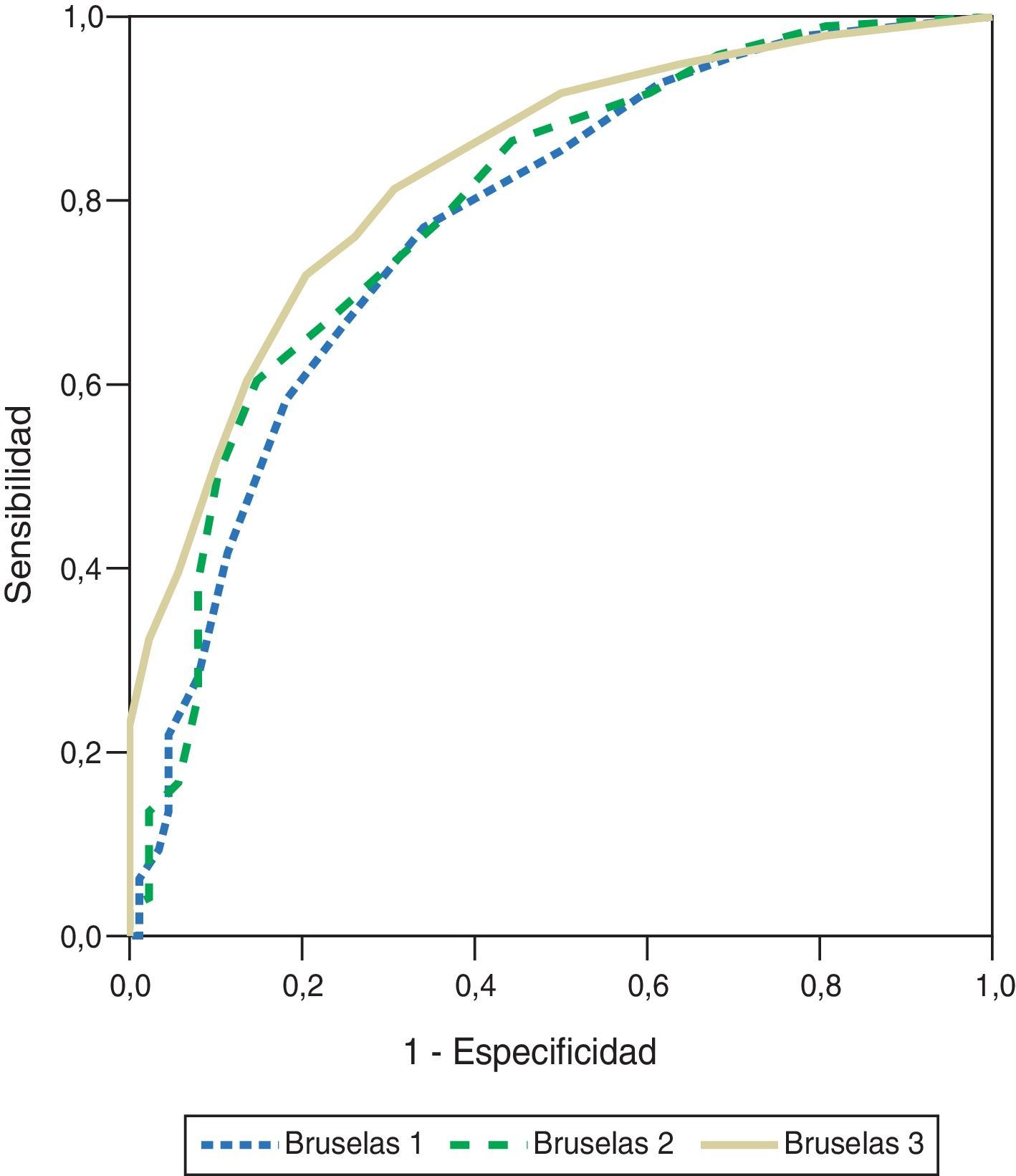
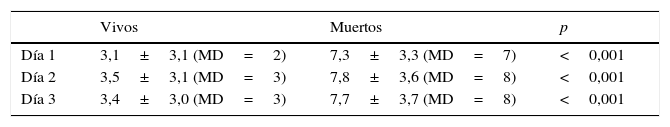
Los valores promedio de la escala modificada de Bruselas para sobrevivientes y no sobrevivientes en los días 1-3 de estancia en UCIR se muestran en la tabla 2. El valor del área ROC que evalúa la discriminación de la escala en los días 2 y 3 fue de 0,818±0,029 (IC 95% 0,761-0,876), y 0,835±0,029 (IC 95% 0,777-0,893), respectivamente (fig. 2) y los valores de χ2H-L fueron 12.174 (p=0,144) y 3.958 (p=0,861), respectivamente.
Actualmente los 3 modelos predictivos más usados en la UTI en el pronóstico de mortalidad al egreso hospitalario son APACHE IV, MPM0-III y SAPS-312. No obstante, solo del 10 al 15% de las UTI usan escalas de puntuación de gravedad y/o disfunción orgánica13. El bajo apego a la implementación de los sistemas de puntuación puede ser consecuencia, en parte, de obstáculos como el costo y la preocupación acerca de su exactitud y aplicabilidad a una población específica de pacientes.
Las escalas de disfunción orgánica fueron desarrolladas en un intento por medir el grado de disfunción orgánica de manera objetiva a lo largo del tiempo, evaluando la morbilidad en la UTI5,14,15. Las escalas que evalúan la disfunción orgánica más usadas en la actualidad (Multiple Organ Dysfunction Score, Logistic Organ Dysfunction Score y SOFA) han demostrado su poder predictivo de mortalidad, ya sea con mediciones únicas o repetitivas16. La escala de Bruselas, si bien fue sustituida por la escala SOFA rápidamente después de su creación5, es usada por algunas UTI en México con buenos resultados8,9. Nuestra UTI introdujo el modelo predictivo SAPS-3 en marzo de 201017, y considerando que la predicción de la mortalidad busca el empleo de modelos más sencillos (menor número de variables) y con la misma o mejor capacidad discriminativa y de calibración que los modelos más sofisticados actuales, nos pareció interesante comparar ambas escalas buscando el poder predictivo de mortalidad de la escala modificada de Bruselas que no fue descrito.
Comparada con SAPS-3, la escala de Bruselas modificada demostró una discriminación excelente, tanto para las primeras 24h de estancia en la UCIR como en los días 2 y 3 de estancia. Es de esperar que la escala por sí misma, sin el uso de un modelo probabilístico, permita obtener un área bajo la curva ROC que represente la probabilidad de que un paciente que no sobrevive tenga un valor en la escala mayor que el de un paciente que sobrevive. Ningún estudio hasta ahora ha reportado el uso de la escala de Bruselas dentro de un modelo de regresión logística. Ya que la escala no brinda un valor cuantitativo de estimación del riesgo de mortalidad, su calibración y exactitud no pueden ser evaluadas para la escala por sí misma18.
Adicionalmente, se evaluó la diferencia entre los valores obtenidos en la escala de Bruselas modificada en los días 2 y 3 de estancia en la UCIR con fines exploratorios, tratando de determinar si el valor se distanciaba más entre vivos y muertos. Los resultados mostraron que los valores se mantuvieron sin cambios. La disfunción orgánica es un proceso dinámico y el grado de la misma puede variar no solo con el tiempo, sino también con el tratamiento2,19. Se puede esperar que al añadir información del curso de tratamiento en la UTI mejore la capacidad de la escala para predecir la posibilidad de sobrevida; no obstante, como se ha visto con otras escalas que usaron mediciones consecutivas18, fallas orgánicas más graves con puntuaciones más altas serán encontradas justo antes de morir. La ausencia de variación de puntuación de la escala en días consecutivos en este estudio puede deberse a muchos factores, uno de los cuales es que a pesar de que 10 de los 60 pacientes que egresaron de la UCIR en las primeras 72h fallecieron, los otros 50 pacientes fueron egresados por mejoría.
Cuando se emplean los valores más anormales de las primeras 24h de estancia en la UTI, el área ROC para la escala SOFA se ha reportado entre 0,61 y 0,88 con χ2H-L de 0,17 a 0,816,18,20,21. La escala Logistic Organ Dysfunction Score6, diseñada para evaluar la probabilidad de morir en base a la disfunción orgánica en el primer día de estancia en la UTI usando el peor valor para cada variable, tiene una capacidad discriminativa que varía de 0,805 a 0,8806,16,21.
Al comparar el valor del área bajo la curva ROC reportado en el estudio mexicano que contrastó el desempeño de las 4 escalas de evaluación del síndrome de disfunción orgánica múltiple7 con el presente reporte (0,893 vs. 0,837), vemos que la primera tiene mejor poder predictivo. Esto es posible debido a que la población del primer estudio fue diferente, ya que incluyó pacientes posquirúrgicos, oncológicos y traumatológicos, mientras que en este estudio se incluyeron pacientes con padecimientos predominantemente respiratorios. La excelente capacidad discriminativa de la escala de Bruselas modificada, similar a la de SAPS-3, puede resultar útil para nuestra población de pacientes; no obstante, a pesar de que su cálculo fue facilitado, no solucionó el problema de la variable cardiovascular que la hizo subóptima4,22, ya que la acidemia puede deberse a otros factores, incluso la falla renal; además, su cálculo requiere de la toma de variables después de 24h, lo que no le brinda ventajas comparada con SAPS-3, que se calcula con variables de la primera hora.
Una desventaja del estudio es que se realizó en un solo centro. Actualmente, se inició la validación externa de la escala modificada de Bruselas en un estudio multicéntrico.
Otra limitación del estudio es su realización en una terapia monovalente, sin embargo, como se describió previamente, una tercera parte de la población no ingresó por enfermedad respiratoria, lo que posiblemente permita la generalización de los resultados.
ConclusionesEn la muestra analizada en nuestra UCIR, el valor más alto de la escala modificada de Bruselas en las primeras 24h de ingreso tiene discriminación y calibración excelentes para predecir la mortalidad de los pacientes a su egreso hospitalario, comparables a los del modelo predictivo SAPS-3. Además, el valor de la puntuación de la escala en los días 2 y 3 de estancia en UCIR es útil discriminando sobrevivientes de no sobrevivientes; su uso en pacientes críticos como predictor de mortalidad es un área a explorar, considerando su sencillez.
FinanciaciónNinguna.
Conflicto de interesesLos autores niegan conflictos de interés relacionados con la elaboración de este trabajo.