INTRODUCCION
El complejo troponina está compuesto por tres subunidades proteicas, unidas laxamente, que desempeñan cada una de ellas un papel específico en el control de la contracción muscular. La troponina T presenta gran afinidad por la tropomiosina, la troponina C por los iones de calcio y la troponina I es el componente inhibitorio del complejo troponina1.
En el miocardio humano existe una sola forma isoforma de troponina I que contiene una secuencia de aminoácidos específica en el extremo N terminal que está ausente en la isoforma de la troponina I del músculo esquelético. Esta secuencia de aminoácidos no se ha encontrado en otros tejidos2.
La troponina I se distribuye uniformemente en aurícula y ventrículo. Se ha evidenciado que la presencia de troponina I en la circulación periférica es altamente específica de lesión miocárdica.
Varios autores han estudiado los cambios de la troponina T en el postoperatorio de la cirugía con circulación extracorpórea. Katus et al3 refieren que los valores máximos observados en el primer y cuarto día del postoperatorio se correlacionan con el tiempo de pinzamiento aórtico. Ordóñez et al4 identifican dos grupos de pacientes, uno con un valor máximo de troponina T superior a 4 ng/ml el primer día del postoperatorio y otro con un valor máximo inferior o igual a 4 indicando que dichas determinaciones son capaces de poner en evidencia el llamado "daño miocárdico mínimo". Además, señalan que en los pacientes con infarto agudo de miocardio perioperatorio (IAMP) se observa una evolución de las concentraciones de troponina T diferente a la de los pacientes sin IAMP. En los primeros, la concentración de troponina T aparece elevada (hasta 20 veces el límite de detección del ensayo), no tan sólo el primer día postintervención, sino que se mantiene así hasta el cuarto y quinto día del postoperatorio.
Las determinaciones seriadas de troponina I son un método sensible y específico para el diagnóstico de IAMP en la cirugía no cardíaca5. En pacientes sometidos a cirugía cardíaca la troponina I es un indicador sensible y específico del daño miocárdico, así como un buen predictor de mortalidad6,7.
El objetivo de nuestro estudio es analizar el valor de la determinación de la troponina I como predictor de morbilidad y, consecuentemente, de estancia prolongada en la UCI en el postoperatorio precoz tras cirugía cardíaca.
MATERIAL Y MÉTODO
Se realizó un estudio prospectivo, observacional, analítico, de cohortes, en el que se incluyeron los pacientes intervenidos de cirugía cardíaca con circulación extracorpórea en el período comprendido entre marzo de 1998 y marzo de 1999 y que fueron ingresados en nuestra unidad de cuidados críticos y urgencias, servicio polivalente con un total de 42 camas, perteneciente a un hospital de tercer nivel (Complejo Hospitalario Universitario Carlos Haya de Málaga). De los 243 pacientes intervenidos se excluyeron los fallecidos dentro de las primeras 24 h del postoperatorio (8 casos), aquellos sometidos a aneurismectomía (4) y las reparaciones de anomalías congénitas (1), así como los casos en los que no se realizó alguna determinación de troponina (13). Se analizaron 217 pacientes intervenidos de forma programada y urgente en dicho período.
La premedicación anestésica se realizó con cloruro mórfico (0,1 mg/kg), y escopolamina (0,005 mg/kg) en pacientes menores de 70 años, por vía intramuscular, administrada una hora antes de ir a quirófano junto a la profilaxis antibiótica. En pacientes con cardiopatía isquémica añadimos atenolol 25 mg oral o parche de nitroglicerina (5-10 cm) según el tratamiento previo. Antes de la inducción anestésica se colocó, previa infiltración con anestésico local, una cánula arterial radial (Seldicath-plastimed) mediante inserción percutánea y se tomaron las muestras de sangre basales. La inducción anestésica se realizó con etomidato (0,2 mg/kg) o midazolam (0,1-0,2 mg/kg), dependiendo de si la fracción de eyección era menor o mayor del 50%, respectivamente, junto a fentanilo (10 µg/kg), bromuro de pancuronio (0,1-0,15 mg/kg en dosis fraccionadas) y oxígeno al 100%, procediéndose a continuación a la intubación orotraqueal y la conexión a ventilación mecánica. Tras dicha inducción, se colocó un catéter de termodilución de Swan-Ganz 7 F (Abboth) por punción de vena yugular interna. En todos los pacientes se empleó parada cardíaca con cardioplejía cristaloide a una temperatura entre 6 y 8 °C con Plasmalyte 148, al que se añadían, por cada 500 ml, 5 mEq de bicarbonato sódico, 4 mEq de acetato sódico, 50 mg de cloruro cálcico y 13 mg de heparina sódica, que fue administrada a unos 10 ml/kg la primera dosis.
Se utilizó la derivación cardiopulmonar habitual con flujo pulsátil (bomba de extracorpórea Stökert) y un oxigenador de membrana Sarns o Monolyth. El flujo de la bomba se mantuvo entre 2 y 2,5 l.min1.m-2 y se empleó una moderada hipotermia (26-28 °C). El cebado de la bomba se hizo con 1.250 cm3 de Ringer lactado y 250 ml de manitol al 20%. Antes de la derivación cardiopulmonar cada paciente recibió heparina sódica (3 mg/kg), que luego fue antagonizada con sulfato de protamina, según el cálculo realizado con un Hemotech (Medtronic). La sangre y los fluidos intravenosos fueron administrados según los cambios en el hematócrito, la presión arterial sistémica y la presión de llenado ventricular izquierdo.
Las variables analizadas fueron:
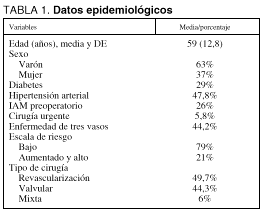
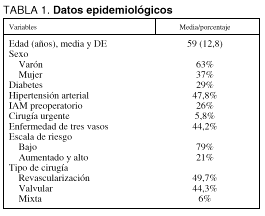
1. Relativas a factores de riesgo y datos epidemiológicos. Edad, sexo, factores de riesgo cardiovascular (diabetes e hipertensión), estudio angiográfico (existencia o no de enfermedad coronaria de tres vasos), presencia de infarto preoperatorio y fracción de eyección preoperatoria. Se clasificaron los pacientes según la escala de riesgo quirúrgico de Tuman, que divide a los pacientes en tres niveles de riesgo: bajo, aumentado y elevado8. En nuestro estudio se agrupan en dos categorías: bajo riesgo, propiamente dicho, y riesgo aumentado.
2. Relativas a la cirugía. Tiempo de circulación extracorpórea, tiempo de pinzamiento aórtico, nivel de hipotermia, vía de administración de la cardioplejía y volumen de la misma. El tipo de cirugía realizada se clasifica en cirugía de revascularización miocárdica, valvular y mixta (revascularización más valvular).
El carácter urgente de la cirugía se define por la necesidad de intervenir por la presencia de compromiso hemodinámico, angor incontrolado a terapia mixta, incluyendo balón de contrapulsación o por complicaciones de la angioplastia o la coronariografía.
3. Relativas a la evolución postoperatoria inmediata. Estancia en la UCI, necesidad de balón de contrapulsación, síndrome de bajo gasto postoperatorio, morbilidad y mortalidad intraunidad.
Se consideró estancia prolongada en la unidad aquella que superaba los 4 días. Se definió morbilidad, según los criterios de Tuman, como la presencia de una o más de las siguientes complicaciones:
* Infarto perioperatorio: nuevos y persistentes cambios electrocardiográficos postoperatorios y un incremento en las enzimas cardíacas específicas (CPK-MB).
* Bajo gasto cardíaco: índice cardíaco (IC) menor de 2 l.min-1.m-2, con necesidad de inotrópicos durante más de 24 h y/o implantación de balón de contrapulsación aórtico.
* Ventilación mecánica prolongada: superior a 48 h o necesidad de reintubación y ventilación mecánica.
* Fracaso renal: incremento de creatinina sérica en más de 2 mg/dl respecto a la preoperatoria o necesidad de diálisis.
* Complicación infecciosa: neumonía nosocomial (cambios radiológicos, fiebre, leucocitosis y cultivo de esputo positivo). Infección mediastínica o sepsis con cultivo positivo.
* Neurológica: alteraciones de la conciencia, focalidad motora, coma o daño intracraneal documentado. No se consideró la psicosis, demencia y agitación o confusión a no ser que coexistiera con focalidad neurológica.
Medida de la troponina I
Se determinó la troponina I basal (Tp0) antes del inicio de la cirugía, a las 24 h del inicio de la misma (Tp1) y a las 96 h de la inducción anestésica (Tp4). Las determinaciones cuantitativas de troponina I se realizaron en suero con enzimoinmunoanálisis fluorométrico (Stratus®-DADE).
Análisis estadístico
Las variables cuantitativas se expresan como media y desviación estándar (DE) y las variables cualitativas se expresan como número de casos en porcentajes. Las diferencias entre porcentajes fueron analizadas con la prueba de la c2, aplicando el test exacto de Fisher cuando estaba indicado. Para la comparación de medias se utilizó la t de Student o el análisis de la variancia. Realizamos un análisis univariante relacionando cada variable con nuestra variable dependiente (morbilidad) mediante la c2 o la t de Student, eligiendo las variables que resultaban significativas para la construcción de nuestro modelo. Posteriormente, se realizó un estudio de regresión logística mediante el método de paso adelante según el estadístico de Wald, incluyendo las variables anteriores. Los criterios de entrada de las variables se establecieron en 0,05 y de salida en 0,1. Una vez demostrada la asociación estadísticamente significativa entre el valor de la troponina en el primer y cuarto día con la morbilidad postoperatoria, se calculó el punto de corte de mayor discriminación diagnóstica mediante la utilización de las curvas de características de recepción operativa o de rendimiento diagnóstico (curvas ROC), para la elección del punto de corte de máxima discriminación diagnóstica, es decir, aquel donde la suma de la sensibilidad y la especificidad es más próxima a 2.
La significación estadística se definió como un valor de p < 0,05. El análisis fue realizado con el programa SPSS 8.0 para Windows.
RESULTADOS
En la tabla 1 se establecen las características clínicas y demográficas de nuestra casuística quirúrgica. En la tabla 2 aparecen los valores de las variables intra y postoperatorias. El 28,7% de los pacientes presentaron morbilidad con los criterios establecidos; de ellos, un 70% presentaban síndrome de bajo gasto. La estancia media fue 4,7 (6) días con un rango de 1-54 días.
Los valores de la troponina I determinada a las 24 h tras la cirugía oscilaron entre 0,15 y 101 ng/ml con un valor medio de 12 (13) ng/ml. Los resultados en el cuarto día variaron de 0,1 a 43 ng/ml, 3,1 (6,09). Los valores de troponina I en los días primero y cuarto de los pacientes que presentaron morbilidad frente a los que no la desarrollaron fueron diferentes de forma significativa: 20,8 (17,8) ng/ml frente a 8,7 (8,8) ng/ml y 6,9 (9,3) ng/ml frente a 1,5 (2,6) ng/ml, respectivamente.
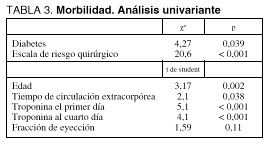
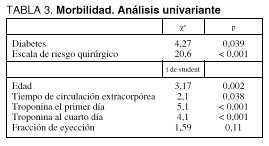
En el análisis univariante, las variables con significación estadística fueron las representadas en la tabla 3. En el estudio de regresión logística, las variables incluidas en el modelo con significación estadística fueron las indicadas en la tabla 4. En nuestro modelo, para el valor de corte 0,5, el porcentaje de aciertos es de un 85,07%. La calibración de dicho modelo mediante el test de Hosmer y Lemeshow (c2 = 17,53; p = 0,025) presenta una adecuada predicción del modelo. La discriminación del modelo mediante un estudio del área bajo la curva de las diferentes probabilidades individuales respecto a la morbilidad también es adecuada: área bajo la curva de 0,83 (0,86-0,89) y p < 0,0001.
La odds ratio (OR) de presentar morbilidad, en los sujetos con troponina > 10 ng/ml en el primer día (Tp1+), fue de 2,4, con un intervalo de confianza (IC) de 1,8-3,2 (p < 0,001). La OR de presentar estancia prolongada (> 4 días) en los sujetos Tp1+ fue de 1,8 con un IC de 1,4-2,5 (p < 0,001).
La determinación de la troponina I a las 24 h de la cirugía, como variable predictora de morbilidad en los pacientes sometidos a cirugía con circulación extracorpórea presenta una sensibilidad del 75% y una especificidad del 70% para un punto de corte de 10 ng/ml. Como predictora de estancia prolongada para el mismo punto de corte presentó una sensibilidad del 64% y una especificidad del 67%.
DISCUSION
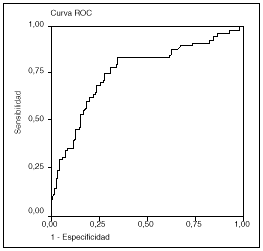
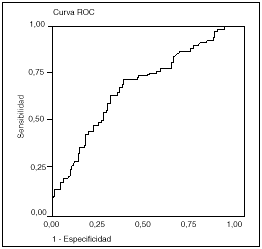
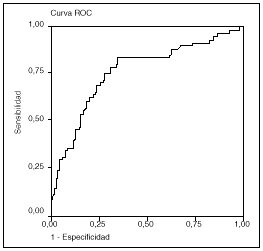
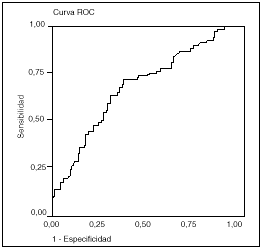
El valor de la troponina I a las 24 h del inicio de la cirugía en los pacientes sometidos a circulación extracorpórea nos permite predecir la aparición de morbilidad y la prolongación de la estancia con una sensibilidad del 75 y el 64%, y una especificidad del 70 y el 67%, respectivamente, para un punto de corte en 10 ng/ml (figs. 1 y 2).
Fig. 1. Troponina a las 24 h del inicio de la cirugía y su relación con la morbilidad. Área 0,77 (IC: 0,69-0,84; p < 0,001).
Fig. 2. Troponina a las 24 h y su relación con la estancia prolongada (> 4 días). Área 0,69 (IC: 0,61-0,76; p < 0,001).
La determinación de troponina I es un método altamente sensible y específico para detectar el daño miocárdico tanto en humanos como en animales9. Se ha demostrado la concordancia entre la aparición de defectos segmentarios en la motilidad de la pared cardíaca, detectados por ecocardiografía, y las elevaciones de la troponina I5,7,10-17. El desarrollo de IAMP tiene implicaciones pronósticas en la evolución del postoperatorio. Durante la estancia hospitalaria los pacientes que presentan IAMP tienen un riesgo aumentado de presentar complicaciones, que van desde arritmias graves hasta la muerte. Por otro lado, la elevación de troponina, por sí misma, no es un indicador de obstrucción de la arteria coronaria. Además, su valor aumenta tanto en el IAM-Q como en el no Q; también aumenta de forma significativa en los pacientes sometidos a circulación extracorpórea sin que presenten IAM. Este tipo de elevación es atribuido al daño miocárdico debido a la canulación de la aurícula derecha, una inadecuada cardioprotección, el tiempo de cirugía prolongado, el tipo de cardioplejía utilizada y su vía de administración, etc. Esta elevación suele ocurrir en las primeras 12 h, presenta una cinética diferente y su pico no suele ser muy elevado18.
Birdi et al19 han utilizado la determinación de troponina I como medio para probar que el daño miocárdico era menor en pacientes con cirugía mínimamente invasiva frente a los sometidos a bypass coronario tradicional, ya que en los primeros el valor de la troponina sérica I era significativamente menor. Chocron et al20 utilizaron la valoración de los niveles de troponina I para demostrar que la cardioplejia anterógrada intermitente medianamente templada es menos lesiva para el miocardio que la fría o la templada.
Otros autores han determinado incluso la troponina I en líquido pericárdico, encontrando picos más altos y más precoces que en el suero, tras un daño miocárdico, aunque no recomiendan su determinación rutinaria21.
Reich et al22 han relacionado las anomalías hemodinámicas intraquirúrgicas con complicaciones posquirúrgicas (accidente cerebrovascular, infarto agudo de miocardio) y con la mortalidad, usando como marcadores de daño miocárdico la troponina I, la troponina T y la CK-MB.
La importancia de la troponina I es tal que una elevación precoz (dentro de las primeras 24 h posquirúrgicas), junto a una disfunción miocárdica detectada por ecocardiograma en cirugía pediátrica, es suficiente para aplicar una terapia adecuada antes de que aparezca cualquier signo clínico de fallo hemodinámico7.
Provenchere et al6 llegan a la conclusión de que una elevación de la troponina I, después de realizar un procedimiento con injerto aortocoronario, reemplazamiento valvular o valvuloplastia mitral está fuertemente asociado con un riesgo elevado de mortalidad intrahospitalaria. Concluyen que una determinación aislada dentro de las primeras 20 h tras cirugía permite una temprana identificación de pacientes con un riesgo de muerte aumentado.
Nuestro estudio relaciona las complicaciones posquirúrgicas con los valores de troponina I medidos en el primer y el cuarto día tras la cirugía, siendo su asociación estadísticamente significativa, tanto para cirugía valvular como de revascularización miocárdica. Quisimos establecer un punto de corte con sensibilidad y especificidad óptimas que nos permitiera la máxima discriminación diagnóstica del test, para establecer un pronóstico evolutivo, lo que redundaría en un mejor control clínico del paciente y en la prevención de las posibles complicaciones. Para ello, utilizamos las curvas ROC. Como indican Gensini et al18, el pico de troponina aparece precozmente, por lo cual el área bajo la curva resultó más significativa en el primer día.
En nuestra casuística, con la limitación del tamaño de la muestra y aplicando un análisis de regresión logística, hemos encontrado tres variables predictoras de la aparición de la morbilidad postoperatoria, que son la edad del paciente, la categoría de riesgo según la escala de Tuman modificada y un valor de troponina I > 10 ng/ml a las 24 h del inicio de la cirugía cardíaca.
AGRADECIMIENTOS
Queremos agradecer su colaboración a todo el personal médico y enfermería de la unidad de cuidados críticos y urgencias, y los servicios de cirugía cardiovascular, anestesia y laboratorio.