La insuficiencia respiratoria aguda supone una de las causas más frecuentes de ingreso en los servicios de Medicina Intensiva y la oxigenoterapia sigue constituyendo una terapéutica de primera línea en el manejo de estos pacientes. En los últimos años, la oxigenoterapia de alto flujo ha sido descrita como una alternativa útil a la oxigenoterapia convencional en los pacientes con insuficiencia respiratoria aguda. La oxigenoterapia de alto flujo permite administrar un flujo de gas totalmente acondicionado hasta a 60L/min mediante cánulas nasales, obteniendo una rápida mejoría de los síntomas debido a diferentes mecanismos como, por ejemplo, una reducción de la resistencia de la vía aérea superior, cambios en el volumen circulante y la generación de cierto grado de presión positiva. Además, todo ello se consigue junto con una mejor tolerancia y comodidad por parte del paciente. Sin embargo, la experiencia en adultos es todavía limitada y no existen guías clínicas que establezcan recomendaciones para su uso. En este artículo se pretende revisar la evidencia existente sobre el uso de oxigenoterapia de alto flujo en pacientes adultos con insuficiencia respiratoria aguda, así como sus posibles aplicaciones, ventajas y limitaciones.
Acute respiratory failure represents one of the most common causes of intensive care unit admission and oxygen therapy remains the first-line therapy in the management of these patients. In recent years, high-flow oxygen via nasal cannula has been described as a useful alternative to conventional oxygen therapy in patients with acute respiratory failure. High-flow oxygen via nasal cannula rapidly alleviates symptoms of acute respiratory failure and improves oxygenation by several mechanisms, including dead space washout, reduction in oxygen dilution and inspiratory nasopharyngeal resistance, a moderate positive airway pressure effect that may generate alveolar recruitment and an overall greater tolerance and comfort with the interface and the heated and humidified inspired gases. However, the experience in adults is still limited and there are no clinical guidelines to establish recommendations for their use. This article aims to review the existing evidence on the use of high-flow oxygen via nasal cannula in adults with acute respiratory failure and its possible applications, advantages and limitations.
La insuficiencia respiratoria aguda (IRA) supone una causa frecuente de ingreso en los servicios de Medicina Intensiva1 y la oxigenoterapia sigue constituyendo, sin lugar a dudas, uno de los tratamientos de primera línea en su manejo2. En condiciones de IRA, podemos administrar oxígeno de una manera invasiva o no invasiva. Sin embargo, siempre que sea posible se debería tratar de evitar la instauración de un soporte ventilatorio invasivo.
Existen distintas formas de aplicación de oxigenoterapia no invasiva, como, por ejemplo, mediante máscara nasobucal o a través de cánulas nasales. Sin embargo, la oxigenoterapia no invasiva presenta una serie de factores limitantes que condicionan su eficacia y, en consecuencia, también limitan la corrección de la hipoxemia y de la clínica asociada a la IRA. Los principales factores limitantes son, por un lado, la tolerancia del sistema de aplicación, y por otro, la limitación del flujo de oxígeno administrado. Este, en general, se limita a 15L/min3, y normalmente se administra en condiciones no ideales de temperatura y humedad (deberían ser37°C y 100% de humedad relativa). Esta limitación del flujo administrado supone que se produzca una dilución del oxígeno administrado con el aire ambiente, condicionado por el pico de flujo inspiratorio del paciente. Por tanto, a mayor pico de flujo inspiratorio, mayor dilución, con lo que disminuye la FiO2 real suministrada al paciente2,4. Esta situación, con poca traducción clínica en pacientes con hipoxemia leve, implica que, en pacientes con IRA grave que presentan una hipoxemia importante y que realizan picos de flujo inspiratorios mayores de 30L/min, la corrección de la IRA pueda no ser suficiente mediante oxigenoterapia convencional. Una alternativa que solventaría estas limitaciones de la oxigenoterapia convencional es el uso de dispositivos de ventilación mecánica no invasiva (VMNI), si bien la principal limitación de estos dispositivos es la incomodidad y la mala tolerancia por parte del paciente de sus interfaces5.
Una reciente alternativa es la oxigenoterapia de alto flujo (OAF)6, que permite suministrar un flujo de gas de hasta 60L/min mediante unas cánulas nasales de silicona, con el gas suministrado acondicionado a nivel de temperatura y humedad ideales (37°C y 100% de humedad relativa). Hasta hace pocos años esta técnica de oxigenoterapia se había utilizado fundamentalmente en neonatos7–9. Sin embargo, su uso en pacientes adultos ha ido incrementándose exponencialmente a lo largo de los últimos años10.
La utilización de la OAF permite una mejora en la oxigenación por una serie de mecanismos distintos, como son la disminución de la dilución del oxígeno administrado con el aire ambiente11,12, la disminución del espacio muerto12–14, el aumento del volumen circulante15,16 y la generación de presión positiva en la vía aérea (CPAP)16–19. También podría producir efectos beneficiosos a nivel hemodinámico20, mejorar la capacidad para la realización de esfuerzos e incrementar el bienestar5, y gracias a la humidificación activa del gas administrado, mejorar el transporte mucociliar21,22.
El objetivo del presente artículo es realizar una puesta al día de las posibles aplicaciones clínicas de la OAF, analizando los mecanismos por los que puede ser útil en pacientes adultos con IRA, en qué pacientes puede ser más útil y cómo debemos usarla.
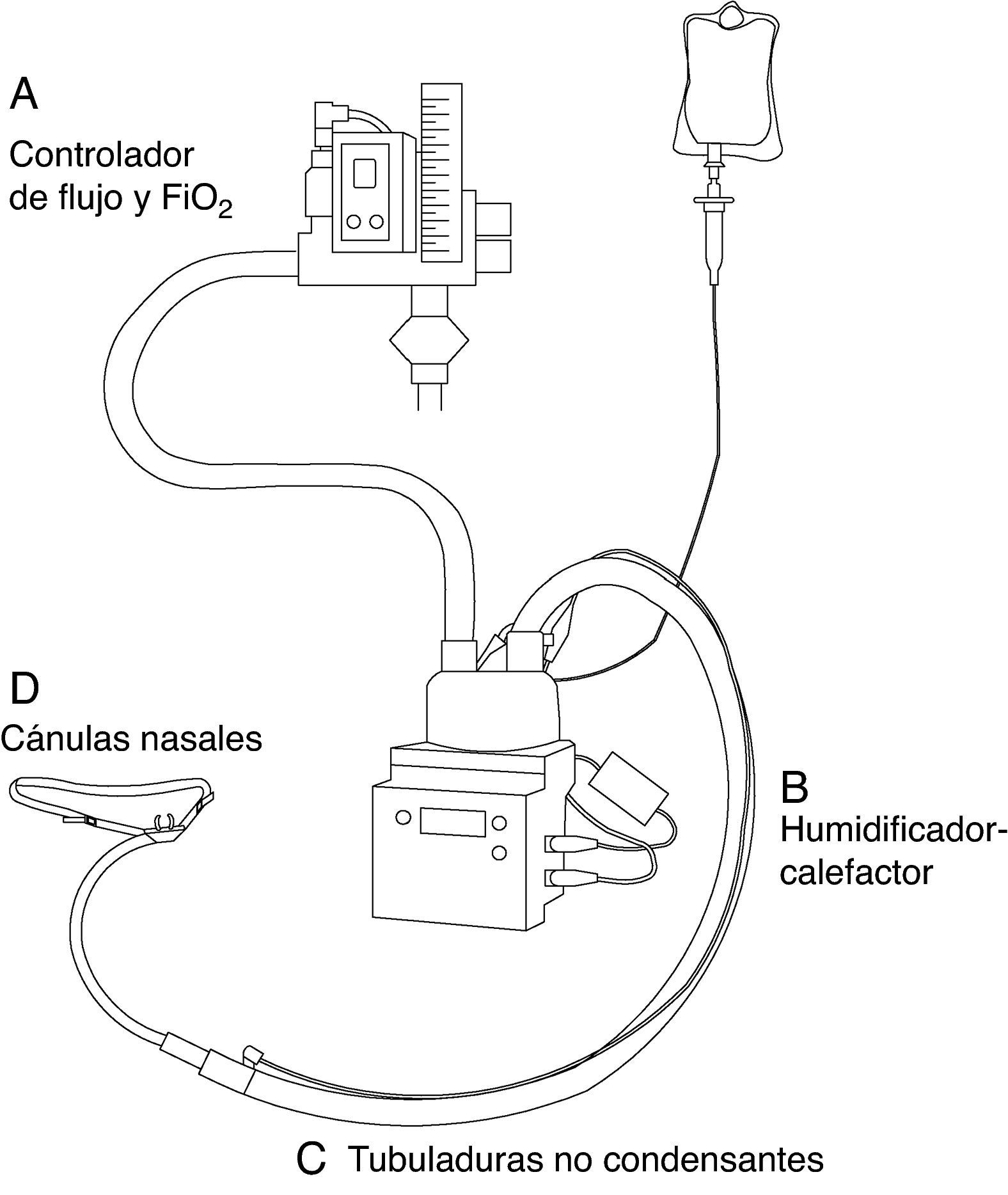
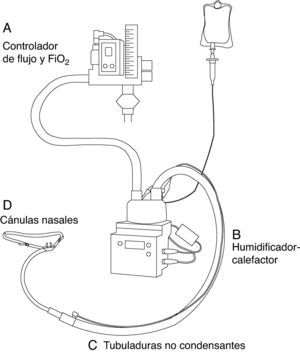
EquipamientoPara la administración de OAF se necesitan 4 componentes: 1) interface con el paciente; 2) sistema de administración de alto flujo que permita controlar este y la FiO2 administrada; 3) sistema humidificador-calefactor, y 4) tubuladuras no condensantes (fig. 1).
InterfaceLa interface que se utiliza son unas cánulas nasales especiales hechas de silicona y más largas que las cánulas convencionales. Existen varios tamaños y, por tanto, se debe seleccionar aquel que mejor se adapte a las narinas de nuestro paciente. Además, existen adaptadores para los pacientes traqueostomizados.
Controlador de flujo y fracción inspirada de oxígenoSe necesita un sistema que permita administrar gas a alto flujo (0-60L/min) y, además, ajustar la FiO2 administrada. Existen 2 sistemas distintos para lograr esto:
- -
Mezcla de oxígeno con aire comprimido mediante 2 tomas de pared independientes conectadas con una pieza en «Y» o mediante respiradores comerciales (Dräger, Lübeck, Alemania), entre otros.
- -
Mezcla de oxígeno con aire ambiente mediante turbina (sistema AirvoTM, Fisher & Paykel Healthcare Ltd., Auckland, Nueva Zelanda).
La clave fundamental para su uso clínico es la humidificación efectiva del gas administrado. Los sistemas comerciales más utilizados son el sistema OptiflowTM(Fisher & Paykel Healthcare Ltd., Auckland, Nueva Zelanda) y el VapothermTMPrecision Flow (Vapotherm, Exeter, EE. UU.). Estos sistemas permiten la administración del gas calentado a temperatura corporal (37°C) y con una humedad relativa del 100%.
Tubuladuras no condensantesExisten tubuladuras de distintas casas comerciales. Lo más importante a tener en cuenta en su elección es que estos sistemas deberían tener mecanismos para prevenir y minimizar la condensación en las tubuladuras, ya que se ha demostrado que este fenómeno favorece la aparición de infecciones23.
Mecanismos fisiológicos de acción y efectos clínicos del alto flujoLa OAF presenta unas características y mecanismos de acción que pueden ser especialmente beneficiosos en pacientes con IRA grave. A continuación revisaremos los principales mecanismos por los que se logran los efectos beneficiosos de la OAF.
Mejoría de la oxigenaciónLa OAF presenta como uno de sus principales beneficios la mejoría de la hipoxemia de los pacientes con IRA. Este hecho se logra mediante varios mecanismos, siendo los principales: la menor dilución con el aire ambiente del gas suministrado durante la inspiración y una cierta presurización de la vía aérea, dando lugar a un cierto efecto CPAP-like.
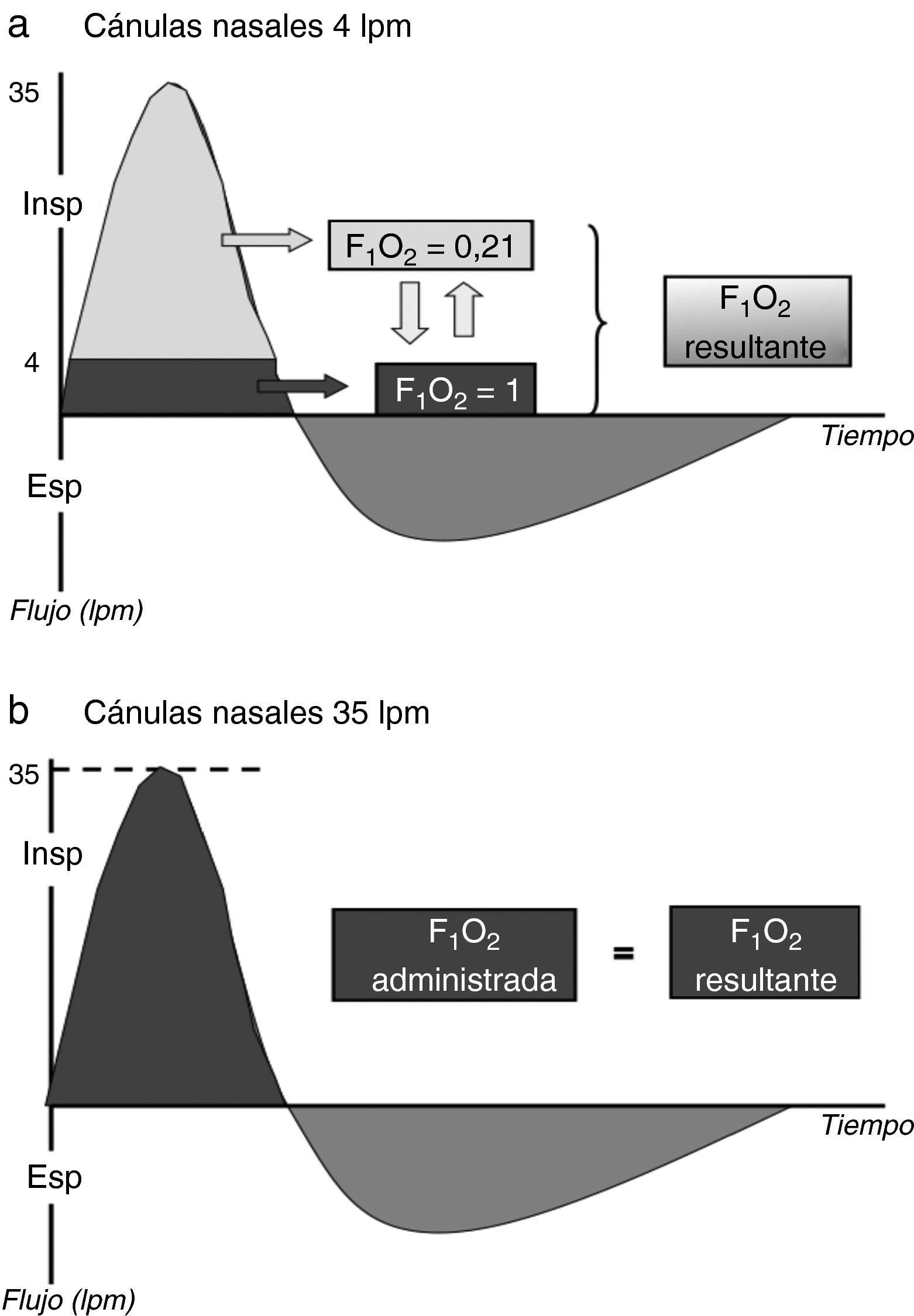
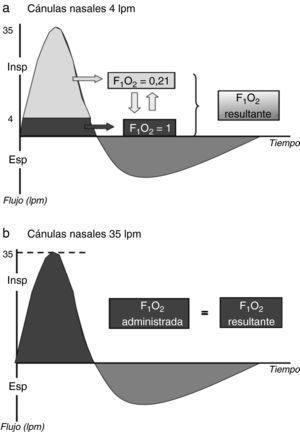
Menor diluciónUno de los beneficios de la OAF es la posibilidad de suministrar un flujo suficiente para satisfacer el pico de demanda inspiratoria (PDI) del paciente, con lo que la FiO2 suministrada se aproxima a la real que recibe el enfermo. Esto se debe a que el flujo de gas suministrado no se diluiría con aire ambiente (fig. 2). En condiciones normales, el PDI es de aproximadamente 30-40L/min24, por lo tanto, este podría ser, a priori, un rango de flujo recomendado cuando se empieza a utilizar la OAF. En pacientes con IRA grave, el PDI será probablemente mayor. Por este motivo, son precisamente estos pacientes donde el fenómeno de dilución del oxígeno es especialmente importante. Este hecho explicaría, al menos en parte, la mejora en la oxigenación de estos pacientes con la OAF25,26. Por otro lado, gracias a que se minimiza la dilución del oxígeno administrado con el aire ambiente, se consigue un mejor control de la concentración de oxígeno administrado27–29.
Dilución del oxígeno administrado usando un sistema de bajo flujo (a) o alto flujo (b). En gris oscuro: oxígeno; en gris claro: aire ambiente. Durante una inspiración normal, el pico de demanda inspiratoria es de 30-40L/min. Con el uso de la oxigenoterapia de alto flujo, la FiO2 administrada sería igual a la real, mientras que con un sistema de bajo flujo la FiO2 real sería menor a la administrada.
Otro posible mecanismo de acción es la generación de una cierta presión positiva en la vía aérea. Este incremento de presiones se ha demostrado a nivel de nasofaringe, de cavidad oral, así como de presiones esofágicas teleespiratorias y traqueales17–19.
Varios estudios han demostrado que con la utilización de flujos de entre 35 y 60L/min se consiguen presiones medias espiratorias a nivel de faringe de 2-3cmH2O con la boca abierta y de 5-7cmH2O con la boca cerrada18,19. Además, se ha demostrado que el uso de la OAF permite un aumento de la impedancia pulmonar al final de la espiración15,16, parámetro que se correlaciona con el volumen pulmonar. Así pues, este hecho es importante ya que significa que la mejoría en la oxigenación sería debida en parte a una mejora del reclutamiento alveolar5,26,30, debida al menos en parte a este aumento de presiones de la vía aérea.
Disminución del espacio muertoOtro de los aspectos a tener en cuenta es que el flujo suministrado directamente a la nasofaringe lava CO2 del receptáculo anatómico, lo que evita la reinhalación y proporciona un reservorio de gas fresco14,31. Este hecho reduce el espacio muerto anatómico e incrementa la ventilación alveolar12, dando lugar a una mejor tolerancia al ejercicio32, una reducción de la disnea y una mejor oxigenación17.
Disminución del trabajo respiratorio y del coste metabólico del acondicionamiento de gasesEl uso de gas totalmente acondicionado (suministrado a temperatura y humedad ideales) ha demostrado una mejor tolerancia y comodidad en los pacientes con IRA5,33. Pero también permite una disminución de la frecuencia respiratoria5,16,29 y una mejoría en la oxigenación. El acondicionamiento del gas administrado que permite la OAF afecta indirectamente a la oxigenación. La humidificación activa mejora la función mucociliar, facilita la expulsión de secreciones y disminuye la formación de atelectasias, lo que mejora la ratio ventilación/perfusión y la oxigenación5. Además, la administración de gas totalmente acondicionado permite una disminución en la resistencia de la vía aérea, lo que disminuiría el trabajo respiratorio del paciente4,26.
Efecto sobre el patrón ventilatorio y hemodinámicoDurante la inspiración, la presión negativa limita el flujo inspiratorio debido al colapso que se produce en la nasofaringe. La OAF, al generar cierto grado de presión positiva en la vía aérea, permite contrarrestar este fenómeno34. Dado que la OAF permite administrar flujos iguales o mayores al PDI del paciente, podría minimizar la resistencia de la vía aérea superior disminuyendo el trabajo respiratorio12. Se ha demostrado, además, una mejoría de la sincronía toracoabdominal con la OAF en comparación con la oxigenoterapia convencional35.
Por otra parte, el uso de OAF da lugar a un aumento de la impedancia pulmonar y, por lo tanto, a un aumento de los volúmenes tidales15,16. Este hecho se suele acompañar de una disminución de la frecuencia respiratoria sin cambios en la PaCO25,26,30. Tanto este cambio en el patrón ventilatorio, que podría conllevar una reducción del trabajo respiratorio, como la generación de un cierto grado de presión positiva intratorácica podrían generar cambios en el patrón hemodinámico de los pacientes en situación de IRA36. Un estudio reciente ha analizado los efectos hemodinámicos de la OAF en pacientes con insuficiencia cardíaca estable20. Estos efectos consistían en una disminución de la precarga del ventrículo derecho (medida a través de una disminución del colapso de la vena cava inferior), lo que podría suponer una mejora hemodinámica en los pacientes con IRA secundaria a disfunción miocárdica20.
Mayor comodidadDe forma frecuente, el fracaso de la VMNI se produce por la intolerancia a las interfaces. Los pacientes pueden experimentar claustrofobia o ansiedad, pueden provocar eritema, dolor o ulceración en el puente nasal, así como sequedad y congestión nasal, irritación ocular y distensión gástrica. Además, las posibles fugas aéreas añaden malestar y pueden interferir con el disparo y ciclado del respirador.
Toda la evidencia científica que existe al respecto refleja que la tolerancia a la OAF es tan buena o mejor que la de otros métodos de oxigenoterapia30, ya que permite un mayor bienestar5,36 y genera menos ruido37 y menor sequedad nasal5. Además, con este sistema se facilita la comunicación oral y permite la ingesta sin desconexiones del circuito.
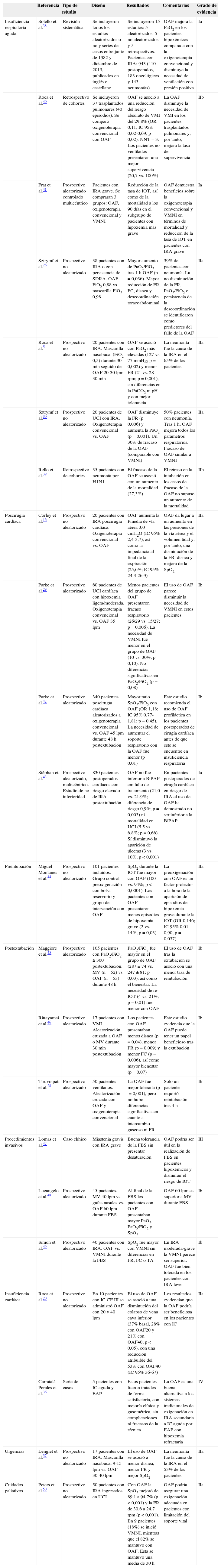
Principales indicaciones clínicasDebido a los diferentes mecanismos de acción expuestos previamente, la OAF presenta un amplio espectro de aplicaciones clínicas38. Las principales áreas donde existe evidencia para su uso se muestran a continuación. Además, en la tabla 1 se resumen estas indicaciones analizando los principales estudios publicados y el grado de evidencia existente hasta el momento.
Grado de evidencia de las principales indicaciones clínicas para el uso de oxigenoterapia de alto flujo
| Referencia | Tipo de estudio | Diseño | Resultados | Comentarios | Grado de evidencia | |
|---|---|---|---|---|---|---|
| Insuficiencia respiratoria aguda | Sotello et al.38 | Revisión sistemática | Se incluyeron todos los estudios aleatorizados o no y series de casos entre junio de 1982 y diciembre de 2013, publicados en inglés o castellano | Se incluyeron 15 estudios: 5 aleatorizados, 5 no aleatorizados y 5 retrospectivos. Pacientes con IRA: 943 (410 postoperados, 183 oncológicos y 143 neumonías) | OAF mejora la PaO2 en los pacientes hipoxémicos comparada con la oxigenoterapia convencional y disminuye la necesidad de ventilación con presión positiva | Ia |
| Roca et al.40 | Retrospectivo de cohortes | Se incluyeron 37 trasplantados pulmonares (40 episodios). Se comparó oxigenoterapia convencional con OAF | OAF se asoció a una reducción del riesgo absoluto de VMI del 29,8% (OR 0,11; IC 95% 0,02-0,69; p=0,02). NNT=3. Los pacientes no ventilados presentaron una mejor supervivencia (20,7 vs. 100%) | La OAF disminuye la necesidad de VMI en los pacientes trasplantados pulmonares y, por tanto, mejora la tasa de supervivencia | IIb | |
| Frat et al.41 | Prospectivo aleatorizado controlado multicéntrico | Pacientes con IRA grave. Se compraran 3 grupos: OAF, oxigenoterapia convencional y VMNI | Reducción de la tasa de IOT, así como de la mortalidad a los 90 días en el subgrupo de pacientes con hipoxemia más grave | OAF demuestra beneficios sobre la oxigenoterapia convencional y VMNI en términos de mortalidad y reducción de la tasa de IOT en pacientes con IRA grave | Ia | |
| Sztrymf et al.26 | Prospectivo no aleatorizado | 38 pacientes con IRA o con persistencia de SDRA. OAF FiO2 0,88 vs. mascarilla FiO2 0,98 | Mayor aumento de PaO2/FiO2 tras 1h OAF (p=0,036). Mayor reducción de FR, FC, disnea y descoordinación toracoabdominal | 39% de pacientes con neumonía. La no disminución de la FR, PaO2/FiO2 o persistencia de la descoordinación se identificaron como predictores del fallo de la OAF | IIa | |
| Roca et al.5 | Prospectivo no aleatorizado | 20 pacientes con IRA. Mascarilla nasobucal (FiO2 0,5) durante 30min seguido de OAF 20-30lpm 30min | OAF se asoció con PaO2 más elevadas (127 vs. 77mmHg; p=0,002) y menor FR (21 vs. 28rpm; p=0,001), sin diferencias en la PaCO2 ni pH y con mejor tolerancia | La neumonía fue la causa de la IRA en el 65% de los pacientes | IIa | |
| Sztrymf et al.30 | Prospectivo no aleatorizado | 20 pacientes de UCI con IRA. Oxigenoterapia convencional vs. OAF | OAF disminuye la FR (p=0,006) y aumenta la PaO2 (p=0,001). Un 30% de fracaso de la OAF (comparable con VMNI) | 50% pacientes con neumonía. Tras 1h, OAF mejora todos los parámetros respiratorios. Fracaso de OAF similar a VMNI | IIa | |
| Rello et al.39 | Retrospectivo de cohortes | 35 pacientes con neumonía por H1N1 | El fracaso de la OAF se asoció con un aumento de la mortalidad (27,3%) | El retraso en la intubación en los casos de fracaso de la OAF no supuso un aumento de la mortalidad | IIb | |
| Poscirugía cardíaca | Corley et al.16 | Prospectivo no aleatorizado | 20 pacientes con IRA poscirugía cardíaca. Oxigenoterapia convencional vs. OAF | OAF aumenta la Pmedia de vía aérea 3,0cmH2O (IC 95% 2,4-3,7), así como la impedancia al final de la expiración (25,6%; IC 95% 24,3-26,9) | OAF da lugar a un aumento en las presiones de la vía aérea y el volumen tidal y, por tanto, una disminución de la FR, disnea y mejora de la SpO2 | IIa |
| Parke et al.29 | Prospectivo aleatorizado | 60 pacientes de UCI cardíaca con hipoxemia ligera/moderada. Oxigenoterapia convencional vs. OAF 35lpm | Menos pacientes del grupo de OAF presentaron fracaso respiratorio (26/29 vs. 15/27; p=0,006). La necesidad de VMNI fue menor en el grupo de OAF (10 vs. 30%; p=0,10). No diferencias significativas en PaO2/FiO2 (p=0,08) | El uso de OAF parece disminuir la necesidad de VMNI en estos pacientes | Ib | |
| Parke et al.42 | Prospectivo aleatorizado | 340 pacientes poscirugía cardíaca aleatorizados a oxigenoterapia convencional vs. OAF 45lpm durante 48h postextubación | Mayor ratio SpO2/FiO2 con OAF (OR 1,18; IC 95% 0,77-1,81; p=0,45). La necesidad de aumentar el soporte respiratorio con la OAF fue menor (p=0,01) | Este estudio recomienda el uso de OAF profiláctica en los pacientes postoperados de cirugía cardíaca antes de que este se encuentre en insuficiencia respiratoria | Ib | |
| Stéphan et al.43 | Prospectivo aleatorizado, multicéntrico. Estudio de no inferioridad | 830 pacientes postoperados cardíacos con riesgo elevado de IRA postextubación | OAF no fue inferior a BiPAP en: fallo de tratamiento (21,0 vs. 21.9%; diferencia de riesgo 0,9%; p=0,003) ni mortalidad en UCI (5,5 vs. 6.8%; p=0,66). Sí disminuyó la aparición de úlceras (3 vs. 10%; p<0,001) | En pacientes postoperados de cirugía cardíaca en riesgo de IRA el uso de OAF ha demostrado no ser inferior a la BiPAP | Ia | |
| Preintubación | Miguel-Montanes et al.44 | Prospectivo no aleatorizado | 101 pacientes incluidos. Grupo control preoxigenación con bolsa reservorio y grupo de intervención con OAF | SpO2 durante la IOT fue mayor con OAF (100 vs. 94%; p<0,0001). Los pacientes con OAF presentaron menos episodios de hipoxemia grave (2 vs. 14%; p=0,03) | La preoxigenación con OAF es un factor protector a la hora de la aparición de episodios de hipoxemia grave durante la IOT (OR 0,146; IC 95% 0,01-0,90; p=0,037) | IIa |
| Postextubación | Maggiore et al.45 | Prospectivo aleatorizado | 105 pacientes con PaO2/FiO2≤300 postextubación. MV (n=52) vs. OAF (n=53) durante 48h | PaO2/FiO2 fue mayor en el grupo de OAF (287±74 vs. 247±81; p=0,03), así como el bienestar. La necesidad de re-IOT (4 vs. 21%; p=0,01) fue menor con OAF | El uso de OAF tras la extubación se asoció con una menor tasa de reintubación | Ib |
| Rittayamai et al.46 | Prospectivo aleatorizado | 17 pacientes con VMI. Aleatorización cruzada a OAF o MV durante 30min postextubación | Los pacientes con OAF presentaban menos disnea (p=0,04), menor FR (p=0,009) y menor FC (p=0,006), así como mayor bienestar (p=0,07) | Este estudio evidencia que la OAF puede tener un papel beneficioso tras la extubación | Ib | |
| Tiruvoipati et al.28 | Prospectivo aleatorizado | 50 pacientes ventilados. Aleatorización cruzada con OAF y oxigenoterapia convencional | La OAF fue mejor tolerada (p=0,001), pero no hubo diferencias significativas en cuanto a intercambio gaseoso ni FR | Solo un paciente requirió reintubación tras 4h | Ib | |
| Procedimientos invasivos | Lomas et al.47 | Caso clínico | Miastenia gravis con IRA grave | Buena tolerancia de la FBS sin presentar desaturación | OAF podría ser útil en la realización de FBS en pacientes hipoxémicos y disminuir el riesgo de IOT | III |
| Lucangelo et al.48 | Prospectivo aleatorizado | 45 pacientes. MV 40lpm vs. gafas nasales vs. OAF 60lpm durante FBS | Al final de la FBS los pacientes con OAF presentaban mayor PaO2, PaO2/FiO2 y SpO2 | OAF 60lpm es superior a MV durante FBS | Ib | |
| Simon et al.49 | Prospectivo aleatorizado | 40 pacientes con IRA. OAF vs. VMNI durante la FBS | SpO2 fue mayor con VMNI sin diferencias en FR, FC o TA | En IRA moderada-grave la VMNI parece ser superior. OAF fue bien tolerada en los pacientes con IRA leve | Ib | |
| Insuficiencia cardíaca | Roca et al.20 | Prospectivo no aleatorizado | En 10 pacientes con IC CF III se administró OAF con 20 y 40lpm | El uso de OAF se asoció a una disminución del colapso de vena cava inferior (37% basal, 28% con OAF20 y 21% con OAF40; p<0,05), con una reducción atribuible del 53% con OAF40 (IC 95% 36-67) | Los resultados evidencian que la OAF podría ser beneficiosa en los pacientes con IC | IIa |
| Carratalá Perales et al.36 | Serie de casos | 5 pacientes con IC aguda y EAP | Estos pacientes fueron tratados de forma satisfactoria, con mejoría clínica y gasométrica, sin complicaciones ni fracasos de la técnica | La OAF es una buena alternativa a los sistemas tradicionales de oxigenación en IRA secundaria a IC aguda por EAP con hipoxemia refractaria | IV | |
| Urgencias | Lenglet et al.37 | Prospectivo no aleatorizado | 17 pacientes con IRA. Mascarilla nasobucal 9-15lpm vs. OAF 30-40lpm | El uso de OAF se asoció a menor disnea, menor FR y mejor SpO2 | La neumonía fue la causa de la IRA en el 53% de los pacientes | IIa |
| Cuidados paliativos | Peters et al.50 | Prospectivo no aleatorizado | 50 pacientes con IRA ingresados en UCI | Con OAF la SpO2 mejoró de 89,1 a 94,7% (p<0,001) y la FR de 30,6 a 24,7rpm (p<0,001). En 9 pacientes (18%) se inició VMNI, mientras que el 82% se mantuvo con OAF. Esta se mantuvo una media de 30h | OAF podría asegurar una oxigenación adecuada en pacientes con limitación del soporte vital | IIa |
BiPAP: sistema de bipresión positiva; EAP: edema agudo de pulmón; FBS: fibrobroncoscopia; FC: frecuencia cardíaca; FiO2: francción inspirada de oxígeno; FR: frecuencia respiratoria; IC: insuficiencia cardíaca; IC 95%: intervalo de confianza al 95%; IOT: intubación orotraqueal; IRA: insuficiencia respiratoria aguda; MV: mascarilla Venturi; NNT: número de pacientes necesarios a tratar; OAF: oxigenoterapia de alto flujo; OR: odds ratio; PaO2: presión parcial arterial de oxigeno; SDRA: síndrome de distrés respiratorio agudo; SpO2: saturación de oxígeno; TA: tensión arterial; UCI: Unidad de Cuidados Intensivos; VMI: ventilación mecánica invasiva; VMNI: ventilación mecánica no invasiva.
Niveles de evidencia según la U. S. Agency for Health Research and Quality (Ia: metaanálisis o varios ensayos controlados aleatorizados. Ib: al menos un ensayo controlado aleatorizado. IIa: al menos un estudio controlado bien diseñado sin aleatorizar. IIb: al menos un estudio de cohortes. III: estudios descriptivos no experimentales bien diseñados, como los estudios comparativos, estudios de correlación o estudios de casos y controles. IV: documentos u opiniones de comités de expertos o experiencias clínicas o estudios de series de casos).
El estudio de Roca et al.5 fue el primero en demostrar los beneficios del uso de la OAF en pacientes con IRA. Tras solo 30min de uso de la OAF evidenciaban una mejoría significativa tanto en los parámetros clínicos como fisiológicos. Estos resultados fueron confirmados posteriormente por Sztrymf et al.30, quienes corroboraron una reducción de la frecuencia respiratoria y una mejoría en la oxigenación de estos pacientes.
Además, el uso de OAF permite un mejor manejo de las secreciones respiratorias30,39, hecho que podría ser de especial importancia en los pacientes con IRA de etiología infecciosa.
Por otra parte, el uso de la OAF podría reducir la necesidad de VMNI e incluso de ventilación mecánica invasiva (VMI) en los pacientes con IRA. Este posible beneficio de la OAF se ha analizado en 4 estudios26,29,30,40. En el de Sztrymf et al.30 se evidenciaba un fracaso de la OAF de aproximadamente un 30%, lo cual es equiparable a la tasa de fracasos de la VMNI30. El grupo de Parke et al.29 encontró que solo un 10% de los pacientes con IRA moderada-grave tratados con OAF necesitaban de VMI, mientras que este porcentaje ascendía hasta un 30% en los que se usaba mascarilla nasobucal. Más recientemente, en una población de trasplantados pulmonares con IRA, la OAF disminuía significativamente la necesidad de VMI con una reducción del riesgo absoluto de ventilación mecánica del 30%, siendo necesarios solo 3 pacientes para evitar una intubación, con potenciales efectos sobre la morbimortalidad y el coste-eficacia del sistema40.
Sin embargo, la cuestión principal de si el uso de OAF permite disminuir la necesidad de VMI persiste todavía sin resolver. La impresión de muchos clínicos es que efectivamente el uso de OAF evita la intubación en muchos pacientes con IRA; sin embargo, no existe ningún ensayo clínico controlado que así lo demuestre. Un estudio reciente que evaluó el impacto clínico de la OAF en pacientes con IRA grave encontró una tasa de éxitos del 68%, requiriendo de ventilación mecánica (ya sea invasiva o no invasiva) solo un 32% de los pacientes26. Todavía más llamativos son los resultados del estudio FLORALI41, en el que se muestran los beneficios de la OAF en comparación con la oxigenoterapia convencional y la VMNI en términos de mortalidad y reducción de las tasas de intubación en pacientes con hipoxemia grave. En este estudio se analizaron pacientes con IRA grave tratados con OAF, oxigenoterapia convencional o VMNI. Se evidenció una menor tasa de intubación, así como una reducción en la mortalidad en el subgrupo de pacientes más graves (con una relación PaO2/FiO2<200mmHg) que fueron tratados con OAF.
Por otra parte, es importante conocer que existen una serie de predictores precoces (en las primeras 12h) del fallo de la OAF, como son la persistencia de la taquipnea, la descoordinación toracoabdominal y la usencia de mejoría de la hipoxemia26.
En resumen, en los pacientes con IRA grave el uso de OAF podría permitir: 1) una mejoría rápida de la disnea; 2) una mejoría de la hipoxemia; 3) un mejor manejo de las secreciones respiratorias, y 4) una disminución de la necesidad de ventilación mecánica.
Preoxigenación en la maniobra de la intubación traquealEn los pacientes críticos la maniobra de intubación orotraqueal se asocia hasta con un 20% de complicaciones potencialmente graves, básicamente relacionadas con la aparición de hipoxemia en el contexto del procedimiento51. La VMNI podría utilizarse para preoxigenar al paciente que va a ser intubado. Sin embargo, ha de retirarse durante la laringoscopia y, por lo tanto, no permite la oxigenación del paciente durante el procedimiento. En cambio, el uso de OAF no interfiere con la laringoscopia y, por tanto, permitiría la administración de oxígeno durante el procedimiento14. Miguel-Montanes et al. han demostrado que con el uso de la OAF durante la preoxigenación se reduce la prevalencia de hipoxemia grave durante la maniobra de intubación cuando se compara con el uso de una mascarilla con reservorio44. Del mismo modo, en un estudio experimental realizado recientemente se demostró que la administración de oxígeno a flujos de 10L/min retrasa la aparición de hipoxemia grave durante la apnea, lo que evidencia que el uso de OAF durante la intubación orotraqueal podría ser útil sobre todo en pacientes hipoxémicos51.
Weaning de la ventilación mecánicaEl uso de la OAF tras retirar la VMI podría ser útil tanto para prevenir como para tratar la insuficiencia respiratoria postextubación14,42. Se han publicado 4 estudios al respecto y todos han demostrado una mejoría de todos los parámetros respiratorios45,46, así como del bienestar si se compara con el uso de mascarilla nasobucal28,45, una disminución en la necesidad de aumento del soporte respiratorio42, además de una reducción de la tasa de reintubación (del 21 al 4%)45. Recientemente, el grupo de Stéphan43 ha publicado un estudio de no inferioridad de OAF frente a VMNI, en concreto BiPAP, en pacientes postoperados cardíacos en riesgo de insuficiencia respiratoria. Este estudio no evidencia diferencias en cuanto a fracaso del tratamiento ni mortalidad en UCI entre los 2 sistemas, y en cambio sí muestra que el uso de OAF se relaciona con una disminución significativa de lesiones cutáneas ya dentro de las primeras 24h de uso. Por otro lado, el uso de OAF en el proceso de decanulación de los pacientes traqueostomizados es otra área prometedora de desarrollo; sin embargo, no existe ningún trabajo publicado en el momento actual.
Oxigenoterapia durante procedimientos invasivosDurante la realización de procedimientos invasivos como son las fibrobroncoscopias es habitual que se produzca un empeoramiento de la hipoxemia en relación con la hipoventilación que se produce y el uso de sedantes. Este empeoramiento de la hipoxemia puede ser todavía mayor si se realiza un lavado broncoalveolar y puede persistir varias horas después de la realización de la exploración48. El uso de OAF ha demostrado efectos beneficiosos en cuanto a un menor empeoramiento de la hipoxemia y comodidad si se compara con la oxigenoterapia convencional47,48. Recientemente, el estudio de Simon et al.49 mostró un menor grado de hipoxemia durante la realización de la fibrobroncoscopia a favor de la VMNI en los pacientes con hipoxemia grave; sin embargo, la tolerancia y el bienestar de estos pacientes seguían siendo muy superiores con el uso de OAF49. Del mismo modo, la utilización de OAF también debería considerarse en la realización de otros procedimientos invasivos, como podrían ser las ecocardiografías transesofágicas o las endoscopias digestivas14,31.
Insuficiencia cardíacaNo es infrecuente encontrar pacientes con insuficiencia cardíaca aguda que, una vez estabilizados, persisten hipoxémicos y disneicos a pesar de la oxigenoterapia convencional. Los resultados de un estudio reciente muestran que en estos pacientes la OAF mejora la disnea debido a una reducción de la frecuencia respiratoria y a una mejoría de la hipoxemia36. Por otra parte, también se ha observado que en pacientes con insuficiencia cardíaca crónica en fase estable, la OAF daba lugar a una disminución en el colapso de la vena cava inferior sin disminución del gasto cardíaco, evidenciando que el uso de OAF provocaba una disminución de la precarga de ventrículo derecho probablemente secundaria a la generación de cierta presión positiva intratorácica y al aumento del volumen pulmonar20. Por lo tanto, la mejoría que proporciona la OAF en este tipo de pacientes podría deberse fundamentalmente tanto a la mejoría de la oxigenación como a la mejoría del patrón hemodinámico11,20,36. Sin embargo, no existe ningún estudio que compare VMNI con OAF en la fase aguda del edema pulmonar.
Utilización fuera del servicio de Medicina IntensivaLa hipoxemia y la disnea también son dos de los síntomas más frecuentes en los pacientes ingresados en los servicios de Urgencias. Lenglet et al.37 analizaron los potenciales efectos beneficiosos y la factibilidad del uso de la OAF en pacientes con IRA (secundaria en su mayoría a una infección respiratoria o edema agudo de pulmón) ingresados en Urgencias comparándola con la oxigenoterapia convencional. Los resultados evidenciaron que la OAF conseguía una mejoría más rápida de la sensación disneica, la oxigenación y los demás parámetros respiratorios, además de presentar una mejor tolerancia y ser más confortable para los pacientes, sin que su uso presentase mayor dificultad que el empleo de la oxigenoterapia convencional. Su uso en el transporte extrahospitalario queda todavía por estudiar.
Cuidados paliativosEn los pacientes en los que la VMI no está indicada, el uso de la OAF podría ser beneficioso15 ya que este dispositivo permite una disminución de la sensación disneica y una mejoría de la hipoxemia y de la tos, mediante un dispositivo que presenta buena tolerancia por parte de los pacientes y que les permite comunicarse e incluso alimentarse37,50,52,53. De hecho, una constante en muchos de los estudio publicados hasta la fecha es la mejoría en el bienestar de los pacientes tratados con OAF.
Exacerbación de la enfermedad pulmonar obstructiva crónicaEn el caso de la insuficiencia respiratoria hipercápnica, la OAF también podría ser beneficiosa en términos de reducción de la PaCO2 y de mejora del pH probablemente en relación con el aumento de presión que genera a nivel de la vía aérea superior54. Sin embargo, es importante resaltar que, en estos pacientes, podría ser útil la administración de altos flujos de gas siempre y cuando utilicemos FiO2 bajas para disminuir el riesgo de hipercapnia. Además, estos pacientes con enfermedad respiratoria crónica se benefician especialmente de la mejoría de la función mucociliar que favorece la OAF54,55. Sin embargo, son necesarios más estudios que comparen el uso de OAF con el de VMNI/CPAP en este subgrupo de pacientes.
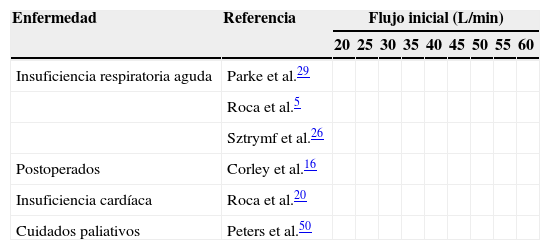
Inicio de la oxigenoterapia de alto flujoEn la tabla 2 se resumen los flujos de gas utilizados en los diferentes estudios. En general, se podría utilizar un flujo inicial de entre 30 y 40L/min. En cuanto a la FiO2, debemos administrar la necesaria para obtener la saturación arterial de oxígeno deseada. Por otra parte, es importante asegurarnos de que el sistema alcanza la temperatura adecuada (37°C) para la administración del gas.
Weaning del sistemaEs difícil establecer pautas para el destete de la OAF y su sustitución por un sistema de oxigenoterapia convencional. Sin embargo, parecería razonable primero disminuir la FiO2 y, posteriormente, el flujo6. Una recomendación aceptable podría ser la de mantener el flujo administrado hasta alcanzar una oxigenación correcta con una FiO2 menor de 0,5. La reducción en el flujo debería ser lenta (5L/min cada 6-8h). Finalmente, cuando obtengamos una oxigenación correcta con 20L/min o menos y con una FiO2 menor de 0,5 podríamos plantearnos la sustitución de la OAF por un sistema de oxigenoterapia convencional56. No obstante, en algunos pacientes es necesario el uso de OAF de forma intermitente durante la fase de destete.
Contraindicaciones y complicacionesNo se han descrito efectos adversos importantes en relación con la utilización de la OAF. Los sistemas de humidificación activa permiten administrar gas totalmente acondicionado y, por lo tanto, los efectos secundarios a nivel de las estructuras nasofaríngeas se minimizan enormemente. En los pacientes con EPOC, la utilización de altas concentraciones de oxígeno puede producir acidosis respiratoria debido a la reducción de la frecuencia respiratoria y las alteraciones de la ventilación-perfusión57. Existen varios sistemas de alto flujo disponibles. El ideal es aquel que resulte más confortable para el paciente y que tenga el mejor sistema de humidificación y calentamiento con tubuladuras no condensantes. Estos sistemas deberían tener mecanismos para prevenir y minimizar la condensación en las tubuladuras, ya que este fenómeno favorece la aparición de infecciones, como, por ejemplo, un brote de colonización o infección por Ralstonia reportado por la FDA con el sistema de VapothermTM23, ya controlado en la actualidad.
ConclusionesEn resumen, la OAF es una nueva opción de oxigenoterapia que, mediante el calentamiento y la humidificación, permite la administración de gas totalmente acondicionado a muy altos flujos, mejorando la oxigenación y el bienestar de los pacientes, y minimizando los efectos adversos sobre las estructuras nasofaríngeas. Con la evidencia actual, la OAF es una opción terapéutica atractiva y útil en los pacientes con IRA, ya que permite una mejoría de la oxigenación, una disminución del trabajo respiratorio y un mayor bienestar de los pacientes. Sin embargo, son necesarios más estudios que determinen su posible impacto en términos de morbimortalidad y coste-efectividad.
Conflicto de interesesFisher & Paykel colabora con el IMIM mediante una beca de investigación posdoctoral.