Identificar los determinantes asociados a la estrategia invasiva precoz (EIP) en mujeres con síndrome coronario agudo sin elevación de ST (SCASEST).
DiseñoEstudio de cohortes retrospectivo. Análisis crudo y ajustado de la realización de EIP mediante regresión logística no condicional.
ÁmbitoUnidades coronarias participantes en 2010-2011 en el registro ARIAM-SEMICYUC.
PacientesCuatrocientas cuarenta mujeres con SCASEST. Se excluyeron 16 por datos insuficientes y 58 con coronariografía electiva (>72h).
Variables analizadasDemográficas, factores de riesgo coronario, medicación previa, comorbilidad. Características clínicas, analíticas, hemodinámicas y electrocardiográficas del episodio.
ResultadosLas mujeres tratadas conservadoramente presentaban mayor edad, mayor prevalencia de anticoagulación oral, diabetes, lesiones coronarias previas e insuficiencia cardiaca (p<0,005), mayor riesgo hemorrágico e isquémico basal (p=0,05) y mayor frecuencia cardiaca al ingreso (p<0,05). Tras el ajuste solo la edad mayor de 80 años (OR: 0,48; IC 95%: 0,27-0,82; p=0,009), las lesiones coronarias conocidas (OR: 0,47; IC 95%: 0,26-0,84, p=0,011) y la frecuencia cardiaca (OR: 0,98; IC 95%: 0,97-0,99, p=0,003) se asociaron de forma independiente al tratamiento conservador. El tabaquismo (OR: 2,50; IC 95%: 1,20-5,19; p=0,013) y el electrocardiograma de alto riesgo (OR: 2,96; IC 95%: 1, 72-4,97; p<0,001) se asociaron a la EIP. La exclusión de muertes precoces (<24h) no alteró estos resultados.
ConclusionesEn mujeres con SCASEST el tabaquismo y el electrocardiograma de alto riesgo al ingreso son factores independientes asociados a la EIP. Las lesiones coronarias previas conocidas, la edad >80 años y el aumento de la frecuencia cardiaca son factores independientes asociados al tratamiento conservador.
To identify determinants associated to an early invasive strategy in women with acute coronary syndromes without ST elevation (NSTE-ACS).
DesignA retrospective cohort study was made. Crude and adjusted analysis of the performance of the early invasive strategy using logistic regression.
SettingCoronary Units enrolled in 2010 - 2011 in the ARIAM-SEMICYUC registry.
PatientsA total of 440 women with NSTE-ACS were studied. Sixteen patients were excluded due to insufficient data, together with 58 patients subjected to elective coronary angiography (> 72h).
Variables analyzedDemographic parameters, coronary risk factors, previous medication, comorbidity. Clinical, laboratory, hemodynamic and electrocardiographic data of the episode.
ResultsWomen treated conservatively were of older age, had oral anticoagulation, diabetes, previous coronary lesions, and heart failure (p<0,005), increased baseline bleeding and ischemic risk (p=0,05) and a higher heart rate upon admission (p<0,05). After adjustment, only age > 80 years (OR 0,48, 95% CI 0,27 to 0,82, p=0,009), known coronary lesions (OR 0,47, 95% CI 0,26-0,84, p=0,011), and heart rate (OR 0,98, 95% CI 0,97-0,99, p=0,003) were independently associated to conservative treatment. Smoking (OR 2.50, 95% CI 1.20 to 5.19, p=0,013) and high-risk electrocardiogram (OR 2.96, 95% CI 1.72 to 4.97, p<0,001) were associated to the early invasive strategy. The exclusion of early deaths (<24h) did not alter these results.
ConclusionsIn women with NSTE ACS, smoking and a high-risk electrocardiogram upon admission were independent factors associated to the early invasive strategy. Previous coronary lesions, age > 80 years and increased heart rate were independent factors associated to conservative treatment.
La controversia sobre la estrategia diagnóstica y terapéutica más adecuada en las mujeres con síndrome coronario agudo (SCA) sigue vigente. Estudios previos han demostrado diferencias fundamentales entre las características basales de hombres y mujeres que se presentan con síndrome coronario agudo sin elevación de ST (SCASEST): las mujeres presentan mayor edad, más comorbilidad (diabetes, hipertensión), más sintomatología atípica, mayor incidencia de insuficiencia cardiaca y menor prevalencia de enfermedad coronaria obstructiva, lo que puede favorecer una diferente estrategia diagnóstica y también diferente tratamiento1–4. Estas diferencias pueden explicarse por factores biológicos5, aunque también por la infrautilización de las directrices de tratamiento recomendadas por las sociedades científicas6 que son neutrales en sus recomendaciones con respecto al género7–10. Pese a ello, estudios recientes demuestran que las mujeres con SCA tienen aún una mayor probabilidad de ser tratadas de forma conservadora y presentan una mayor mortalidad intrahospitalaria11. Desde la perspectiva del intervencionismo coronario, esta mayor propensión al tratamiento conservador puede deberse a la diferente valoración de la relación riesgo-beneficio de la estrategia invasiva precoz (EIP) en las mujeres, sobre todo en pacientes de bajo riesgo12 ya que no reduce la tasa de mortalidad o el infarto de miocardio en comparación con una estrategia invasiva selectiva, a diferencia de lo que ocurre en los varones13. Esta recomendación se basa en el análisis de subgrupos de ensayos realizados hace una década14,15 donde el exceso de riesgo se concentraba sobre todo en la necesidad de revascularización quirúrgica tras el diagnóstico y no en la estrategia de revascularización percutánea precoz14.
Los estudios que analizan desigualdades en la utilización de procedimientos diagnósticos o terapéuticos en el SCA analizan a las mujeres en su conjunto1,2,11,16,17. Sin embargo, se ha prestado una menor atención a los subgrupos de mujeres en los que se concentra el mayor o menor esfuerzo terapéutico, en concreto respecto al intervencionismo coronario. La identificación de estos subgrupos con diferente probabilidad de ser sometidas a intervencionismo coronario precoz permitiría un análisis desagregado del problema de las desigualdades de esfuerzo terapéutico en mujeres.
El objetivo de este estudio es identificar alguno de los determinantes de la realización de la EIP en mujeres con SCASEST a partir de los datos del registro ARIAM-SEMICYUC18.
MétodosSe realizó un estudio de cohortes retrospectivo. Se incluyeron en el análisis 440 mujeres con SCASEST de menos de 48h de evolución. Se excluyeron 58 pacientes a las que les fue realizada una coronariografía electiva (>72h). Dieciséis pacientes fueron excluidas para el análisis por falta de datos analizables respecto a la estrategia recibida.
El desenlace principal del análisis fue la ejecución de una EIP definida como la realización de una angiografía coronaria seguida o no de revascularización dentro de las primeras 72h de ingreso.
Las variables incluidas como posibles predictores asociadas a la realización de la EIP incluyen factores demográficos como la edad, el uso de medicación previa al ingreso (AAS, tienopiridinas, betabloqueantes, IECAS-ARA II, estatinas, digoxina, antiarrítmicos y acenocumarol), factores de riesgo coronario (hipertensión arterial, diabetes, dislipidemia, obesidad, tabaquismo, antecedentes familiares), datos de comorbilidad (arteriopatía periférica, insuficiencia cardiaca, infarto de miocardio, angina, lesiones coronarias conocidas, accidente cerebrovascular [ACV], enfermedad pulmonar obstructiva crónica [EPOC] e insuficiencia renal), así como características clínicas (presentación con dolor en reposo, fibrilación auricular), analíticas (elevación o no de troponina), hemodinámicas (tensión arterial, Killip inicial y frecuencia cardiaca al ingreso) y electrocardiográficas del episodio. Se consideraron como cambios electrocardiográficos de alto riesgo aquellos sugestivos de afectación del tronco de coronaria izquierda, el descenso de ST de más de 2mm en más de 2 derivaciones, la elevación transitoria de ST, la FV primaria y el bloqueo AV de alto grado al ingreso19. Se optó por categorizar los valores de troponina de forma binaria de modo que la variable «troponina elevada» incluye cualquier valor de troponina distinto al rango normal. Se escogieron estas variables al ser aquellas que se manejan de forma habitual en el momento de decidir el tipo de estrategia a adoptar en cada caso.
También se consideró si los casos fueron atendidos en centros con disponibilidad de realizar un cateterismo. Se valoró el riesgo isquémico basal tanto mediante los diferentes niveles de estratificación de riesgo GRACE como con la escala TIMI. Los puntos de corte de riesgo considerados en la escala GRACE fueron los establecidos para estimar mortalidad intrahospitalaria8,10,20 para estimar riesgo bajo (<108), intermedio (109-140) y alto (>140). Respecto a la escala TIMI, se consideró riesgo aumentado con puntuaciones a partir de 49,21. El riesgo hemorrágico se cuantificó mediante un índice ad hoc basado en el número de predictores independientes de hemorragias mayores del registro GRACE22. Se consideró que todas las pacientes incluidas presentaban, de manera basal, al menos un factor de riesgo hemorrágico ya que el sexo femenino es uno de los predictores independientes de hemorragias mayores del registro GRACE. Las otras variables consideradas fueron la edad avanzada, los antecedentes de hemorragias, los valores basales de hemoglobina/hematocrito, la presión arterial media y la disfunción renal medida por la concentración de creatinina sérica o bien por la tasa de filtración glomerular calculada por la ecuación de Cockcroft-Gault19,23.
En el análisis estadístico-descriptivo se calcularon las proporciones para las variables categóricas y las medianas con percentiles 25 y 75 en el caso de variables continuas. Los contrastes de hipótesis sobre proporciones se realizaron mediante el test Ji-cuadrado. Las variables cuantitativas se contrastaron mediante pruebas no paramétricas (test de Mann-Whitney). Los contrastes fueron bilaterales con un nivel de significación alfa del 5%.
Para determinar los factores predictores independientes del cateterismo precoz aquellas variables asociadas en el análisis univariante a la realización de una EIP con una p<0,10 se incluyeron en un modelo de regresión logística binaria que se analizó mediante una estrategia hacia atrás, eliminándose en cada paso la variable menos significativa. El efecto de la asociación entre la edad y la realización de una EIP se analizó de forma gráfica. Dicha asociación no era lineal sino de tipo «mínimo umbral». Por ello, se optó por categorizar la edad como variable binaria con el punto de corte a nivel de dicho umbral (80 años) y como tal se introdujo en el modelo.
La eliminación de variables no dependió solamente de su nivel de significación, sino también de su impacto en las odds ratios (OR) ajustadas de las demás variables.
La asociación entre las variables predictoras y la realización de una EIP se estimó mediante el cálculo de las OR ajustadas y de sus intervalos de confianza (IC) de 95%.
Los análisis se realizaron con el programa estadístico Statistical Package for Social Sciences, versión 19.0 (SPSS, Chicago, Illinois).
ResultadosDurante el periodo de 2010 participaron 43 centros que aumentaron a 56 en 2011 (anexo). En 2010 se reclutaron 187 mujeres con SCASEST (27,7% del total de pacientes con SCASEST) y durante 2011, 253 pacientes (27,3%)18. De las 440 pacientes analizadas, 220 pacientes (60,1%) fueron sometidas a una EIP y 146 (39,9%) recibieron tratamiento conservador.
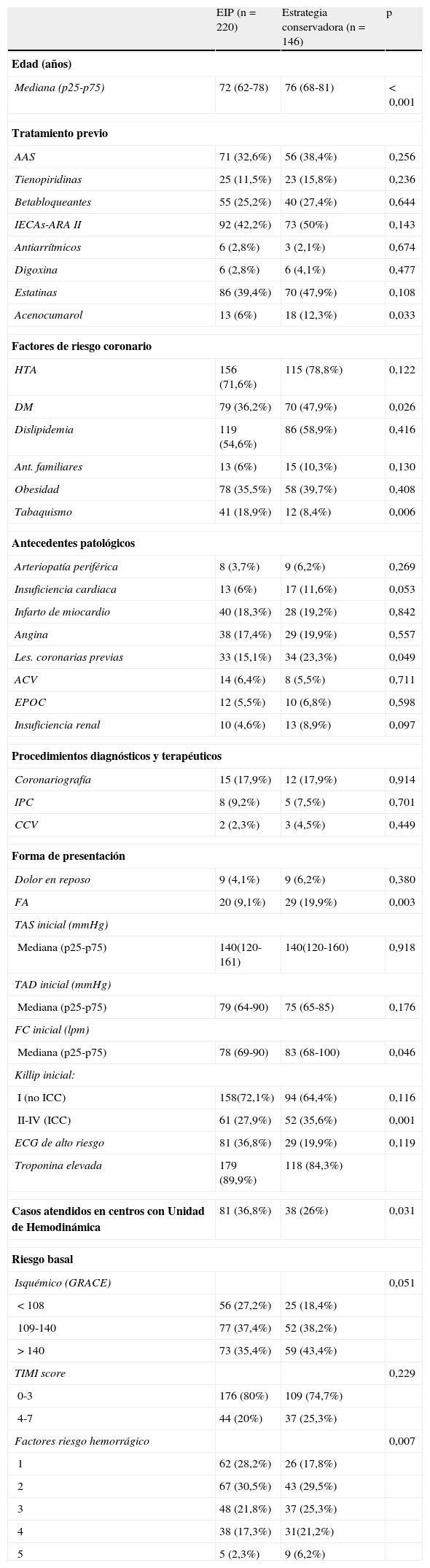
En el análisis univariante (tabla 1) los factores que se asociaron significativamente a la EIP en las mujeres fueron el tabaquismo, la disponibilidad de la Unidad de Hemodinámica en el centro donde se atiende el caso y los trazados electrocardiográficos de alto riesgo.
Características de los pacientes según la estrategia
| EIP (n=220) | Estrategia conservadora (n=146) | p | |
| Edad (años) | |||
| Mediana (p25-p75) | 72 (62-78) | 76 (68-81) | <0,001 |
| Tratamiento previo | |||
| AAS | 71 (32,6%) | 56 (38,4%) | 0,256 |
| Tienopiridinas | 25 (11,5%) | 23 (15,8%) | 0,236 |
| Betabloqueantes | 55 (25,2%) | 40 (27,4%) | 0,644 |
| IECAs-ARA II | 92 (42,2%) | 73 (50%) | 0,143 |
| Antiarrítmicos | 6 (2,8%) | 3 (2,1%) | 0,674 |
| Digoxina | 6 (2,8%) | 6 (4,1%) | 0,477 |
| Estatinas | 86 (39,4%) | 70 (47,9%) | 0,108 |
| Acenocumarol | 13 (6%) | 18 (12,3%) | 0,033 |
| Factores de riesgo coronario | |||
| HTA | 156 (71,6%) | 115 (78,8%) | 0,122 |
| DM | 79 (36,2%) | 70 (47,9%) | 0,026 |
| Dislipidemia | 119 (54,6%) | 86 (58,9%) | 0,416 |
| Ant. familiares | 13 (6%) | 15 (10,3%) | 0,130 |
| Obesidad | 78 (35,5%) | 58 (39,7%) | 0,408 |
| Tabaquismo | 41 (18,9%) | 12 (8,4%) | 0,006 |
| Antecedentes patológicos | |||
| Arteriopatía periférica | 8 (3,7%) | 9 (6,2%) | 0,269 |
| Insuficiencia cardiaca | 13 (6%) | 17 (11,6%) | 0,053 |
| Infarto de miocardio | 40 (18,3%) | 28 (19,2%) | 0,842 |
| Angina | 38 (17,4%) | 29 (19,9%) | 0,557 |
| Les. coronarias previas | 33 (15,1%) | 34 (23,3%) | 0,049 |
| ACV | 14 (6,4%) | 8 (5,5%) | 0,711 |
| EPOC | 12 (5,5%) | 10 (6,8%) | 0,598 |
| Insuficiencia renal | 10 (4,6%) | 13 (8,9%) | 0,097 |
| Procedimientos diagnósticos y terapéuticos | |||
| Coronariografía | 15 (17,9%) | 12 (17,9%) | 0,914 |
| IPC | 8 (9,2%) | 5 (7,5%) | 0,701 |
| CCV | 2 (2,3%) | 3 (4,5%) | 0,449 |
| Forma de presentación | |||
| Dolor en reposo | 9 (4,1%) | 9 (6,2%) | 0,380 |
| FA | 20 (9,1%) | 29 (19,9%) | 0,003 |
| TAS inicial (mmHg) | |||
| Mediana (p25-p75) | 140(120-161) | 140(120-160) | 0,918 |
| TAD inicial (mmHg) | |||
| Mediana (p25-p75) | 79 (64-90) | 75 (65-85) | 0,176 |
| FC inicial (lpm) | |||
| Mediana (p25-p75) | 78 (69-90) | 83 (68-100) | 0,046 |
| Killip inicial: | |||
| I (no ICC) | 158(72,1%) | 94 (64,4%) | 0,116 |
| II-IV (ICC) | 61 (27,9%) | 52 (35,6%) | 0,001 |
| ECG de alto riesgo | 81 (36,8%) | 29 (19,9%) | 0,119 |
| Troponina elevada | 179 (89,9%) | 118 (84,3%) | |
| Casos atendidos en centros con Unidad de Hemodinámica | 81 (36,8%) | 38 (26%) | 0,031 |
| Riesgo basal | |||
| Isquémico (GRACE) | 0,051 | ||
| <108 | 56 (27,2%) | 25 (18,4%) | |
| 109-140 | 77 (37,4%) | 52 (38,2%) | |
| >140 | 73 (35,4%) | 59 (43,4%) | |
| TIMI score | 0,229 | ||
| 0-3 | 176 (80%) | 109 (74,7%) | |
| 4-7 | 44 (20%) | 37 (25,3%) | |
| Factores riesgo hemorrágico | 0,007 | ||
| 1 | 62 (28,2%) | 26 (17,8%) | |
| 2 | 67 (30,5%) | 43 (29,5%) | |
| 3 | 48 (21,8%) | 37 (25,3%) | |
| 4 | 38 (17,3%) | 31(21,2%) | |
| 5 | 5 (2,3%) | 9 (6,2%) | |
AAS: ácido acetilsalicílico; Ant. familiares: antecedentes familiares; ARA II: antagonistas de los receptores de la angiotensina ii; CCV: cirugía cardiovascular; DM: diabetes mellitus; ECG: electrocardiograma; EIP: estrategia invasiva precoz; FA: fibrilación auricular; FC (lpm): frecuencia cardiaca (lat/min); GRACE: Global Registry of Acute Coronary Events; HTA: hipertensión arterial; ICC: insuficiencia cardiaca congestiva; IECAs: inhibidores de la enzima convertidora de angiotensina; IPC: intervencionismo percutáneo coronario; Les. coronarias previas: lesiones coronarias previas; mmHg: milímetros de mercurio; TAD: tensión arterial distólica; TAS: tensión arterial sistólica; TIMI: thrombolysis in myocardial infarction.
Por el contrario, la edad (mayor de 80 años), la presencia de diabetes mellitus, la insuficiencia cardiaca y el alto riesgo isquémico basal (estratificado según el sistema de puntuación GRACE) se asociaron paradójicamente con la estrategia conservadora. La presencia de lesiones coronarias conocidas, la fibrilación auricular, el tratamiento previo con acenocumarol y el riesgo hemorrágico elevado también se asociaron significativamente con la estrategia conservadora (tabla 1).
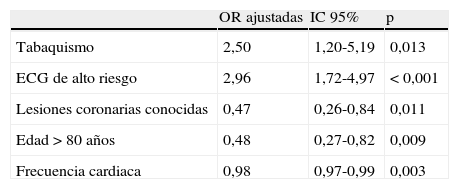
El análisis de regresión logística (tabla 2) identificó como variables predictoras independientes asociadas al uso de una estrategia invasiva el electrocardiograma de alto riesgo (OR ajustada: 2,96; IC 95%: 1,72-4,97; p<0,001) y el tabaquismo (OR ajustada: 2,50; IC 95%: 1,20-5,19; p=0,013). La disponibilidad de la Unidad de Hemodinámica no se asoció de forma independiente a la EIP. De las variables que se asociaron con la estrategia conservadora en el análisis univariante, la edad avanzada (OR ajustada: 0,48; IC 95%: 0,27-0,82; p=0,009), la existencia de lesiones coronarias conocidas (OR ajustada: 0,47; IC 95%: 0,26-0,84, p=0,011) y la frecuencia cardiaca (OR ajustada: 0,98; IC 95%: 0,97-0,99, p=0,003) se confirmaron como variables predictoras independientes asociadas a la estrategia conservadora.
Predictores independientes asociados a la estrategia invasiva precoz
| OR ajustadas | IC 95% | p | |
| Tabaquismo | 2,50 | 1,20-5,19 | 0,013 |
| ECG de alto riesgo | 2,96 | 1,72-4,97 | <0,001 |
| Lesiones coronarias conocidas | 0,47 | 0,26-0,84 | 0,011 |
| Edad >80 años | 0,48 | 0,27-0,82 | 0,009 |
| Frecuencia cardiaca | 0,98 | 0,97-0,99 | 0,003 |
ECG: Electrocardiograma; IC: interval de confianza; OR: odds ratio.
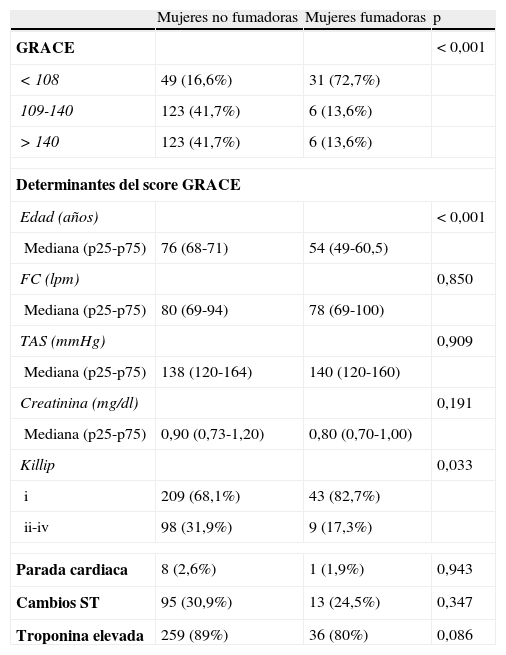
El porcentaje de pacientes fumadoras fue de 12,5% (53 pacientes), de las cuales el 60,4% (32%) eran fumadoras activas. El riesgo isquémico de estas pacientes fue significativamente menor (tabla 3). En el análisis desagregado de los determinantes del score GRACE las pacientes fumadoras se caracterizaron por ser significativamente más jóvenes y presentar menos insuficiencia cardiaca al ingreso (tabla 3).
Características determinantes del riesgo isquémico de los pacientes según antecedente de tabaquismo
| Mujeres no fumadoras | Mujeres fumadoras | p | |
| GRACE | <0,001 | ||
| <108 | 49 (16,6%) | 31 (72,7%) | |
| 109-140 | 123 (41,7%) | 6 (13,6%) | |
| >140 | 123 (41,7%) | 6 (13,6%) | |
| Determinantes del score GRACE | |||
| Edad (años) | <0,001 | ||
| Mediana (p25-p75) | 76 (68-71) | 54 (49-60,5) | |
| FC (lpm) | 0,850 | ||
| Mediana (p25-p75) | 80 (69-94) | 78 (69-100) | |
| TAS (mmHg) | 0,909 | ||
| Mediana (p25-p75) | 138 (120-164) | 140 (120-160) | |
| Creatinina (mg/dl) | 0,191 | ||
| Mediana (p25-p75) | 0,90 (0,73-1,20) | 0,80 (0,70-1,00) | |
| Killip | 0,033 | ||
| i | 209 (68,1%) | 43 (82,7%) | |
| ii-iv | 98 (31,9%) | 9 (17,3%) | |
| Parada cardiaca | 8 (2,6%) | 1 (1,9%) | 0,943 |
| Cambios ST | 95 (30,9%) | 13 (24,5%) | 0,347 |
| Troponina elevada | 259 (89%) | 36 (80%) | 0,086 |
FC (lpm): frecuencia cardiaca (lat/min); GRACE: Global Registry of Acute Coronary Events; TAS: tensión arterial sistólica.
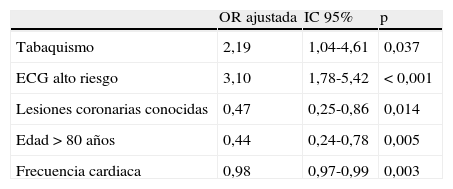
Para confirmar la validez de los resultados se realizó un análisis de sensibilidad consistente en la exclusión del análisis de los pacientes que fallecen en las primeras 24h (10 pacientes, 2,5%). Tras excluir las muertes precoces del análisis, el análisis multivariante tuvo resultados similares (tabla 4).
Predictores independientes asociados a la estrategia invasiva precoz tras la exclusión de muertes precoces
| OR ajustada | IC 95% | p | |
| Tabaquismo | 2,19 | 1,04-4,61 | 0,037 |
| ECG alto riesgo | 3,10 | 1,78-5,42 | <0,001 |
| Lesiones coronarias conocidas | 0,47 | 0,25-0,86 | 0,014 |
| Edad >80 años | 0,44 | 0,24-0,78 | 0,005 |
| Frecuencia cardiaca | 0,98 | 0,97-0,99 | 0,003 |
ECG: electrocardiograma; IC: intervalo de confianza; OR: odds ratio.
En el presente estudio el grupo de mujeres tratadas con una EIP fueron significativamente más jóvenes, con menor riesgo isquémico y hemorrágico, con mayor porcentaje de pacientes fumadoras, con cambios electrocardiográficos de alto riesgo y atendidas en centros con disponibilidad de realizar estudios hemodinámicos.
Por el contrario, el grupo de pacientes tratadas de forma conservadora se caracterizó por una mayor edad, mayor porcentaje de pacientes diabéticas, tratadas crónicamente con dicumarínicos y mayor gravedad al ingreso (mayor prevalencia de insuficiencia cardiaca, mayor riesgo isquémico basal), confirmando la relación inversa entre el riesgo isquémico y la realización de la estrategia invasiva ya descrita en la población general22,24. No se encontraron diferencias significativas en cuanto a comorbilidad (EPOC, obesidad, insuficiencia renal crónica). El subgrupo tratado de forma conservadora presentaba también mayor riesgo hemorrágico, lo que apoyaría la asociación dosis-respuesta entre riesgo hemorrágico y uso de la EIP que constituye un importante hallazgo de recientes estudios22 y sugiere que la menor utilización de una EIP en los pacientes de alto riesgo puede deberse al mayor riesgo hemorrágico de estos pacientes.
El análisis multivariante muestra que la probabilidad de recibir una EIP aumenta en el subgrupo de pacientes fumadoras y con cambios electrocardiográficos indicadores de lesiones graves al ingreso. De estos 2 factores, la relación de los cambios electrocardiográficos de riesgo y la actitud intervencionista no plantea problemas de interpretación y corresponde a la aplicación de las guías vigentes de práctica clínica7–10. El efecto observado del tabaquismo sobre el tipo de estrategia adoptada reproduce los resultados de otros análisis25,26. Este efecto resultó independiente de la edad en el análisis de regresión, lo que sugiere un efecto específico de este factor de riesgo sobre el tratamiento y la evolución de los SCA. De hecho, se ha descrito un efecto paradójico consistente con mejor pronóstico en los pacientes fumadores con IAM y angina inestable e IAM que no se explica únicamente por covariables clínicas como la edad, el sexo o el tratamiento recibido25,26. En el estudio de Poon et al.11 la infraestimación del riesgo isquémico real de las pacientes fue el motivo más común para adoptar una estrategia conservadora. Una posible hipótesis que explicaría nuestros resultados sería la sobreestimación del riesgo de estas pacientes. No podemos excluir la posibilidad de que otros factores, como una menor percepción del riesgo hemorrágico de estas pacientes, influyan en la decisión sobre el tipo de estrategia a adoptar.
Respecto a los factores asociados de modo independiente a la estrategia conservadora, la existencia de lesiones coronarias conocidas previamente puede sugerir tanto la existencia de lesiones no revascularizables ya conocidas como la ausencia de las mismas. El 87% de las pacientes (n=23) con lesiones coronarias previas habían sido sometidas a cateterismo con anterioridad, de las cuales el 52% (12/23) tenían antecedentes de intervencionismo coronario y 12% (3/23) de revascularización quirúrgica. Una limitación de este estudio es la ausencia de datos en el registro para explorar las características de estas lesiones ya que un factor de riesgo conocido es la IPC previa. La edad avanzada (>80 años) fue también una variable predictora asociada a la estrategia conservadora, coincidiendo así con otros estudios que indican que el binomio género femenino/edad avanzada disminuye el uso de la revascularización en el SCASEST11. La mayor frecuencia cardiaca al ingreso también se asoció de modo independiente con la estrategia conservadora. Este dato coincide con análisis similares11. La relación entre el incremento de la frecuencia cardiaca y la mortalidad cardiovascular es bien conocida. El aumento de la frecuencia cardiaca es un dato predictivo de mayor mortalidad a corto y largo plazo en pacientes con SCA27 y también se interpreta como dato del uso contradictorio de la estrategia conservadora en los pacientes más graves24. En estudios recientes la infraestimación del riesgo isquémico real de las pacientes fue el motivo más común para adoptar una estrategia conservadora11. Este es un dato relevante que sugiere la necesidad de replantear una correcta valoración del riesgo y el beneficio en la toma de decisiones sobre el diagnóstico y el tratamiento precoz de los SCASEST en mujeres, teniendo en cuenta además que los riesgos de la EIP se basan en datos probablemente obsoletos y que no están directamente en relación con la técnica percutánea14,15.
Un aspecto considerado en el análisis fue la posibilidad de que los pacientes más graves, que fallecen pocas horas tras el ingreso sin tiempo a realizar la coronariografía, estuvieran influyendo en el resultado al ser analizados en el mismo grupo que las pacientes tratadas de forma conservadora. Sin embargo, los resultados fueron similares tras la exclusión de las pacientes fallecidas en las primeras 24h (tabla 3).
La validez de estos resultados debe ser tomada con cautela ya que proceden de un registro observacional de cohortes cuya principal limitación es su vulnerabilidad al efecto de los factores de confusión11,25. Otra limitación está en un posible sesgo de selección en los pacientes ya que solo se estudian los pacientes que ingresan en las unidades coronarias que voluntariamente participan en el proyecto ARIAM-SEMICYUC. Una tercera limitación del análisis de este tipo de registros podría deberse a que el uso sistemático de las escalas de valoración de riesgo y sus diferentes puntos de corte pueden no ser herramientas utilizadas en la clínica habitual, sino datos cumplimentados a posteriori en el registro. Sin embargo, sí son de uso clínico habitual los determinantes individuales que constituyen dichas escalas.
Como conclusión, en este estudio el tabaquismo y el electrocardiograma de alto riesgo al ingreso identifican un subgrupo de mujeres con SCASEST con mayor probabilidad de ser sometidas a intervencionismo precoz de modo independiente. La existencia de lesiones coronarias previas, la edad avanzada y el incremento de la frecuencia cardiaca son factores independientes para el tratamiento conservador. Serían necesarias nuevas herramientas de análisis de decisiones respecto al intervencionismo coronario en la población femenina.
FinanciaciónEl registro ARIAM es un proyecto financiado por la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Andalucía: Hospital Nuestra Señora de Valme (Sevilla): Dolores Herrera Rojas, Ana Loza Vázquez, Antonio Campanario García, José Antonio Sánchez Román, María Marín Herrero y Alejandro Úbeda Iglesias. Andorra: Hospital de Nuestra Señora de Meritxell (Andorra la Vella): Antonio Margarit Ribas. Aragón: Hospital General San Jorge (Huesca): Juan Carlos López Claver, Lorenzo Labarta Monzón, Jesús Escos Orta, Aránzazu Lander Azcona, Carlos Serón Arbeloa, Isabel Garrido Ramírez de Arellano y María Isabel Marquina Lacueva; Hospital Clínico Universitario Lozano Blesa (Zaragoza): Emilia Civeira Murillo, Luis Mariano Giner Smith y Luis Martín Villén; Hospital Maz (Zaragoza): Isabel Yuste Serrano, Pedro Bernad, Santiago Temiño, Victoria Rull, Raquel Valero y Noelia Artesero; Hospital Universitario Miguel Servet (Zaragoza): Joaquín Joven Lafont, José Luis Ibáñez Langa, Alejandra Morón, Jose Luis Ibañez Langa, Javier Muñoz Marco, Jesús Lorente Cortés, Teresa Sanz, Agustín Nebra, Antonio Luis Ruiz, Ignacio González y Antonio Luis Aguilar. Comunidad Foral de Navarra: Hospital Virgen del Camino (Pamplona/Iruña): José Ramos Castro. Castilla y León: Complejo Asistencial de Palencia (Palencia): Jose I. Alonso Fernández, Houssein Bouchotrouch y Maite Ortega Sáez; Hospital El Bierzo (Ponferrada): Julián J. Sandoval Garzón; Hospital General de Segovia (Segovia): Pablo Ancillo García y Antonio José Montón Rodríguez; Hospital General Yagüe (Burgos): Oliverio López Gimeno; Hospital Santa Bárbara (Soria): Christian J. Salas; Hospital Felipe II (Valladolid): Juan José Sanz Hernán; Hospital Universitario del Río Hortega (Valladolid): Marta García García, Ana María Prieto y Rubén Herrán Monge; Hospital Virgen de la Concha (Zamora): Ana carolina Caballero Zirena. Castilla-La Mancha: Hospital General de Ciudad Real (Ciudad Real): Carmen Martín Rodríguez, Mariana Portilla Botelho y Alfonso Ambros Checa; Hospital Universitario de Guadalajara (Guadalajara): Elena Yáñez Parareda; Hospital Santa Bárbara (Puertollano): Francisca Prieto Valderrey y Emilio Moreno Millán. Catalunya: Hospital General de L’Hospitalet (L’Hospitalet de Llobregat): José Julián Berrade Zubiri; Hospital de Sabadell (Sabadell): Consuelo Guía Rambla y Xaime García Nogales; Hospital de Sant Boi (Sant Boi de Llobregat): Alejandra Fernández Trujillo; Hospital General de Catalunya (Sant Cugat del Vallès): Elisabet Manero Caballero y Rocío Toledo; Hospital de Terrassa (Terrassa): Joaquín Amador Amerigo; Hospital de Sant Pau y Santa Tecla (Tarragona): Yolanda del Castillo; Hospital de Sant Joan de Déu (Manresa): Josep M. Alcoverro Pedrola. Comunidad Valenciana: Hospital General Universitario de Alicante (Alicante): José Cánovas Robles, Mónica Díaz Barranco, Victoria Ortolá Vercher y Francisco Ángel Jaime Sánchez; Hospital Universitario de la Ribera (Alzira): Lucia Arias Portaceli, Ana Abalos García, Martín Parejo Montell y Juan Fernández Cabrera; Hospital General de Castelló (Castellón de la Plana): Laura Albert Rodrigo, Patricia Casero Roig, Susana Altaba Tena y Amparo Ferrándiz; Consorcio Hospitalario Provincial de Castellón (Castellón): Javier Madero; Hospital de la Plana (Vila-Real): Elena Porcar Rodado; Hospital de Villajoyosa (Villajoyosa): Pedro Manzano Hinojosa; Hospital General de Elche (Elche): Jaime Latour Pérez, Eva de Miguel Balsa, Karel Pino Izquierdo y Francisco Javier Coves Orts; Hospital Torrevieja Salud UTE (Torrevieja): Eugenio Herrrero Gutiérrez; Hospital Dr. Peset Aleixandre (Valencia): Luis García Ochando y Luisa F. Martín Osorio; Hospital de Manises (Manises): Mónica Talavera Peregrina y Concha Cortés Navalón; Hospital Vega Baja (Orihuela): Cristina Portillo Requena y Fadoua Laghzaoui; Hospital de Requena (Valencia): Carlos José Folgado Bisbal; Hospital de Sagunto (Sagunto): Regina Calvo Embuena; Hospital del Vinalopó (Elche): David Martín Langerwerf; Hospital Universitario de San Juan de Alicante (San Juan de Alicante): Cristina Molla Jiménez; Clínica Quirón de Valencia (Valencia): Javier Tornero López; Hospital Arnau de Vilanova (Valencia): Moisés Rico Sala, Mercedes García Sanz y Eugenia de la Fuente O’Connor; Hospital Clínico Universitario (Valencia): Ricardo Oltra Chordá; Hospital Universitario La Fe (Valencia): María Paz Fuset Cabanes, Isabel Madrid López, Karla Vacacela Cordova y Esther Villarreal Tello; Hospital de Vinaros (Vinaròs): María Desamparados Oliva Gimeno. Extremadura: Hospital San Pedro de Alcántara (Cáceres): Eduardo Corchero, Elena Gallego Curto, Alberto Fernández Zapata y Abilio Arrasqueta Llanes; Hospital Don Benito (Villanueva de la Serena): Juan Diego Jiménez Delgado; Hospital de Mérida (Mérida): Marcelo Pérez Arriaga, Fernando Vázquez Fuentes, Mercedes Antona Díez y Guadalupe Borge Rodríguez; Hospital Virgen del Puerto (Plasencia): Eva Guerra Nevado y Anton Arana Llanderal; Hospital de Zafra (Zafra): Miguel González Lar e Hilario Badiola Villa. Galicia: Hospital Xeral de Lugo (Lugo): María Luisa Martínez Rodríguez y Rebeca Álvarez-Lata; Complejo Hospitalario de Ourense (Ourense): María José de la Torre y Román Rodríguez Álvarez-Granada; Hospital Miguel Domínguez (Pontevedra): Raúl José González González; Hospital Arquitecto Marcide (Ferrol): Carmen J. Fernández González. La Rioja: Hospital San Pedro (Logroño): María de la Concepción Pavía Pesquera, Verónica Díaz de Antoñana y Lidia Martínez Camarero. Madrid: Hospital Universitario Príncipe de Asturias (Alcalá Henares): José Andrés Cambronero Galache y Cristina Martínez; Hospital del Henares (Coslada): Inés Torrejón Pérez; Hospital de Fuenlabrada (Fuenlabrada): Mercedes Rubio Regidor, Marialving Fuentes Salazar y Febechi Afamefule Afamefule; Hospital Severo Ochoa (Leganés): Frutos del Nogal Sáez; Hospital La Moraleja (Madrid): Miguel Ángel Palma Gamiz; Hospital del Tajo (Aranjuez): Miriam Chana García; Hospital Infanta Leonor (Madrid): Paloma Rico Cepeda. País Vasco: Hospital de Cruces (Barakaldo): Katherine García Castillo y Victoria Boado Varela. Principado de Asturias: Hospital San Agustín (Avilés): Josefa Rengel Jiménez. Murcia: Hospital Rafael Méndez (Lorca): Carlos Luis Albacete Moreno; Hospital General Universitario Reina Sofía (Murcia): Francisco Felices Abad, Isabel Cremades Navalón, Lisa Ortín Katnich, Fátima Martínez-Lozano Aranaga, José L. Espinosa Berenguel, Blanca Gallego Pérez y Martín Vigil Velis.