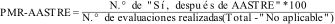Desde el punto de vista de la seguridad, la pandemia impuso dinámicas de trabajo atípicas que provocaron visibles brechas en la seguridad clínica en todos los niveles de la atención sanitaria.
ObjetivosComprobar que los Análisis Aleatorios de Seguridad en Tiempo Real (AASTRE) son factibles y útiles en un escenario de elevada presión asistencial.
DiseñoEstudio prospectivo (enero a septiembre de 2022).
ÁmbitoHospital universitario con 350 camas. Dos UCI polivalentes (12 y 14 camas).
IntervencionesSe planificaron dos auditorías de seguridad a la semana para determinar la factibilidad y la utilidad de las 32 medidas de seguridad.
Variables de interés principales1) Factibilidad: proporción de auditorías completadas respecto a las programadas y el tiempo empleado. 2)Utilidad: cambios en el proceso de atención realizados como resultado de la aplicación de AASTRE.
ResultadosSe analizaron un total de 390 pacientes día (179 fueron pacientes no-COVID y 49 COVID). En los pacientes COVID la edad, el SAPS-3, la estancia y la mortalidad en la UCI fueron significativamente mayores respecto a los pacientes no-COVID. En cuanto a la factibilidad, el 93,8% de las rondas planificadas fueron realizas con un tiempo promedio empleado por auditoría de 25±8minutos. Globalmente se produjeron cambios en el proceso de atención en el 11,8% de las medidas analizadas.
ConclusionesAASTRE, en un ambiente de elevada complejidad asistencial, resultó ser una herramienta factible y útil, con solo dos intervenciones semanales de menos de 30minutos. Globalmente, AASTRE permitió revertir situaciones inseguras a seguras en más del 10% de las evaluaciones.
From a safety perspective, the pandemic imposed atypical work dynamics that led to noticeable gaps in clinical safety across all levels of health care.
ObjectivesTo verify that Real-Time Random Safety Analyses (AASTRE) are feasible and useful in a high-pressure care setting.
DesignProspective study (January to September 2022).
SettingUniversity hospital with 350 beds. Two mixed ICUs (12 and 14 beds).
InterventionsTwo safety audits per week were planned to determine the feasibility and usefulness of the 32 safety measures (grouped into 8 blocks).
Main variables of interest1) Feasibility: Proportion of completed audits compared to scheduled audits and time spent. 2)Utility: Changes in the care process made as a result of implementing AASTRE.
ResultsA total of 390 patient-days were analyzed (179 were non-COVID patients and 49 were COVID patients). In the COVID patient subgroup, age, ICU stay, SAPS-3, and ICU mortality were significantly higher compared to the non-COVID patient subgroup. Regarding feasibility, 93.8% of planned rounds were carried out with an average audit time of 25±8minutes. Overall, changes in the care process were made in 11.8% of the measures analyzed.
ConclusionsIn a high-complexity care environment, AASTRE proved to be a feasible and useful tool with only two interventions per week lasting less than 30minutes. Overall, AASTRE allowed unsafe situations to be turned safe in more than 10% of the evaluations.
Todavía reciente, es fácil recordar la tensión ejercida por la pandemia (virus SARS-CoV-2) sobre el sistema sanitario1. Mucho antes, en Medicina Intensiva, ya era conocida una fuerte asociación entre la elevada presión asistencial y la falta de adherencia a las guías de práctica clínica y, secundariamente, a un empeoramiento del pronóstico, incluida una mayor mortalidad2-4.
Desde el punto de vista de la seguridad, la pandemia impuso dinámicas de trabajo atípicas que provocaron brechas en la seguridad clínica en todos los niveles de la atención sanitaria5. Concretamente, se describieron alteraciones significativas en la percepción de la cultura de seguridad asociadas a déficits estructurales, de liderazgo y de comunicación6. Otros autores pusieron de manifiesto ineficiencias en el sistema por la falta de estandarización de los procesos7.
En la UCI, los incidentes relacionados con la seguridad del paciente (IRSP) durante la pandemia se tradujeron en un incremento de las bacteriemias primarias8, bacteriemias asociadas a catéteres venosos centrales9, neumonías asociadas a la ventilación mecánica, infecciones urinarias asociadas a la presencia de sonda vesical, insuficiencia renal y eventos tromboembólicos y vasculares, todos ellos asociados a una mayor mortalidad10,11. Asociado a estos IRSP, los profesionales se vieron aún más tensionados al verse obligados a adaptarse a nuevos estándares de seguridad12. Paralelamente, durante este periodo los sistemas de notificación de IRSP fueron infrautilizados13-15.
Nuestro grupo ha desarrollado una herramienta proactiva de seguridad denominada Análisis Aleatorios de Seguridad en Tiempo Real (AASTRE) que se ha asociado con una mejora en los indicadores de calidad de estructura, proceso y resultado. AASTRE ha demostrado ser más útil en situaciones de elevada carga asistencial y en pacientes más graves16,17. Esta herramienta se fundamenta en un grupo de medidas, basadas en la evidencia científica, que se consideran de obligado cumplimiento durante la actividad asistencial en la UCI. La aleatorización hace referencia a que no es posible conocer, con anterioridad a las rondas de seguridad, ni las medidas ni los pacientes auditados, porque ambos son aleatorizados el día de la auditoría.
Enfatizando en la idea de la importancia de la seguridad clínica y teniendo en cuenta la paradoja del abandono de la misma durante la pandemia, los objetivos de este estudio son: 1)Describir la adaptación de AASTRE a la dinámica de trabajo de la pandemia. 2)Comprobar que AASTRE es factible y útil en un escenario real de pandemia. 3)Construcción de una plataforma web que haga visible los resultados de forma sencilla, continua e intuitiva para el clínico.
Material y métodosDiseñoEstudio prospectivo desarrollado en un hospital universitario con 350 camas y dos UCI polivalentes (12 y 14 camas). Durante el periodo de estudio en ambas unidades se atendieron indistintamente pacientes COVID y no-COVID. La UCI dispone de un sistema de información clínica (SIC) donde se almacenan los datos provenientes de los dispositivos de cabecera del paciente, la información generada en otros departamentos y la generada/registrada por los propios profesionales durante la atención al paciente, y de donde se han extraído los datos para el análisis en el presente estudio.
Periodo de intervenciónEntre enero de 2022 y septiembre de 2022, coincidiendo con la sexta y última ola de la pandemia.
Descripción de AASTREAASTRE es una herramienta proactiva de seguridad ya validada18,19 que permite detectar situaciones inseguras y convertirlas en seguras en tiempo real; en su versión220,21 verifica 32 medidas de seguridad obligatorias, distribuidas en ocho bloques: 1)ventilación mecánica; 2)hemodinámica; 3)función renal y técnicas de reemplazo renal continuo; 4)analgesia y sedación; 5)tratamiento; 6)nutrición; 7)cuidado de enfermería y estructura, y 8)sistema de información clínica. Cada medida de seguridad tiene una definición específica, criterios de evaluación y una metodología específica para su verificación. AASTRE se planificó 2 veces por semana en cada unidad durante un total de 9meses. En los días de evaluación se seleccionó aleatoriamente el 30% de los pacientes en la UCI y el 50% de los bloques de medidas de seguridad. Todos los pacientes ingresados en la UCI son elegibles para que se les realice AASTRE. Sin embargo, solo se evaluarán aquellas medidas para las cuales cumplan con los criterios de evaluación, en el caso de cada paciente seleccionado. Las posibles respuestas durante las auditorías son: 1)«Sí», cuando la medida analizada se ha realizado/tomado en la ronda diaria de la UCI; 2)«Sí, después de AASTRE», cuando la auditoría de seguridad se utilizó para detectar un error de omisión que ha sido corregido; 3)«No», cuando la medida analizada no se pudo cambiar a pesar de la auditoría, y 4)«No aplicable», cuando el paciente no cumple con los criterios de evaluación. La lista de verificación y las respuestas de las evaluaciones se ingresan en una plataforma web (https://v2.aastre.es/web/index.php). Un profesional sénior (prompter) que no fue directamente responsable del cuidado de ninguno de los pacientes seleccionados en el día de la evaluación llevó a cabo el AASTRE a pie de cama y mediante un dispositivo móvil (tableta) junto con la enfermera y médico (adjunto o residente) responsable, actuando como facilitador y proporcionando retroalimentación a los profesionales durante el intercambio. Se consideró la proporción de cambios en el proceso de atención realizados como resultado de la verificación.
Definición de variables e indicadores- 1.
Número de pacientes-día. Número de pacientes evaluados en el total de días en que se llevaron a cabo auditorías de seguridad.
- 2.
Factibilidad. Número de pacientes en que se completó AASTRE en relación con los programados y tiempo promedio de evaluación.
- 3.
Utilidad. Proporción de cambios en el proceso de atención realizados como resultado de la verificación. En particular, para cada medida de seguridad se definió una variable cuantitativa para analizarla (proporción de mejora relacionada con AASTRE [PMR-AASTRE]). PMR-AASTRE queda definido como un indicador de proceso de tal modo que puede existir un PMR-AASTRE para cada medida, para cada bloque de medidas (PMR-AASTRE-B), o global, para todo el conjunto de medidas (PMR-AASTRE-G). Su cálculo se realizó según la siguiente fórmula:
Un PMR-AASTRE ≥ 10% fue considerado clínicamente relevante17,20.
- 4.
Indicadores de resultado. Mortalidad en UCI, estancia promedio y las tasas de bacteriemia relacionada con catéter venoso central (BRC), neumonía asociada a ventilación mecánica (NAVM), traqueobronquitis asociadas a la ventilación mecánica (TBAVM), infecciones urinarias asociadas al sondaje urinario (IUASU), autorretiradas del tubo endotraqueal (TET), reintubaciones o barotrauma utilizando definiciones de indicadores y métricas ya publicadas en trabajos previos21,22.
- 5.
Análisis multivariado. Se realizó una selección de variables para determinar su impacto de forma independiente con un PMR-AASTRE-G significativo. Estas variables fueron: demográficas (sexo, edad, tipo de paciente y de ingreso), de gravedad (SOFA, APACHE-II, SAPS-3), de carga asistencial (ratio enfermería y médico-paciente además del Nursing Activities Score [NAS]) y las derivadas de la propia patología, gravedad y soporte vital durante su ingreso (COVID, días de estancia y de ventilación mecánica, escala RASS, presencia de shock o necesidad de técnicas continuas de reemplazo renal y el riesgo nutricional).
Los datos demográficos y las variables necesarias para evaluar las medidas de proceso de atención y los indicadores de calidad se extrajeron del SIC, utilizando un proceso de extracción, transformación y carga previamente definido21-23.
Análisis estadísticoPara describir las características basales, las variables continuas se expresaron como mediana (rango de Q1-Q3) y las variables categóricas como número de casos (porcentaje).
Para las características demográficas de los pacientes, las características clínicas, las medidas de proceso de atención y los indicadores de calidad se evaluaron las diferencias entre los grupos utilizando la prueba de chi-cuadrado y la prueba exacta de Fisher para variables categóricas, y la prueba U de Mann-Whitney o la prueba de Wilcoxon para variables continuas. Se realiza mediante Python y el módulo Tableone, donde se aplica el test chi-cuadrado para cada variable.
Se llevó a cabo un análisis multivariado para determinar la relación entre las variables independientes seleccionadas y un PMR-AASTRE-G ≥10%. Con el objetivo de ajustar posibles efectos de confusión, se realizaron análisis de regresión logística múltiple, modelo fijo y método de razón de verosimilitud para posibles efectos de confusión. Los resultados se expresaron como odds ratio y su intervalo de confianza del 95%. El nivel aceptable de significación estadística se estableció en <0,05. El análisis de datos se realizó utilizando el software R (cran.r-project.org).
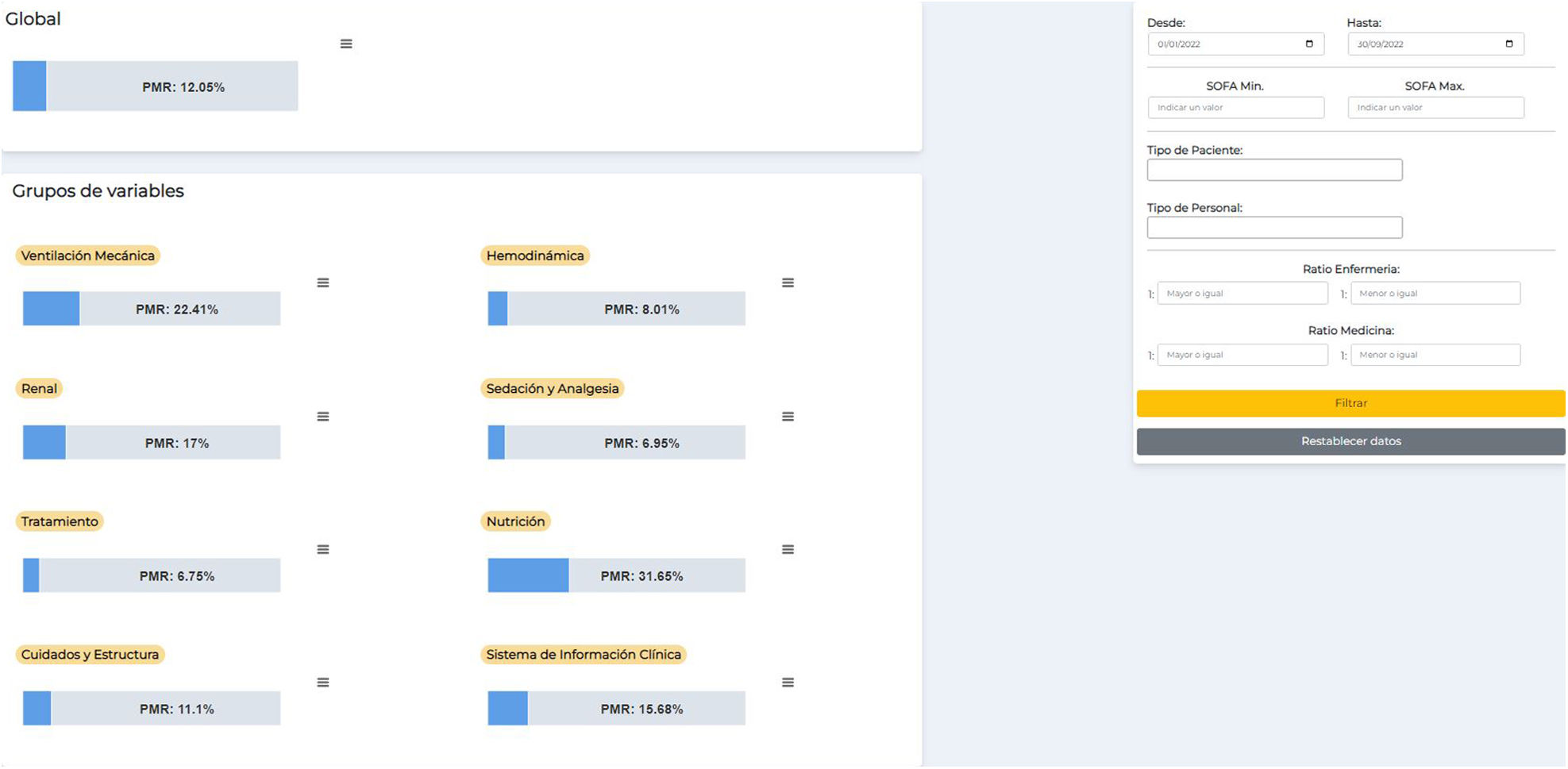
Construcción e implementación de la plataforma de indicadores de procesoPara un uso más eficiente, automatizado y en tiempo real de los datos obtenidos a través de la realización de rondas de seguridad AASTRE se crea una aplicación web desarrollada con software libre (Python, Django, HTML, CSS, Java Script) para acceso a los resultados de AASTRE en forma de gráficas que nos permite filtrar por fecha, SOFA, tipo de paciente, tipo de personal, ratio de enfermería/pacientes y ratio de médico/pacientes, además de poder seleccionar el PMR-AASTRE, ya sea el de cada variable, el PMR-AASTRE-B o PMR-AASTRE-G (fig. 1).
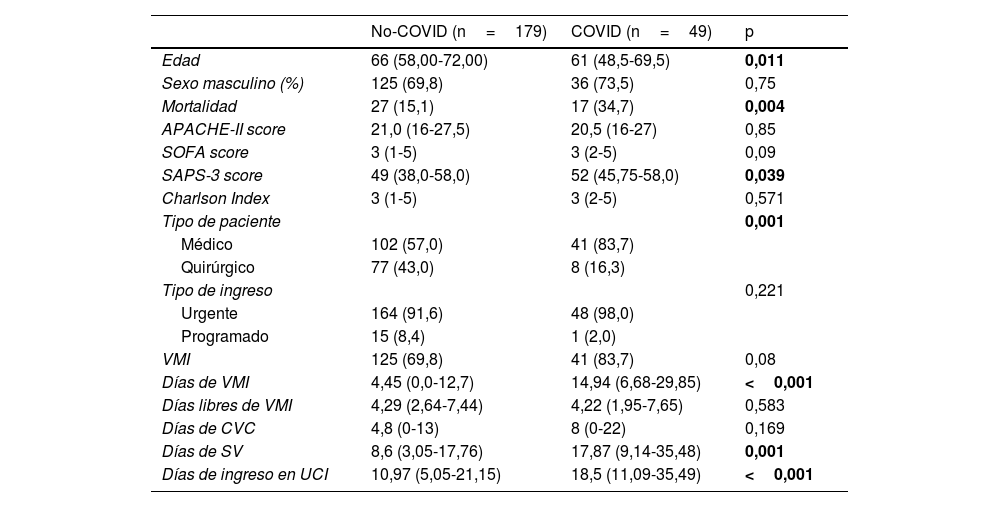
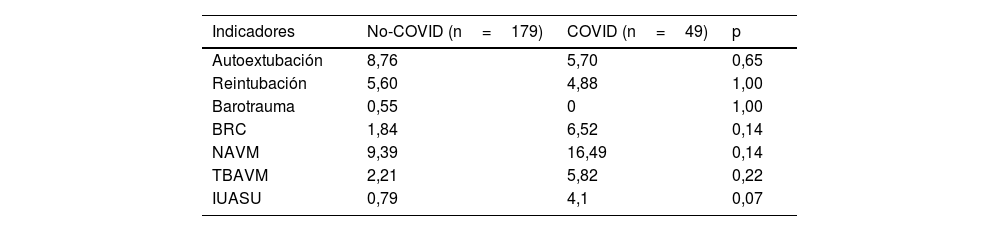
ResultadosDurante el periodo de estudio se analizaron un total de 390 pacientes día, de los cuales 179 fueron pacientes no-COVID y 49 pacientes COVID (tabla 1). Los pacientes COVID fueron significativamente más jóvenes (61 vs 66años; p=0,011) respecto a los pacientes no-COVID. Por su parte, los pacientes COVID tuvieron unos días de estancia, un SAPS-3 y una mortalidad en UCI significativamente mayor respecto a los pacientes no-COVID (18,5 vs 10,97 días; p<0,001; 52 vs 49; p=0,039), y 34,7% vs 15,2%; p=0,004, respectivamente). Además, en los pacientes COVID los días de ventilación mecánica y los días de sonda vesical fueron significativamente más elevados respecto a los pacientes no-COVID (14,94 vs 4,45 días; p<0,001; 17,87 vs 8,6 días; p=0,001, respectivamente). No se encontraron diferencias significativas entre ambos grupos en los indicadores de resultado considerados (tabla 2).
Características de la población (p<0,05)
| No-COVID (n=179) | COVID (n=49) | p | |
|---|---|---|---|
| Edad | 66 (58,00-72,00) | 61 (48,5-69,5) | 0,011 |
| Sexo masculino (%) | 125 (69,8) | 36 (73,5) | 0,75 |
| Mortalidad | 27 (15,1) | 17 (34,7) | 0,004 |
| APACHE-II score | 21,0 (16-27,5) | 20,5 (16-27) | 0,85 |
| SOFA score | 3 (1-5) | 3 (2-5) | 0,09 |
| SAPS-3 score | 49 (38,0-58,0) | 52 (45,75-58,0) | 0,039 |
| Charlson Index | 3 (1-5) | 3 (2-5) | 0,571 |
| Tipo de paciente | 0,001 | ||
| Médico | 102 (57,0) | 41 (83,7) | |
| Quirúrgico | 77 (43,0) | 8 (16,3) | |
| Tipo de ingreso | 0,221 | ||
| Urgente | 164 (91,6) | 48 (98,0) | |
| Programado | 15 (8,4) | 1 (2,0) | |
| VMI | 125 (69,8) | 41 (83,7) | 0,08 |
| Días de VMI | 4,45 (0,0-12,7) | 14,94 (6,68-29,85) | <0,001 |
| Días libres de VMI | 4,29 (2,64-7,44) | 4,22 (1,95-7,65) | 0,583 |
| Días de CVC | 4,8 (0-13) | 8 (0-22) | 0,169 |
| Días de SV | 8,6 (3,05-17,76) | 17,87 (9,14-35,48) | 0,001 |
| Días de ingreso en UCI | 10,97 (5,05-21,15) | 18,5 (11,09-35,49) | <0,001 |
APACHE-II: Acute Physiology and Chronic Health disease Classification System II at admission; COVID: COronaVIrus Disease; CVC: catéter venoso central; SAPS-3: Simplified Acute Physiology Score III at admission; SOFA: Sepsis-related Organ Failure Assessment in the first 24 hours; SV: sonda vesical; UCI: unidad de cuidados intensivos; VMI: ventilación mecánica invasiva.
En negrita se muestran los valores significativos, p<0,05.
Indicadores de resultado
| Indicadores | No-COVID (n=179) | COVID (n=49) | p |
|---|---|---|---|
| Autoextubación | 8,76 | 5,70 | 0,65 |
| Reintubación | 5,60 | 4,88 | 1,00 |
| Barotrauma | 0,55 | 0 | 1,00 |
| BRC | 1,84 | 6,52 | 0,14 |
| NAVM | 9,39 | 16,49 | 0,14 |
| TBAVM | 2,21 | 5,82 | 0,22 |
| IUASU | 0,79 | 4,1 | 0,07 |
BRC: bacteriemias relacionas con catéteres; COVID: COronaVIrus Disease; IUASU: infecciones urinarias asociadas a sondaje urinario; NAVM: neumonía asociada a la ventilación mecánica; TBAVM. traqueobronquitis asociada a la ventilación mecánica.
Las auditorías se realizaron en el 93,8% de los pacientes en que fueron planificadas. En el 6,2% de las ocasiones en que no se pudieron llevar a cabo, las razones más frecuentes fueron: falta de tiempo del prompter y por ausencia del paciente en la UCI en el momento de la auditoría (quirófano, prueba de imagen). La mediana del tiempo empleado en las auditorías fue de 25±8minutos.
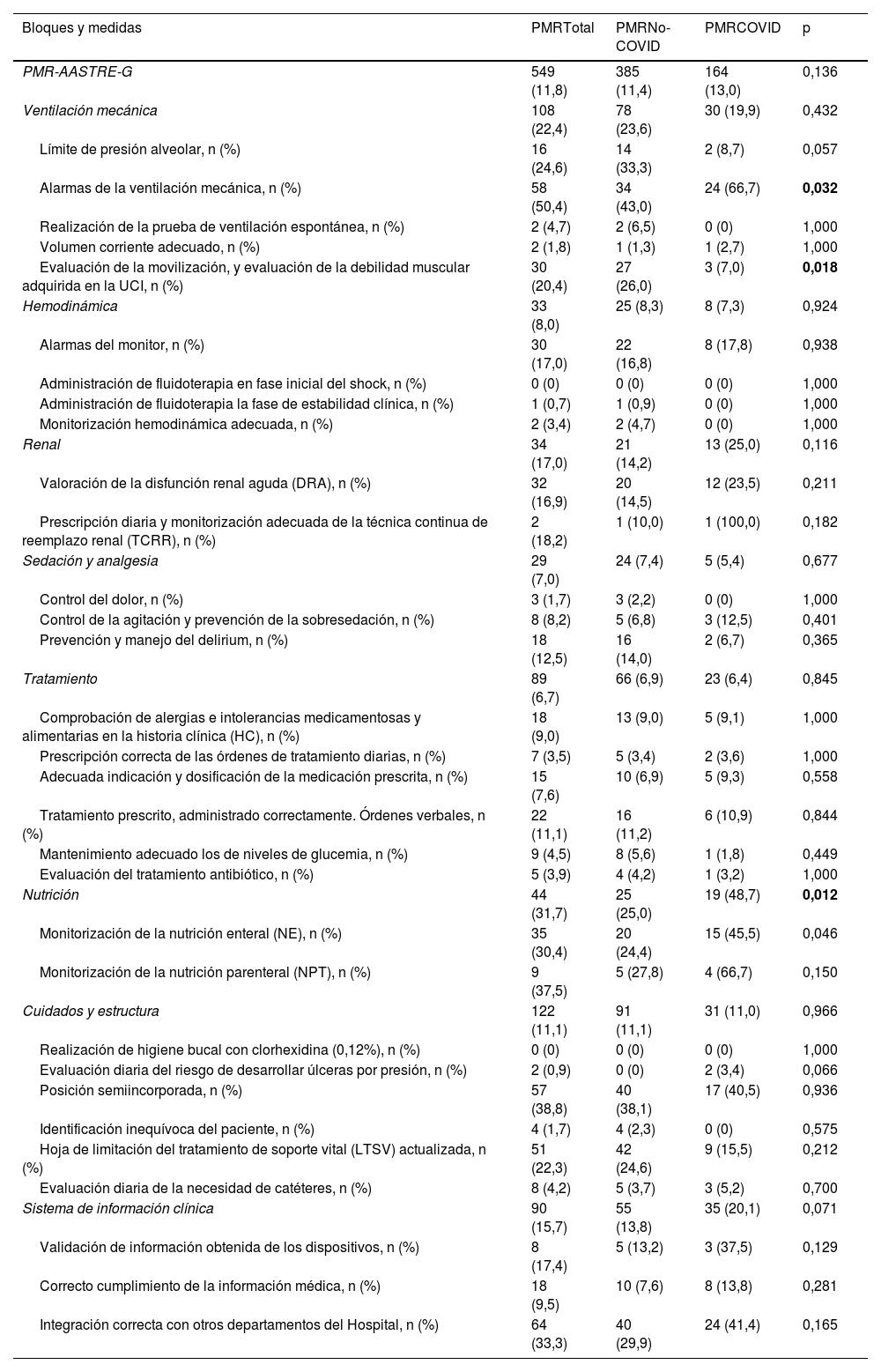
Utilidad (tabla 3)El PMR-AASTRE-G fue del 11,8%. No se objetivaron diferencias significativas del PMR-AASTRE-G entre pacientes COVID y no-COVID. Se observó un PMR-AASTRE-B ≥10% en los mismos bloques de medidas en ambos subgrupos (5 de los 8 bloques). Comparando ambos subgrupos de pacientes, solo el bloque de nutrición mostró diferencias significativas, siendo el PMR-AASTRE-B significativamente mayor en los pacientes COVID (48,7% vs 25,0%; p=0,012).
Resultados de PMR-AASTRE por medidas de obligado cumplimiento según la evidencia científica (p>0,05)
| Bloques y medidas | PMRTotal | PMRNo-COVID | PMRCOVID | p |
|---|---|---|---|---|
| PMR-AASTRE-G | 549 (11,8) | 385 (11,4) | 164 (13,0) | 0,136 |
| Ventilación mecánica | 108 (22,4) | 78 (23,6) | 30 (19,9) | 0,432 |
| Límite de presión alveolar, n (%) | 16 (24,6) | 14 (33,3) | 2 (8,7) | 0,057 |
| Alarmas de la ventilación mecánica, n (%) | 58 (50,4) | 34 (43,0) | 24 (66,7) | 0,032 |
| Realización de la prueba de ventilación espontánea, n (%) | 2 (4,7) | 2 (6,5) | 0 (0) | 1,000 |
| Volumen corriente adecuado, n (%) | 2 (1,8) | 1 (1,3) | 1 (2,7) | 1,000 |
| Evaluación de la movilización, y evaluación de la debilidad muscular adquirida en la UCI, n (%) | 30 (20,4) | 27 (26,0) | 3 (7,0) | 0,018 |
| Hemodinámica | 33 (8,0) | 25 (8,3) | 8 (7,3) | 0,924 |
| Alarmas del monitor, n (%) | 30 (17,0) | 22 (16,8) | 8 (17,8) | 0,938 |
| Administración de fluidoterapia en fase inicial del shock, n (%) | 0 (0) | 0 (0) | 0 (0) | 1,000 |
| Administración de fluidoterapia la fase de estabilidad clínica, n (%) | 1 (0,7) | 1 (0,9) | 0 (0) | 1,000 |
| Monitorización hemodinámica adecuada, n (%) | 2 (3,4) | 2 (4,7) | 0 (0) | 1,000 |
| Renal | 34 (17,0) | 21 (14,2) | 13 (25,0) | 0,116 |
| Valoración de la disfunción renal aguda (DRA), n (%) | 32 (16,9) | 20 (14,5) | 12 (23,5) | 0,211 |
| Prescripción diaria y monitorización adecuada de la técnica continua de reemplazo renal (TCRR), n (%) | 2 (18,2) | 1 (10,0) | 1 (100,0) | 0,182 |
| Sedación y analgesia | 29 (7,0) | 24 (7,4) | 5 (5,4) | 0,677 |
| Control del dolor, n (%) | 3 (1,7) | 3 (2,2) | 0 (0) | 1,000 |
| Control de la agitación y prevención de la sobresedación, n (%) | 8 (8,2) | 5 (6,8) | 3 (12,5) | 0,401 |
| Prevención y manejo del delirium, n (%) | 18 (12,5) | 16 (14,0) | 2 (6,7) | 0,365 |
| Tratamiento | 89 (6,7) | 66 (6,9) | 23 (6,4) | 0,845 |
| Comprobación de alergias e intolerancias medicamentosas y alimentarias en la historia clínica (HC), n (%) | 18 (9,0) | 13 (9,0) | 5 (9,1) | 1,000 |
| Prescripción correcta de las órdenes de tratamiento diarias, n (%) | 7 (3,5) | 5 (3,4) | 2 (3,6) | 1,000 |
| Adecuada indicación y dosificación de la medicación prescrita, n (%) | 15 (7,6) | 10 (6,9) | 5 (9,3) | 0,558 |
| Tratamiento prescrito, administrado correctamente. Órdenes verbales, n (%) | 22 (11,1) | 16 (11,2) | 6 (10,9) | 0,844 |
| Mantenimiento adecuado los de niveles de glucemia, n (%) | 9 (4,5) | 8 (5,6) | 1 (1,8) | 0,449 |
| Evaluación del tratamiento antibiótico, n (%) | 5 (3,9) | 4 (4,2) | 1 (3,2) | 1,000 |
| Nutrición | 44 (31,7) | 25 (25,0) | 19 (48,7) | 0,012 |
| Monitorización de la nutrición enteral (NE), n (%) | 35 (30,4) | 20 (24,4) | 15 (45,5) | 0,046 |
| Monitorización de la nutrición parenteral (NPT), n (%) | 9 (37,5) | 5 (27,8) | 4 (66,7) | 0,150 |
| Cuidados y estructura | 122 (11,1) | 91 (11,1) | 31 (11,0) | 0,966 |
| Realización de higiene bucal con clorhexidina (0,12%), n (%) | 0 (0) | 0 (0) | 0 (0) | 1,000 |
| Evaluación diaria del riesgo de desarrollar úlceras por presión, n (%) | 2 (0,9) | 0 (0) | 2 (3,4) | 0,066 |
| Posición semiincorporada, n (%) | 57 (38,8) | 40 (38,1) | 17 (40,5) | 0,936 |
| Identificación inequívoca del paciente, n (%) | 4 (1,7) | 4 (2,3) | 0 (0) | 0,575 |
| Hoja de limitación del tratamiento de soporte vital (LTSV) actualizada, n (%) | 51 (22,3) | 42 (24,6) | 9 (15,5) | 0,212 |
| Evaluación diaria de la necesidad de catéteres, n (%) | 8 (4,2) | 5 (3,7) | 3 (5,2) | 0,700 |
| Sistema de información clínica | 90 (15,7) | 55 (13,8) | 35 (20,1) | 0,071 |
| Validación de información obtenida de los dispositivos, n (%) | 8 (17,4) | 5 (13,2) | 3 (37,5) | 0,129 |
| Correcto cumplimiento de la información médica, n (%) | 18 (9,5) | 10 (7,6) | 8 (13,8) | 0,281 |
| Integración correcta con otros departamentos del Hospital, n (%) | 64 (33,3) | 40 (29,9) | 24 (41,4) | 0,165 |
COVID: COronaVIrus Disease.
En negrita, p<0,05.
Respecto a las medidas, comparados ambos subgrupos, la revisión de alarmas de la ventilación mecánica (VM) (66,7% vs 43,0%; p=0,032) y la monitorización de la nutrición enteral (45,5% vs 24,4%; p=0,046) fueron significativamente superiores en los pacientes COVID. Sin embargo, la evaluación de la movilización y la evaluación de la debilidad muscular adquirida en la UCI (26,0% vs 7,0%; p=0,018) fueron significativamente superiores en los pacientes no-COVID.
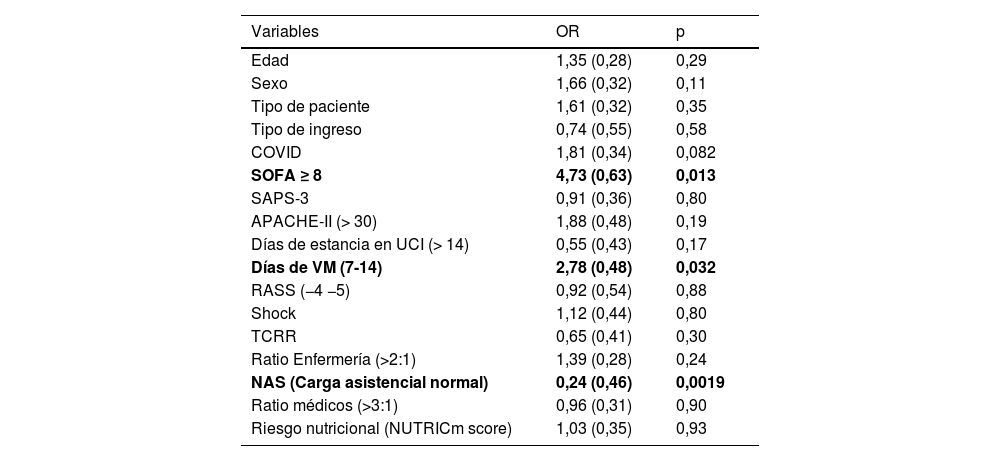
La tabla 4 muestra el impacto de las variables independientes seleccionadas en el PMR-AASTRE-G. El NAS<50 (carga asistencial normal) se asoció a una mayor probabilidad de realizar las medidas de obligado cumplimiento (OR: 0.24 [std 0,46]; p=0,0019). Por otra parte, tanto los días de VM (OR: 2.78 [std 0,48]; p=0,032) como el SOFA ≥8 (OR: 4.73 [std 0,63]; p=0,013) fueron factores que se asociaron de forma independiente a una mayor utilidad global de la herramienta (PMR-AASTRE-G ≥10%).
Análisis multivariado para PMR-AASTRE-G ≥10%. Datos presentados como OR y std entre paréntesis (p<0,05)
| Variables | OR | p |
|---|---|---|
| Edad | 1,35 (0,28) | 0,29 |
| Sexo | 1,66 (0,32) | 0,11 |
| Tipo de paciente | 1,61 (0,32) | 0,35 |
| Tipo de ingreso | 0,74 (0,55) | 0,58 |
| COVID | 1,81 (0,34) | 0,082 |
| SOFA ≥ 8 | 4,73 (0,63) | 0,013 |
| SAPS-3 | 0,91 (0,36) | 0,80 |
| APACHE-II (> 30) | 1,88 (0,48) | 0,19 |
| Días de estancia en UCI (> 14) | 0,55 (0,43) | 0,17 |
| Días de VM (7-14) | 2,78 (0,48) | 0,032 |
| RASS (−4 −5) | 0,92 (0,54) | 0,88 |
| Shock | 1,12 (0,44) | 0,80 |
| TCRR | 0,65 (0,41) | 0,30 |
| Ratio Enfermería (>2:1) | 1,39 (0,28) | 0,24 |
| NAS (Carga asistencial normal) | 0,24 (0,46) | 0,0019 |
| Ratio médicos (>3:1) | 0,96 (0,31) | 0,90 |
| Riesgo nutricional (NUTRICm score) | 1,03 (0,35) | 0,93 |
APACHE-II: ≤14, 15-29, ≥30; COVID: Sí/No; Días de estancia en UCI: <7, 7-14, >14; Días de VM: <7, 7-14, >14; Edad: ≤ 65; >65; NAS (Nursing Activities Score): ≤50 (carga asistencial normal), >50 (alta carga asistencial); RASS: (−1, −2, −3) y (−4, −5); Ratio enfermería: ≤2:1, >2:1; Ratio médico: ≤3:1, >3:1; Riesgo nutricional: bajo riesgo nutricional (0-4), alto riesgo nutricional (5-9); SAPS-3: <60, 60-80, >80; Sexo: hombre/mujer; Shock: portador de NA, vasopresina o dobutamina; SOFA: <4, 4-7, 8-12, >12; TCRR: Sí/No; Tipo de ingreso: urgente/programado; Tipo de pacientes: médico/quirúrgico.
En negrita, p<0,05.
Este es el primer estudio realizado durante la pandemia que evaluó el efecto de una intervención de seguridad que permitió convertir situaciones inseguras en seguras en tiempo real. Se demostraron su factibilidad y su utilidad tanto en pacientes COVID como en no-COVID.
Es destacable la escasa presencia de estudios sobre seguridad clínica durante la pandemia24. Hay autores que describen incidentes relacionados con la seguridad del paciente (IRSP) asociados a retrasos en el tratamiento o a la realización de procedimientos inadecuados, sugiriendo que la utilización de herramientas proactivas de seguridad hubiera podido ser útil en aquel contexto25. Paralelamente, se ha tratado de explicar la brecha en seguridad a través de la necesidad de readaptar los recursos personales: muchos referentes de seguridad volvieron a una actividad netamente asistencial, impidiendo que muchas unidades funcionales pudieran conservar o promover sus actividades26.
AASTRE, por su parte, es una herramienta arraigada en la cultura de nuestra organización. Este hecho probablemente pueda relacionarse con la factibilidad descrita en este estudio. AASTRE se fundamenta en la interacción de los profesionales sanitarios (unos responsables del cuidado del paciente y otros que vehiculizan la comprobación de las medidas [prompter])16. De este modo se aleja la idea de rondas de seguridad vehiculizada por directivos o referentes de seguridad. De hecho, en nuestra experiencia la presencia de médicos en formación y personal de enfermería durante las auditorías convierte el momento de interacción en un espacio de aprendizaje organizativo17 teniendo como centro los procesos. En relación con esto, se ha descrito que uno de los factores que mejora significativamente la aceptación de las auditorías es la construcción de un sentido compartido del resultado de las mismas27.
Un resultado especialmente llamativo fue la elevada utilidad de la herramienta durante el periodo analizado (PMR-AASTRE-G del 11,8%), sensiblemente superior al obtenido por AASTRE en otros periodos anteriores a la pandemia (5,4 y 6,7%)16,17. La utilidad en AASTRE se asocia directamente a una mejoría de la seguridad en tiempo real, dado que las medidas evaluadas, si no estaban realizadas en el momento de la auditoría (errores de omisión), se ejecutaron en ese momento (tiempo real). Estudios previos17 asociaron la utilidad de AASTRE en momentos de mayor sobrecarga asistencial. En este estudio, el equipo asistencial trató indistintamente pacientes COVID y no-COVID, por lo que la sobrecarga asistencial se repartió homogéneamente entre todos los profesionales. Esta sobrecarga mantenida, traducida en fatiga física y cognitiva, se ha relacionado en la pandemia con errores de omisión a través de la influencia en la toma de decisiones y la priorización de las tareas28,29. En relación con la utilidad, Arabi et al.30 concluyeron que, en situaciones como las vividas durante la pandemia, uno de los aprendizajes básicos fue la necesidad de priorizar en la utilización de medidas basadas exclusivamente en la evidencia científica, aspecto que garantiza AASTRE.
Se ha descrito que la carga asistencial (altos ratios de enfermería y médico/paciente) se asoció a una menor calidad asistencial, a un mayor número de eventos adversos, a una mayor estancia hospitalaria y a mayor mortalidad31,32. Margadant et al.33 demostraron que el NAS elevado estaba asociado con la mortalidad intrahospitalaria. En esta dirección, nuestro estudio demostró que evitar la sobrecarga asistencial de enfermería (definida mediante el NAS)34 se asoció con el correcto cumplimiento de las medidas basadas en la evidencia y, por tanto, menor proporción de errores de omisión.
Coincidiendo con lo que describió Ilan et al.35 y lo que se ha demostrado en estudios previos16,17, en nuestro estudio se objetivó que la gravedad del paciente se asoció a una utilidad significativa de la herramienta. Esto se explica porque una alta gravedad de los pacientes provoca que una gran proporción de los esfuerzos de la atención y asistencia médica se destinen a aquellas medidas necesarias para la pronta reanimación del paciente y, por contra, se dejen de lado otras medidas menos urgentes, aunque también importantes y basadas en la evidencia científica.
Es destacable remarcar que, a pesar de ser el grupo COVID un grupo más grave, con mayor días de ingreso, días de ventilación mecánica y días de sonda vesical, no hay diferencias significativas en cuanto a indicadores de resultado como son las tasas de NAVM, traqueobronquitis, BRC e infecciones relacionadas con la sonda vesical, tal y como sí describen otros autores8-10.
El interés de cualquier sistema sanitario es optar a la excelencia velando por el mejor interés de los pacientes. Por esa razón, los profesionales sanitarios como primera medida deben ambicionar conocer cómo desempeñan su función, independientemente de la complejidad contextual. Es este sentido, AASTRE ha demostrado ser un robusto sostén de la calidad asistencial, no solo por su utilidad (ya comentada), sino porque proporciona una forma de retroalimentación cuantitativa que se ha demostrado esencial para pilotar cualquier mejora de la calidad asistencial36.
LimitacionesEste estudio tiene diversas limitaciones. 1)Se trata de un estudio realizado en un único centro. 2)El estudio se llevó a cabo durante la sexta ola de la pandemia, cuando la presión asistencial todavía era elevada, aunque menor en comparación con otros momentos de la misma (aunque todavía lejos de unas condiciones asistenciales normales [Moreno-Mulet et al.37]). En cualquier caso, la menor presión asistencial sin duda favoreció la posibilidad de implementar AASTRE. 3)El estudio se realiza en una época donde ya no había colaboración con otras especialidades (cardiología, pediatría, urgencias, anestesia), como sí pasó en otras olas. Este aspecto hubiera sido interesante analizarlo, ya que en esas circunstancias el uso de AASTRE provoca una interacción entre prompter y médico en formación que permite la formación de un espacio de aprendizaje20 que, probablemente, hubiera tenido todavía más repercusión como herramienta de transmisión de la información y aprendizaje. 4)Por último, no se han tenido en cuenta las herramientas reactivas como son notificaciones de efectos adversos, datos que nos hubiera ayudado a analizar la situación de nuestra UCI en cuanto a seguridad se refiere en la época estudiada.
ConclusionesAASTRE resultó ser una herramienta factible y útil durante la fase final de la pandemia (caracterizada todavía por una moderada presión asistencial) con solo dos intervenciones semanales de aproximadamente de 30minutos. La complejidad asistencial en un entorno de pacientes COVID y no-COVID puede explicar la utilidad de AASTRE en ambos grupos de pacientes con un llamativo aumento del PMR-AASTRE-G respecto a periodos analizados previamente.
FinanciaciónEste estudio ha sido financiado por el Instituto de Salud CarlosIII (ISCIII) a través del proyecto «FIS PI20/01674» y cofinanciado por la Unión Europea y la beca de la Fundación Ricardo Barri Casanovas.
Consideraciones éticasEl estudio fue aprobado por el Comité de Ética e Investigación Clínica (CEIC) del Institut d’Investigació Sanitària Pere Virgili. Referencia: 3/2021. Dadas las características del estudio y el anonimato de los datos, se consideró innecesario obtener consentimiento informado.
Contribución de los autoresMB, GS, MS y AR contribuyeron al diseño del estudio. MB, GS y MS llevaron a cabo las rondas de seguridad. JB y JC contribuyeron en la configuración del SIC y en el cálculo de métricas de los indicadores y medidas de proceso. JC, AR y JB contribuyeron al análisis de datos y análisis estadístico. JC y MB realizaron la construcción e implementación de la plataforma de indicadores de proceso. Todos los autores contribuyeron en la redacción del manuscrito. Todos los autores leyeron y aprobaron el manuscrito final.
Conflicto de interesesLos autores declaran que no tienen intereses financieros o relaciones personales que puedan haber influido en el trabajo presentado en este artículo.
Agradecemos profundamente a los profesionales del Departamento de Medicina Intensiva del Hospital Universitari de Tarragona JoanXXIII por su compromiso en asegurar la calidad de los datos introducidos en el Sistema de Información Clínica.