La hiperleucocitosis puede provocar insuficiencia respiratoria por leucostasis pulmonar. Adicionalmente, el análisis gasométrico puede evidenciar una seudohipoxemia y someter al paciente a tratamientos innecesarios en caso de no ser reconocida.
Presentamos el caso de un varón de 25 años, portador de leucemia mieloide crónica (LMC) diagnosticada hace 10 años con mala adherencia al tratamiento. El paciente ingresa en el servicio de urgencia por astenia y adinamia de 2 semanas de evolución, agregando disnea en las 24h previas. Al examen físico se constata paciente lúcido, apirético, polipnea de 29rpm, estertores crepitantes difusos, oximetría de pulso (SpO2) del 90% con oxigenoterapia mediante máscara de bajo flujo. Hemodinámicamente estable. Abdomen distendido, hepatomegalia y esplenomegalia grado V. En la analítica se destacaba hemoglobina 3,6g/dl, leucocitosis 688.000células/μl, plaquetas 321.000 células/μl. Frotis en sangre periférica compatible con LMC en fase crónica. La radiografía de tórax evidenció una discreta opacidad parahiliar derecha. El paciente ingresó en la unidad de cuidados intensivos con intenso trabajo respiratorio, iniciándose asistencia ventilatoria mecánica (AVM) no invasiva. A los 30minutos, el paciente se encontraba confuso, polipneico (30-35rpm) y con asincronía tóraco-abdominal. Si bien la SpO2 era del 95% la gasometría arterial (Radiometer ABL800 FLEX, Dinamarca) evidenció una insuficiencia respiratoria grave: PaO2=50mmHg, PaCO2=38mmHg, saturación arterial de oxígeno (SaO2) del 86% (fracción inspirada de oxígeno=0,6, presión soporte=8cmH2O, presión positiva al final de la espiración=9cmH2O). Se procedió a intubación orotraqueal y AVM invasiva. Con la sospecha de insuficiencia respiratoria causada por leucostasis se inició tratamiento citorreductor mediante administración de hidroxiurea y leucaféresis asociado a tratamiento molecular de la LMC con dasatinib. Se transfundieron concentrados de glóbulos rojos para corrección de la anemia.
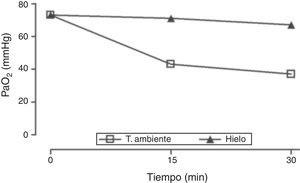
Al ingreso en la unidad se evidenció una marcada disociación entre la oximetría de pulso (SpO2≥95%) y la gasometría arterial (SaO2<90%, PaO2≤50mmHg). Los niveles de metahemoglobina (0%) y carboxihemoglobina (1,4%), así como la p50 (25,9mmHg) fueron normales. Debido a la marcada hiperleucocitosis se planteó una seudohipoxemia o hipoxemia espuria generada por excesivo consumo de oxígeno luego de la extracción de la muestra. Para evaluar esta hipótesis se realizaron en forma simultánea gasometrías arteriales de muestras conservadas a temperatura ambiente o en hielo (para enlentecer el consumo metabólico) durante 30min (leucocitosis 688.000células/μl al momento de la extracción). Mientras la PaO2 y la SaO2 se mantenían relativamente constantes en la sangre conservada en hielo, estas disminuían dramáticamente a temperatura ambiente, apoyando la hipótesis de la seudohipoxemia (fig. 1). La conservación en frío de la muestra y el rápido procesamiento de la misma permitió minimizar este error preanalítico en las determinaciones posteriores.
Medida de PaO2 en muestras de sangre arterial conservadas a temperatura ambiente o en hielo. Ambas muestras fueron extraídas al mismo tiempo (FiO2 1, leucocitosis 688.000 células/μl). Se realizó análisis gasométrico inmediatamente después de la extracción y posteriormente a los 15 y 30min.
FiO2: fracción inspirada de oxígeno; PaO2: presión parcial de oxígeno en sangre arterial; T. ambiente: temperatura ambiente.
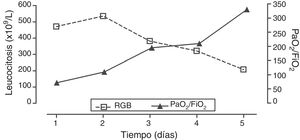
El paciente recibió 6 sesiones de leucaféresis asociadas a tratamiento con hidroxiurea, presentando una evolución favorable con disminución progresiva de la leucocitosis y mejoría gradual del intercambio gaseoso (fig. 2). No presentó complicaciones infecciosas ni otras disfunciones orgánicas, así como tampoco elementos sugestivos de síndrome de lisis tumoral (SLT) o coagulación intravascular diseminada (CID). El paciente se desvinculó de la AVM a los 6 días del ingreso, lúcido y sin alteraciones neurológicas. Luego de permanecer internado en sala de medicina interna fue dado de alta a domicilio asintomático y con franca mejoría del trastorno hematológico (hemoglobina 7,7g/dl, leucocitosis 60.700 células/μl y plaquetas 213.000 células/μl).
La hiperleucocitosis se define como un recuento de glóbulos blancos (RGB) mayor a 100.000 células/μl y se asocia a un incremento de la morbimortalidad en pacientes con distintos tipos de leucemia1. Sus principales manifestaciones clínicas son debidas a leucostasis (infiltración orgánica por células leucémicas), SLT y/o CID2. A nivel pulmonar, la leucostasis puede provocar insuficiencia respiratoria por obstrucción microvascular, alterando la relación ventilación/perfusión y la difusión de gases3. Independientemente de esto, el análisis gasométrico en pacientes con hiperleucocitosis puede evidenciar una seudohipoxemia o hipoxemia espuria, es decir, en pacientes que no tienen verdaderamente una PaO2 disminuida. La principal explicación de este fenómeno, descrito en 1979, se basa en el elevado consumo metabólico por parte de las células sanguíneas luego de la extracción de la muestra4,5. De hecho, la magnitud del mismo se correlaciona con el RGB6. En caso de no ser reconocido puede conducir a errores de interpretación, diagnosticando insuficiencia respiratoria en pacientes que no la tienen o sobredimensionando la gravedad de la misma7. Esto puede tener un impacto negativo sobre los pacientes si se considera la PaO2 como criterio para definir la necesidad de procedimientos diagnósticos o terapéuticos como la AVM. El médico debe tener presente este fenómeno para poder reconocerlo, siendo la discordancia entre SpO2 y SaO2 una observación clave.
Distintos autores han reportado que la conservación en hielo de la muestra y su procesamiento inmediato puede disminuir este error4,5,8. No obstante, este hallazgo no fue consistente en otros trabajos en los que se observó cierta disminución en la PaO2 pese al enfriamiento de la sangre6. Por otra parte, la incorporación de fluoruro de sodio o cianuro de potasio a la muestra podría inhibir el consumo metabólico y prevenir el desarrollo de hipoxemia expuria5,9. En este tipo de pacientes el seguimiento mediante oximetría de pulso cobra especial relevancia, siempre que se descarte la presencia de metahemoglobinemia y carboxihemoglobinemia que pueden afectar la medida de SpO27.
En conclusión, la hiperleucocitosis puede provocar hipoxemia verdadera y/o espuria. Es fundamental mantener un elevado índice de sospecha y despistar la existencia de esta última. En caso de no ser reconocida puede condicionar la aplicación de tratamientos innecesarios y potencialmente perjudiciales para los pacientes.