Comparar la administración precoz de surfactante, antes de las 12h de vida, frente a tardía, en prematuros tardíos (nacidos entre 34+0 y 36+6 semanas de gestación) con distrés respiratorio moderado/grave.
DiseñoEstudio retrospectivo, observacional, analítico, caso/control, con prematuros tardíos ingresados entre 2012-2021. Se dividen en 2 grupos: surfactante administrado ≤12h de vida y >12h, y se compara la evolución, mediante análisis univariante.
ÁmbitoUnidad de cuidados intensivos neonatal (UCIN) nivel III de un hospital universitario.
Pacientes o participantesCincuenta y siete pacientes, 30 en el grupo precoz y 27 en el tardío. Criterios de inclusión: neonatos de 34+0 a 36+6 semanas de gestación, con síndrome de dificultad respiratoria y necesidad de ventilación no invasiva y surfactante.
IntervencionesNinguna.
Variables de interés principalesSociodemográficas, clínicas y evolutivas: redosificación, duración de soporte respiratorio, oxígeno y tiempo en dejar de precisarlo tras el surfactante. También complicaciones y duración de hospitalización.
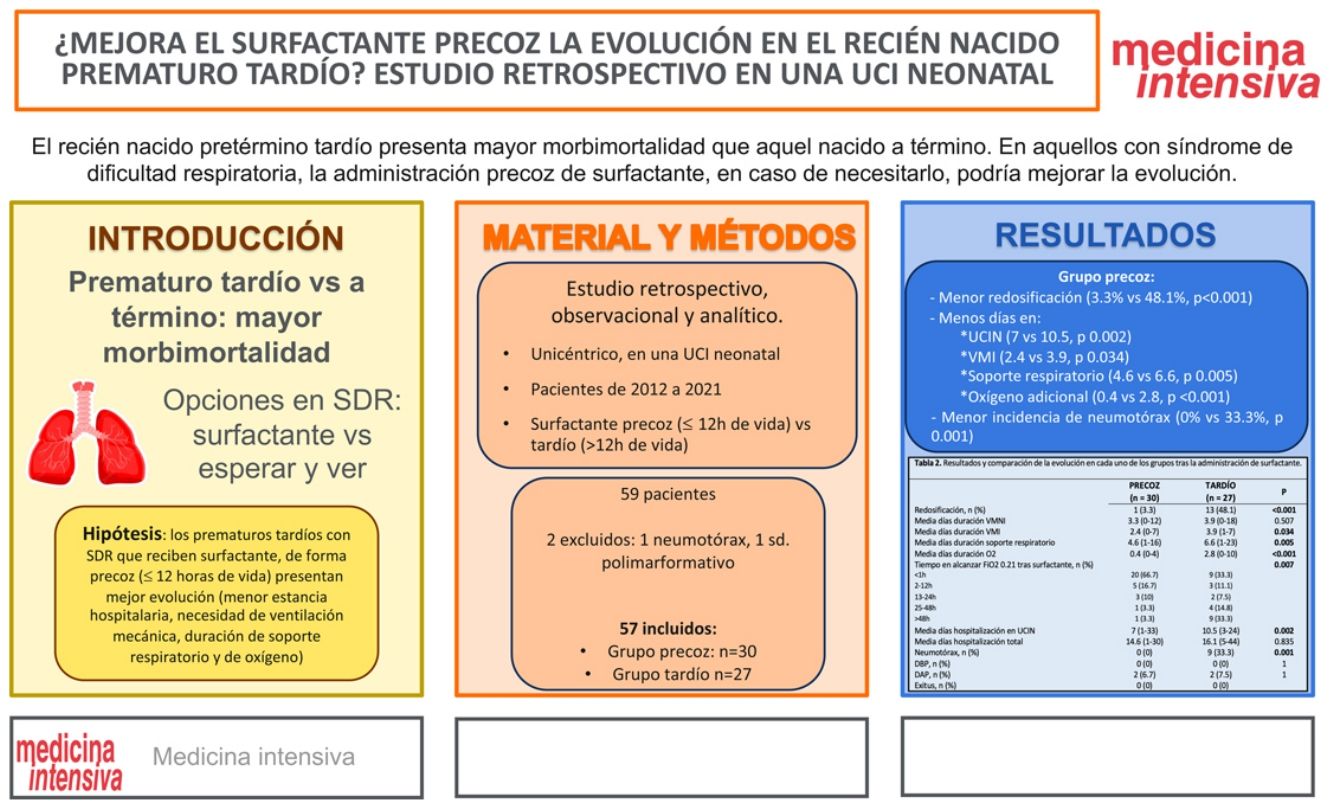
ResultadosEn el grupo precoz hubo menor necesidad de redosificación (3,3 vs. 48,1%; p<0,001) y disminución de duración, en días, de estancia en UCIN (7 vs. 10,5; p 0,002), ventilación mecánica invasiva (2,4 vs. 3,9; p 0,034), soporte respiratorio total (4,6 vs. 6,6; p 0,005) y oxigenoterapia (0,4 vs. 2,8; p<0.001). También, menor incidencia de neumotórax (0 vs. 33,3%; p 0,001). Además, a las 12h de la administración, mantenían FiO2 0,21 el 83,4 vs. 44,4% en el tardío.
ConclusionesEn nuestro estudio, la administración precoz en prematuros tardíos proporciona beneficios en cuanto a asistencia respiratoria y complicaciones. Sugerimos la ampliación de estudios para poder establecer recomendaciones en este grupo de pacientes.
To compare the early administration of surfactant, before 12hours of life, versus late, in late preterm neonates (born between 34+0 and 36+6 weeks of gestation), with moderate-severe respiratory distress.
DesignRetrospective, observational, analytical, case-control study, with late preterm infants admitted between 2012-2021. It is divided into 2 groups: surfactant administered ≤12hours of life and >12h and evolution is compared using univariate analysis.
SettingNeonatal Intensive Care Unit (NICU) level III of a Universitary Hospital.
Patients or participants57 patients, 30 in the early group and 27 in the late group. Inclusion criteria: neonates from 34+0 to 36+6 weeks of gestation, with respiratory distress syndrome, in need of non-invasive ventilation and surfactant.
InterventionsNone.
Main variables of interestSociodemographic, clinical and evolutionary: redosing, duration of respiratory support, oxygen and time to stop requiring it after surfactant. Also, complications and length of hospitalization.
ResultsIn the early group there was less need for redosing (3.3% vs 48.1%, P<.001) and a decrease in duration, in days, of stay in the NICU (7 vs 10.5, P .002), invasive mechanical ventilation (2.4 vs 3.9, p0.034), total respiratory support (4.6 vs 6.6, P0.005) and oxygen therapy (0.4 vs 2.8, P<.001). Also, lower incidence of pneumothorax (0% vs 33.3%, P .001). Furthermore, 12hours after administration, 83.4% maintained FiO2 0.21, compared to 44.4% in the late administration.
ConclusionsIn our study, early administration in late preterm infants provides benefits in terms of respiratory assistance and complications. We suggest expanding studies to establish recommendations in this group of patients.
El prematuro tardío, nacido entre las 34+0 y las 36+6 semanas de gestación, representa el 70-74% de todos los partos prematuros. Presentan unas características que les confieren un riesgo de morbimortalidad hasta 2-3 veces mayor que aquellos nacidos a término, doblando los costes medios de salud de estos últimos1–3.
En el estudio del grupo SEN34-36 en 20182, con la participación de 9.121 pacientes de 34 hospitales, se objetivó que el 58,6% de los prematuros tardíos precisó ingreso en la unidad de neonatología, y hasta el 15% en la unidad de cuidados intensivos neonatal (UCIN), con una estancia media de 11 y 12 días, respectivamente.
Una de las causas principales de ingreso de esta población son las complicaciones respiratorias, desarrollándose el síndrome de dificultad respiratoria (SDR) hasta en el 10%. Esto condiciona una mayor morbimortalidad y una estancia hospitalaria más prolongada, con el perjuicio adicional de separación madre-hijo1–3. El tratamiento respiratorio, mejor establecido en recién nacidos más prematuros, genera controversia. Es por ello que, en ocasiones, se adopta una actitud expectante respecto a la administración de surfactante, decidiéndose su uso más tardíamente, cuando la evolución no es la esperada1–5.
La evidencia actual en los prematuros tardíos sugiere un menor riesgo de mortalidad, escape aéreo, hipertensión pulmonar persistente y duración del soporte respiratorio cuando reciben surfactante6–8. Tal y como indica la última Guía de Consenso Europeo, ante la heterogeneidad de los datos, actualmente no hay suficiente evidencia para establecer recomendaciones3.
Debido a lo anteriormente citado se presenta este estudio. El objetivo primario fue describir la evolución clínica tras el uso de surfactante en un grupo de prematuros tardíos. Como objetivo secundario se compara en función del tiempo de aplicación para determinar si un uso precoz resulta protector.
Material y métodosDiseño del estudio y participantesEstudio retrospectivo, observacional y analítico, en un solo centro, realizado desde enero de 2012 a diciembre de 2021, en una UCIN de tercer nivel.
Criterios de inclusiónRecién nacidos desde 34+0 hasta 36+6 semanas de gestación con diagnóstico de SDR, que precisen ventilación mecánica, tanto no invasiva (VNI), en forma de CPAP o presión positiva intermitente nasal (VPPIn); como invasiva (VMI). Además, debían haber recibido surfactante.
Los criterios para el diagnóstico de SDR fueron los pacientes con imagen radiológica típica (disminución de volumen pulmonar, infiltrado reticular) y requerimientos de oxígeno y/o distrés.
Criterios de exclusión- –
SDR leve, considerado como aquel SDR que se resuelve sin llegar a recibir surfactante.
- –
Taquipnea transitoria del recién nacido (TTRN), definida como distrés con rápida mejoría (menos de 12-24h), necesidades de FiO2<0,3 e imagen típica en radiografía (hiperinsuflación, líquido en cisuras).
- –
Pacientes con escape aéreo secundario a la reanimación en paritorio.
- –
Malformaciones mayores, cromosomopatías y/o enfermedades metabólicas.
Las radiografías de cada paciente son analizadas por los investigadores para distinguir entre TTRN y SDR.
Se dividieron los pacientes recogidos en 2 grupos: aquellos que recibieron el surfactante antes de las 12h de vida, incluidas, y aquellos en los que se administró más tardíamente. La decisión de las 12h de vida como punto de corte entre precoz y tardío fue arbitraria.
ProcedimientosSe utilizó surfactante de origen porcino, poractant alfa, a una dosis inicial de 200mg/kg y en caso de precisar redosificación a 100mg/kg. Los criterios para la administración fueron los establecidos en los años de recogida: FiO2≥0,3-0,4 a pesar de CPAP≥6cmH2O o distrés moderado-grave persistente junto con imagen radiológica compatible con SDR. Se decidió redosificación cuando persistían requerimientos de oxígeno o precisaba ventilación mecánica invasiva, tras 6-12h de la primera dosis, con un máximo de 3 dosis.
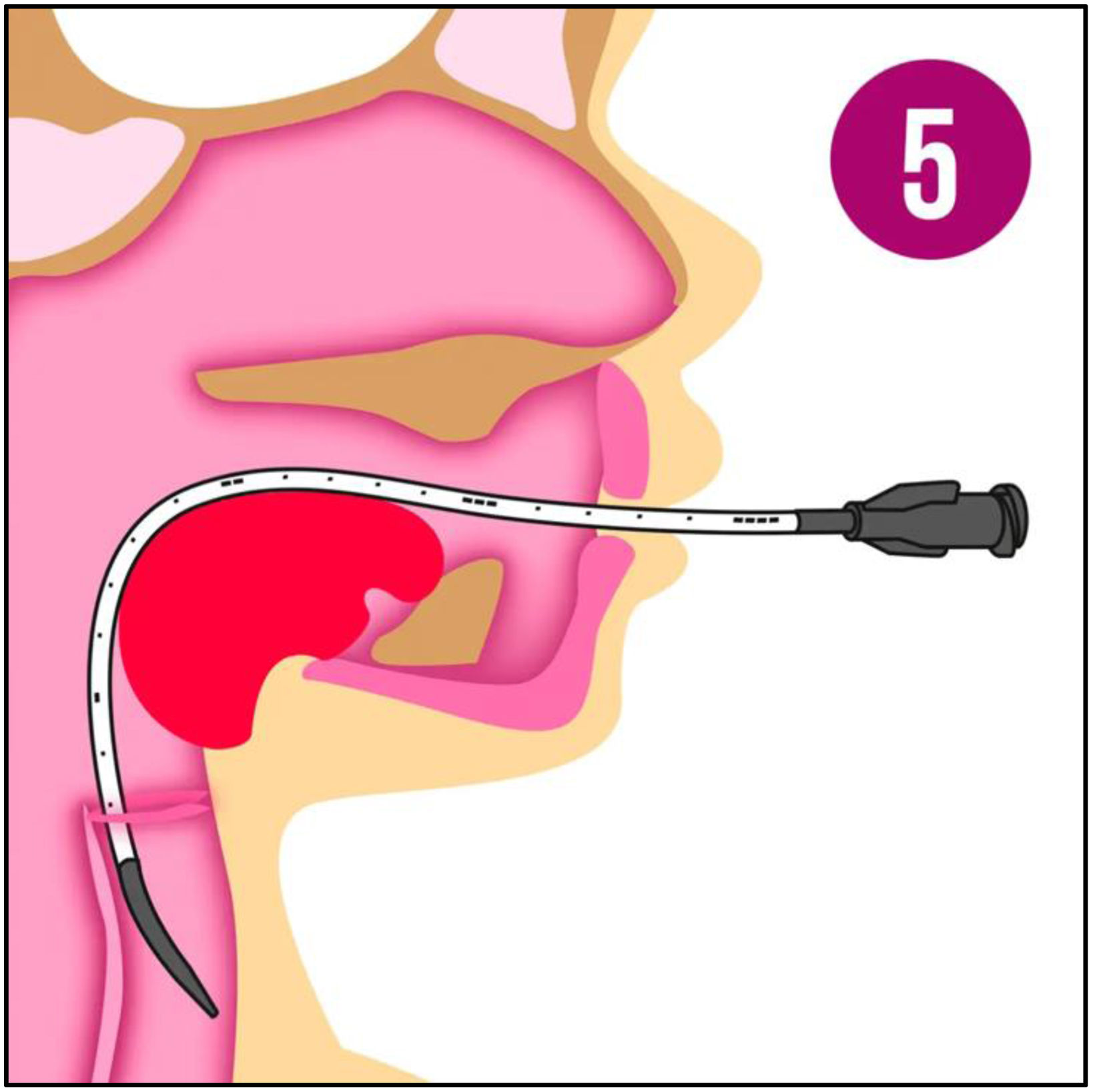
Se administró a través de tubo endotraqueal, por requerir intubación a criterio del facultativo, o mediante método mínimamente invasivo (less invasive surfactant administration [LISA]). Para este último se empleaba, inicialmente un angiocatéter de 16G en base al estudio de Dargaville et al.9–11. Posteriormente, a partir de 2017 se comenzó a utilizar el catéter LISAcath® de Chiesi, hecho de poliuretano y con un diámetro de 5 french (fig. 1). La técnica consiste en instilar el surfactante a través de dicho catéter, colocado, mediante laringoscopia directa, más allá de las cuerdas vocales, mientras el paciente se mantiene conectado a VNI (fig. 2). Durante y después del procedimiento se realiza aspiración a través de sonda orogástrica para comprobar la correcta administración.
Catéteres empleados en la técnica LISA: angiocatéter de 16G (imagen de elaboración propia) y LisaCath®19,20.
Realización de la técnica LISA con catéter Surfcath®21, empleado actualmente en nuestra unidad.
Se recogieron variables sociodemográficas relacionadas con la situación pre y perinatal de los pacientes, así como de la situación clínica previa y tras recibir el surfactante. También, datos del momento y tipo de administración del mismo, además de la evolución posterior y posibles complicaciones. Todas estas variables quedan recogidas en el anexo 1.
Análisis estadísticoEl análisis descriptivo de datos se realiza mediante el software R versión 4.2.3. Las variables categóricas se describen con números absolutos (n) y porcentajes (%) y son analizadas mediante el test de Chi-cuadrado y la corrección de Yate en caso de ser necesario. Las variables continuas que siguen una distribución normal se comparan usando la media±desviación estándar (DE) y son analizadas con el test de T de Student. En caso contrario se describen con la mediana con rangos y se estudian usando la prueba de U de Mann-Whitney. Se considera significación estadística si p<0,05.
ResultadosSignos de dificultad respiratoriaEntre 2012 y 2021 nacieron, en nuestra área hospitalaria, un total de 966 pretérminos tardíos. Precisaron ingreso en LA UCIN, con diagnóstico de distrés respiratorio, 140 pacientes (14,5%). De ellos, 57 (40,7%) fueron considerados como TTRN, 24 (17,1%) como SDR leve sin necesidad de surfactante y 59 (42,1%) como SDR que precisó surfactante. Hasta 135 de los 140 pacientes (96,4%) requirieron soporte respiratorio en algún momento del ingreso.
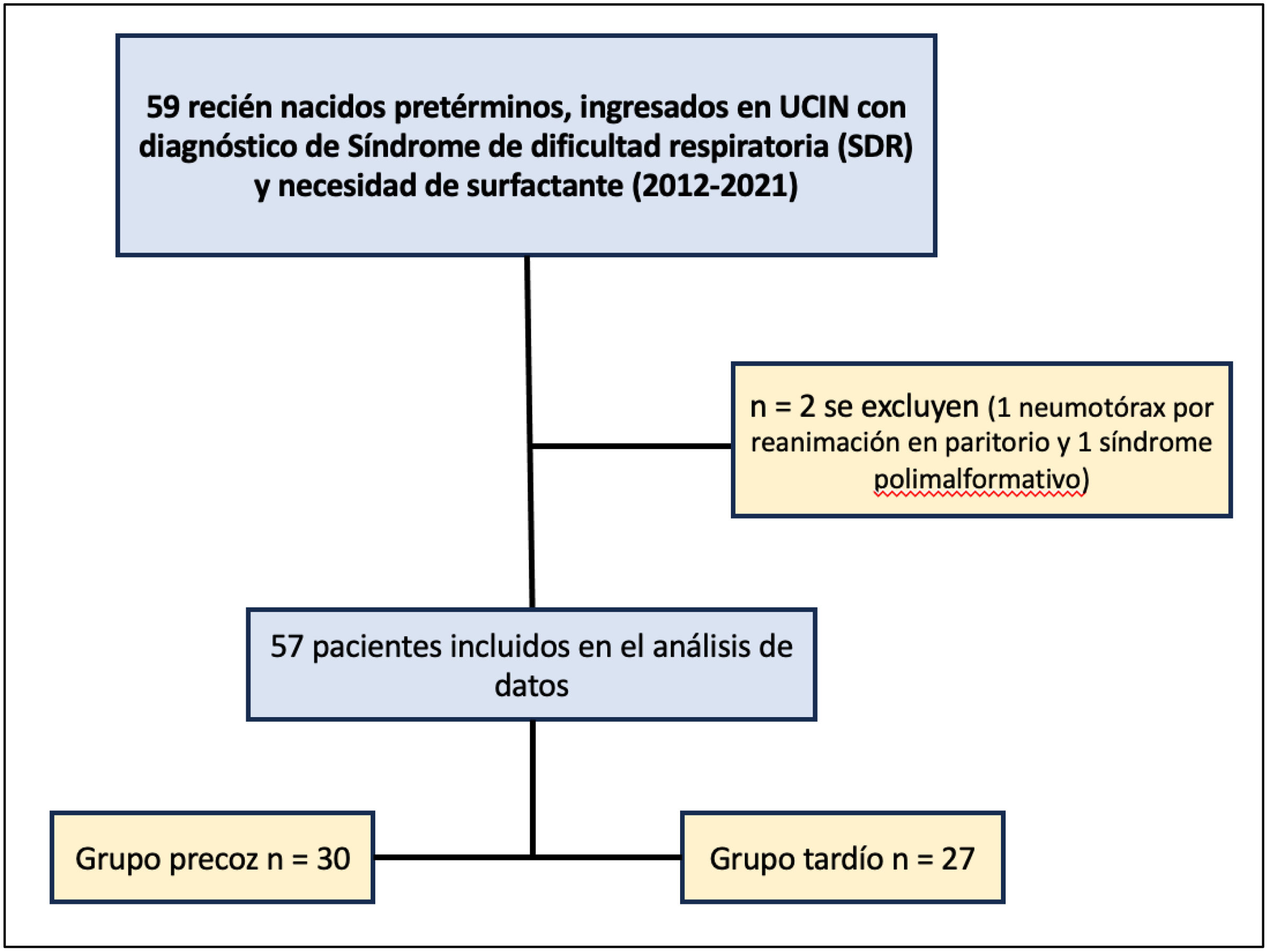
Características epidemiológicasDe los 59 pacientes que precisaron surfactante se incluyeron finalmente 57, quedando 30 recién nacidos (52,6%) en el grupo precoz y 27 (47,4%) en el tardío (fig. 3).
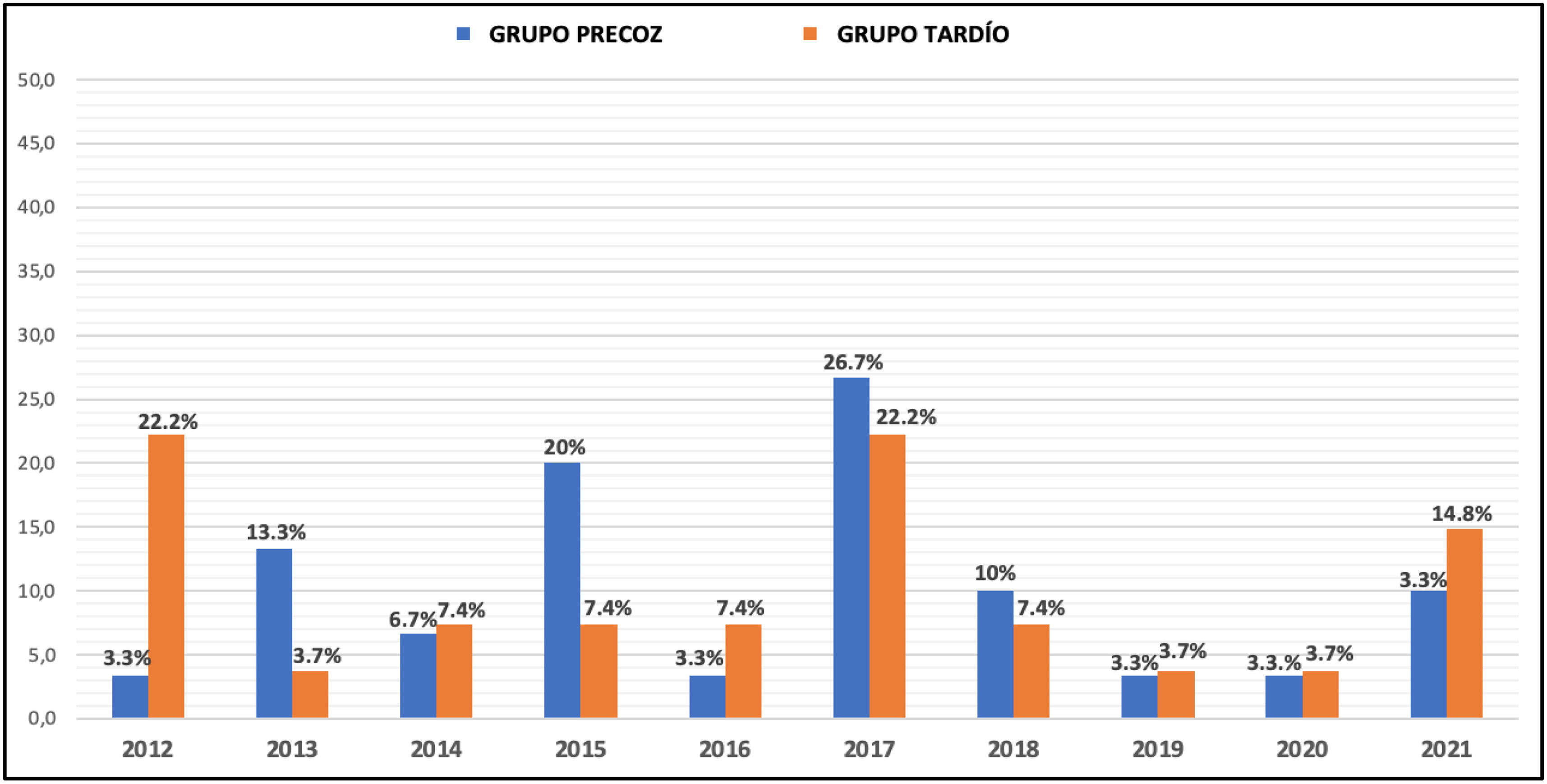
Las características de los grupos a estudio se muestran en la tabla 1 y la distribución por años de recogida se observa en la figura 4.
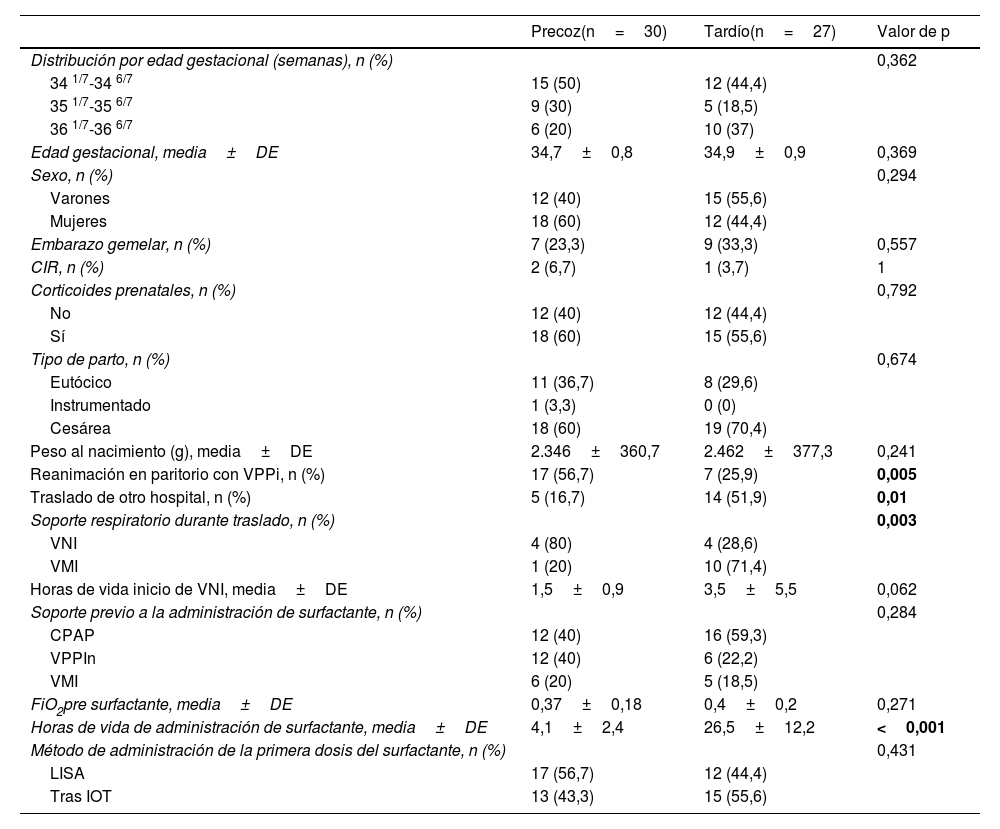
Características demográficas y clínicas de los pacientes incluidos, así como el momento y el método de administración de los surfactantes en cada grupo
| Precoz(n=30) | Tardío(n=27) | Valor de p | |
|---|---|---|---|
| Distribución por edad gestacional (semanas), n (%) | 0,362 | ||
| 34 1/7-34 6/7 | 15 (50) | 12 (44,4) | |
| 35 1/7-35 6/7 | 9 (30) | 5 (18,5) | |
| 36 1/7-36 6/7 | 6 (20) | 10 (37) | |
| Edad gestacional, media±DE | 34,7±0,8 | 34,9±0,9 | 0,369 |
| Sexo, n (%) | 0,294 | ||
| Varones | 12 (40) | 15 (55,6) | |
| Mujeres | 18 (60) | 12 (44,4) | |
| Embarazo gemelar, n (%) | 7 (23,3) | 9 (33,3) | 0,557 |
| CIR, n (%) | 2 (6,7) | 1 (3,7) | 1 |
| Corticoides prenatales, n (%) | 0,792 | ||
| No | 12 (40) | 12 (44,4) | |
| Sí | 18 (60) | 15 (55,6) | |
| Tipo de parto, n (%) | 0,674 | ||
| Eutócico | 11 (36,7) | 8 (29,6) | |
| Instrumentado | 1 (3,3) | 0 (0) | |
| Cesárea | 18 (60) | 19 (70,4) | |
| Peso al nacimiento (g), media±DE | 2.346±360,7 | 2.462±377,3 | 0,241 |
| Reanimación en paritorio con VPPi, n (%) | 17 (56,7) | 7 (25,9) | 0,005 |
| Traslado de otro hospital, n (%) | 5 (16,7) | 14 (51,9) | 0,01 |
| Soporte respiratorio durante traslado, n (%) | 0,003 | ||
| VNI | 4 (80) | 4 (28,6) | |
| VMI | 1 (20) | 10 (71,4) | |
| Horas de vida inicio de VNI, media±DE | 1,5±0,9 | 3,5±5,5 | 0,062 |
| Soporte previo a la administración de surfactante, n (%) | 0,284 | ||
| CPAP | 12 (40) | 16 (59,3) | |
| VPPIn | 12 (40) | 6 (22,2) | |
| VMI | 6 (20) | 5 (18,5) | |
| FiO2pre surfactante, media±DE | 0,37±0,18 | 0,4±0,2 | 0,271 |
| Horas de vida de administración de surfactante, media±DE | 4,1±2,4 | 26,5±12,2 | <0,001 |
| Método de administración de la primera dosis del surfactante, n (%) | 0,431 | ||
| LISA | 17 (56,7) | 12 (44,4) | |
| Tras IOT | 13 (43,3) | 15 (55,6) | |
CIR: crecimiento intrauterino retardado; CPAP: continuous positive airway pressure; DE: desviación estándar; IOT: intubación orotraqueal; LISA: less invasive surfactant administration; RIC: rango intercuartílico; VMI: ventilación mecánica invasiva; VNI: ventilación mecánica no invasiva; VPPIn: ventilación con presión positiva intermitente nasal.
Se han resaltado en negrita los valores de p estadísticamente significativos.
En el grupo de surfactante precoz se objetivó una mayor necesidad de reanimación con VPPi al nacimiento, siendo la diferencia estadísticamente significativa (tabla 1). La mediana de APGAR al minuto de vida fue de 8 en el grupo precoz y 9 en el tardío y a los 5min de 9 y 10.
Previo a la administración del surfactante, la mayoría de los pacientes recibieron VNI (tabla 1), con una presión positiva al final de la espiración (PEEP) 5-6cmH2O.
Administración de surfactanteLa situación previa a la administración de la primera dosis de surfactante y la posterior evolución pueden verse reflejadas en las tablas 1 y 2.
Se objetivó una redosificación hasta 12 veces mayor cuando se administró tardíamente, de forma estadísticamente significativa (p<0,001).
En el grupo tardío, el porcentaje de pacientes trasladados a nuestra unidad desde otros hospitales fue hasta 3 veces superior (tabla 1). De esos 14 pacientes, 11 (78.6%) cumplían criterios para la administración de surfactante antes de las 12h de vida. Sin embargo, solo 6 de los 11 (54.5%) lo recibieron en el hospital emisor y, además, fue de forma tardía.
Comparación entre gruposLos pacientes del grupo precoz precisaron de media menos días de VMI, soporte respiratorio total, oxígeno adicional y días de ingreso en UCIN, de forma estadísticamente significativa. Esto puede observarse en la tabla 2.
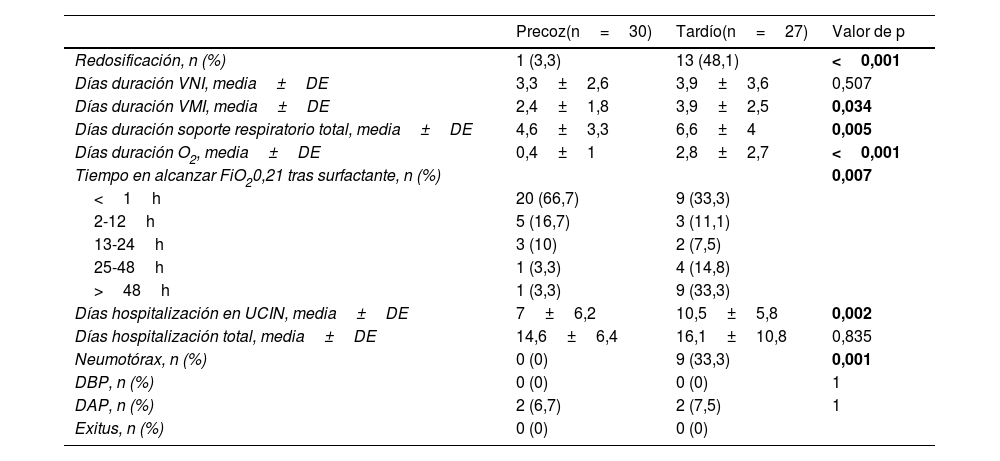
Resultados y comparación de la evolución en cada uno de los grupos tras la administración de surfactante
| Precoz(n=30) | Tardío(n=27) | Valor de p | |
|---|---|---|---|
| Redosificación, n (%) | 1 (3,3) | 13 (48,1) | <0,001 |
| Días duración VNI, media±DE | 3,3±2,6 | 3,9±3,6 | 0,507 |
| Días duración VMI, media±DE | 2,4±1,8 | 3,9±2,5 | 0,034 |
| Días duración soporte respiratorio total, media±DE | 4,6±3,3 | 6,6±4 | 0,005 |
| Días duración O2, media±DE | 0,4±1 | 2,8±2,7 | <0,001 |
| Tiempo en alcanzar FiO20,21 tras surfactante, n (%) | 0,007 | ||
| <1h | 20 (66,7) | 9 (33,3) | |
| 2-12h | 5 (16,7) | 3 (11,1) | |
| 13-24h | 3 (10) | 2 (7,5) | |
| 25-48h | 1 (3,3) | 4 (14,8) | |
| >48h | 1 (3,3) | 9 (33,3) | |
| Días hospitalización en UCIN, media±DE | 7±6,2 | 10,5±5,8 | 0,002 |
| Días hospitalización total, media±DE | 14,6±6,4 | 16,1±10,8 | 0,835 |
| Neumotórax, n (%) | 0 (0) | 9 (33,3) | 0,001 |
| DBP, n (%) | 0 (0) | 0 (0) | 1 |
| DAP, n (%) | 2 (6,7) | 2 (7,5) | 1 |
| Exitus, n (%) | 0 (0) | 0 (0) | |
DAP: ductus arterioso persistente; DBP: displasia broncopulmonar; DE: desviación estándar; UCIN: unidad de cuidados intensivos neonatal; VMI: ventilación mecánica invasiva; VNI: ventilación mecánica no invasiva.
Se han resaltado en negrita los valores de p estadísticamente significativos.
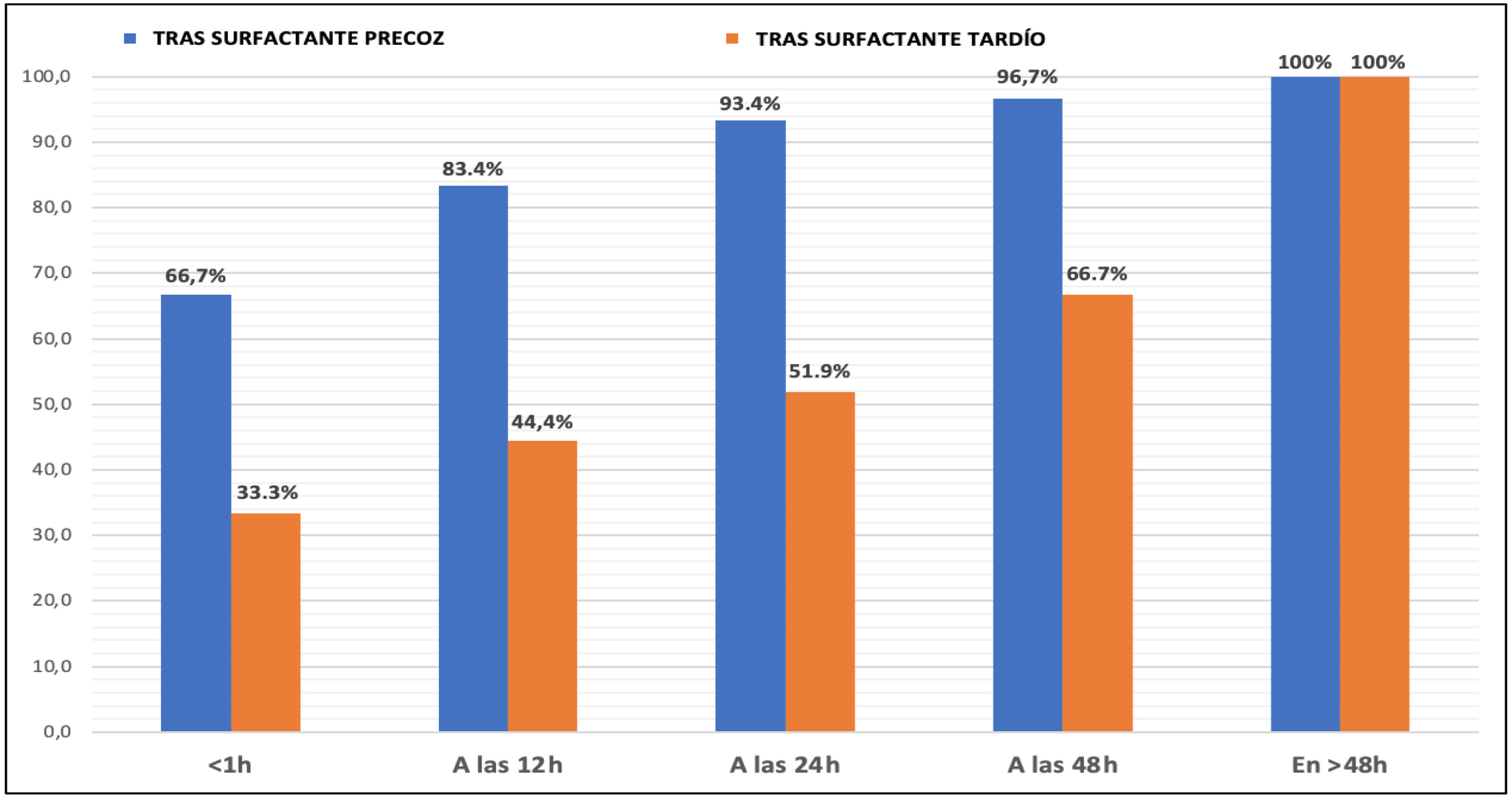
También se analizó el tiempo requerido para dejar de precisar oxígeno suplementario tras la primera dosis de surfactante, representado en la figura 5 en forma de porcentajes acumulados. Se puede ver como en el grupo precoz, 20 pacientes (66,7%) alcanzaron FiO2 0,21 a la hora, mientras que en el tardío dicho tanto por ciento precisó, al menos, 24 (p 0,007).
DiscusiónEn este estudio retrospectivo se analizan los posibles beneficios que puedan derivarse de la administración precoz del surfactante. La administración previa a las 12h de vida, en nuestro trabajo, se ha relacionado con una disminución tanto de los días de asistencia respiratoria como de hospitalización en la UCIN. Además, se han reducido los días con oxígeno, así como el tiempo necesario para dejar de precisarlo después de la primera dosis. Por otro lado, en dicho grupo también se ha observado una menor incidencia de neumotórax.
En la comparación de las características epidemiológicas de ambos grupos, no se encontraron diferencias estadísticamente significativas. Se observó un mayor número de pacientes que requirieron administración de VPPi en la reanimación en paritorio en el grupo de surfactante precoz. Sin embargo, al analizar el APGAR, se obtuvo una mediana al minuto y a los 5min de vida mayor de 8, en ambos grupos. Por ello, no se consideró dicha diferencia de relevancia clínica, ya que esos valores nos podrían indicar que la evolución fue favorable. Probablemente, la mayoría de aquellos prematuros tardíos que requirieron VPPi la recibieron únicamente en los primeros instantes de la asistencia en paritorio, con buena respuesta, no precisando más reanimación. En el grupo tardío se observó una tasa de traslados superior, lo que pudo contribuir a que presentaran un curso clínico más desfavorable, tanto por el estrés del traslado como por la posibilidad de haberse demorado el tratamiento.
La FiO2 media pre-surfactante fue mayor de 0,3 en los 2 grupos. En la mayoría de pacientes del grupo tardío se cumplían criterios radiográficos y clínicos en primeras 12h de vida. Sin embargo, en 12 (44,4%) se administró, de forma no invasiva, más tardíamente y en los otros 15 (55,6%) se esperó a precisar intubación, a criterio del facultativo. Esto podría deberse a que, en prematuros tardíos, se tiende en ocasiones a optimizar soporte respiratorio y mantener actitud expectante. Son pacientes que presentan adecuado esfuerzo respiratorio y la administración del surfactante implica una maniobra intervencionista12. Por otra parte, la implantación más tardía de la técnica LISA en hospitales sin UCIN también pudo contribuir a que se alcanzaran los criterios de intubación, probablemente, más tardíos que los de administración de surfactante.
En términos de asistencia respiratoria, en ambos grupos la VNI se inició al poco tiempo tras el inicio del distrés, si bien es cierto que en el tardío se demoró hasta 2h más respecto al precoz. Esto podría deberse, de nuevo, a la diferencia en el número de traslados. En aquellos hospitales sin UCIN, si la situación clínica lo permite, puede tenderse a iniciar oxigenoterapia de alto o bajo flujo y mantener actitud expectante. Se espera conseguir mejoría sin tener que escalar a VNI, cuyo inicio implicaría la necesidad de cuidados intensivos y el traslado del paciente a otro centro con dicha unidad. Sin embargo, la bibliografía indica que demorar el inicio de la ventilación no invasiva también podría ser un factor que conlleve peor evolución13. Sería importante unificar criterios, tanto para iniciar la asistencia respiratoria, como para administrar surfactante.
Tras la administración precoz de surfactante la mayoría de pacientes dejaron de necesitar FiO2 adicional en las primeras 24h, con un elevado porcentaje que no requería oxígeno a tan solo una hora de recibirlo, manteniendo este beneficio inalterable en su estancia. El paciente que precisó una segunda dosis en el grupo precoz fue el único que recibió la primera justo a las 12h de vida, tardando más de 48h en alcanzar 0,21. El contraste que se aprecia en el grupo tardío es que se precisa hasta 48h desde la administración para encontrar el mismo porcentaje de pacientes sin oxígeno, necesitando además redosificación en 13 recién nacidos (48,1%). De hecho, de los 9 pacientes que tardaron más de 48h en dejar de necesitar oxígeno, 8 recibieron segunda dosis. El paciente al que no se le administró había sido intubado por desarrollar un neumotórax, principal complicación del SDR14. En nuestro estudio no se observó ningún escape aéreo cuando el surfactante se empleaba de forma precoz, frente a un número significativamente mayor cuando se recibía de forma tardía. Suele ocurrir en pacientes con SDR con evolución tórpida, por lo que es de esperar, como así hemos objetivado y se refleja en la bibliografía15, que administrar el tratamiento en las primeras horas de vida pueda contribuir a reducir esta complicación.
La evidencia actual muestra que en prematuros más inmaduros la administración de surfactante en primeras horas de vida tiene efectos beneficiosos16. Sin embargo, en recién nacidos más cercanos a término, no existe consenso sobre las horas de vida adecuadas de administración3,15,17. El punto óptimo debería ser objeto de estudio. El análisis de la bibliografía actual incluye un trabajo publicado por el Grupo Neonatal de la Cochrane en 2012 que analiza los efectos de la administración de surfactante en las primeras 2h en recién nacidos intubados por SDR18. Actualmente está en desarrollo el estudio SURFON1, donde comparan el efecto del surfactante frente a actitud expectante en pretérminos tardíos y a término precoces. En él consideran como óptima la administración del tratamiento en las primeras 2-8h de vida, pero aceptan hasta las 24h.
Es importante tener en cuenta las limitaciones del trabajo. Es un estudio con un bajo tamaño muestral y retrospectivo, lo que conlleva una potencial pérdida de datos, permitiendo solo obtener hipótesis. Todas estas características, propias del tipo de estudio, se han intentado compensar poniendo énfasis en el reclutamiento, minimizando las pérdidas. Por otra parte, es unicéntrico, analizándose años donde la técnica LISA comenzaba a implantarse, con su correspondiente curva de aprendizaje. Destacar el posible sesgo resultante del mayor número de traslados en el grupo tardío, que podría influir en una administración más tardía del surfactante. En el análisis no se utilizó como variable el método de administración, si bien el porcentaje de cada uno era similar en ambos grupos, sin diferencias significativas. Tampoco se tuvo en cuenta la gravedad del distrés, ya que en la mayoría de historias clínicas no estaba recogida la escala de Silverman. Por otra parte, no se contempló si la alimentación se iniciaba o se alcanzaba completa antes de la administración, ni la situación gasométrica previa.
En la serie analizada, los pacientes que recibieron surfactante antes de las 12h de vida mostraron mejor evolución. Se precisan más estudios, prospectivos y multicéntricos, con tamaños muestrales más grandes, que permitan establecer la verdadera utilidad de estos resultados y traten de solucionar todas estas limitaciones.
ConclusionesEn nuestra muestra de prematuros tardíos con SDR, la aplicación precoz de surfactante se ha relacionado con beneficios como la retirada rápida y mantenida del oxígeno suplementario y menor requerimiento de soporte respiratorio y estancia en UCIN. Además, ha reducido el desarrollo de complicaciones.
Por ello, es necesario la ampliación de estudios reglados para comparar los beneficios de la indicación precoz de surfactante en comparación con otras opciones de tratamiento en este rango de edad gestacional.
Responsabilidades éticasEl proyecto cuenta con el informe favorable para su realización por parte del Comité de Ética de la Investigación con medicamentos (CEIm) del Hospital (acta 8/2024). Se aceptó la exención de consentimiento informado dado el carácter retrospectivo y recogida de datos según práctica clínica habitual.
AutoríaEl Dr. Bartual es el investigador principal de este proyecto, siendo responsable del diseño del estudio, la recogida de datos, el análisis de los mismos y la redacción del presente artículo. La Dra. Vizcaíno ha formado parte activa del diseño del estudio y del análisis de datos, así como de la redacción del manuscrito. La Dra. Ferrández ha colaborado en el diseño del estudio y en la redacción del manuscrito.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Sociodemográficas
- –
Número total de pretérminos tardíos nacidos entre 2012-2020 en nuestra área
- –
Número de pretérminos tardíos de entre los nacidos diagnosticados de TTRN
- –
Número de pretérminos tardíos de entre los nacidos diagnosticados de SDR con y sin necesidad de surfactante
- –
Año de recogida
- –
Distribución por edad gestacional: 340/7 - 346/7/350/7 - 356/7/360/7 - 366/7
- –
Sexo: varón/mujer
- –
Embarazo gemelar: sí/no
- –
Crecimiento intrauterino retardado: sí/no
- –
Corticoides prenatales: sí/no
- –
Tipo de parto: eutócico/instrumentado/cesárea
- –
Peso al nacimiento
- –
Traslado de otro hospital: sí/no
Asistencia respiratoria
- –
Reanimación con VPPi durante el parto: sí/no
- –
Tipo de soporte respiratorio durante el traslado: VNI/VMI
- –
Horas de vida al inicio de VNI
- –
Tipo de ventilación mecánica previa a la administración de surfactante: CPAP/VPPIn/VMI
- –
PEEP recibida en caso de VNI
Administración de surfactante
- –
FiO2 que precisaba previa al surfactante
- –
Horas de vida en el momento de la administración de surfactante
- –
Modo de administración de la primera dosis de surfactante: LISA/tras IOT
Evolución
- –
Redosificación: sí/no
- –
Días de VNI tras surfactante
- –
Días de VMI tras surfactante
- –
Días de soporte respiratorio total tras surfactante (VNI, VMI, oxigenoterapia de alto y bajo flujo)
- –
Días con FiO2>0,21 tras primera dosis de surfactante
- –
Horas que tarda el paciente en alcanzar FiO2 0,21 tras la primera dosis de surfactante: <1h/2-12h/13-24h/25-48h/>48h
- –
Días de hospitalización en la UCIN
- –
Días de hospitalización totales
Complicaciones:
- –
Neumotórax: sí/no
- –
DBP: sí/no
- –
DAP: sí/no
- –
Exitus: sí/no