La ventilación mecánica prolongada (VMP) en las unidades de cuidados intensivos pediátricos (UCIP) está aumentando debido a los avances sanitarios y a criterios éticos que favorecen la supervivencia de los niños con enfermedades crónicas. Estos pacientes utilizan numerosos recursos sanitarios, generan alta demanda familiar y presentan riesgo elevado de complicaciones y mortalidad. Entre las enfermedades de base más frecuentes están las enfermedades respiratorias crónicas, neuromusculares, prematuridad, displasia broncopulmonar o cardiopatías, emergiendo en los últimos años la enfermedad oncológica.
En la UCIP, la VMP se realiza principalmente mediante ventilación mecánica invasiva (VMI) con tubo endotraqueal o traqueostomía (TQ), siendo menos frecuente la ventilación no invasiva (VNI). La retirada exitosa de la ventilación requiere estrategias encaminadas a identificar y corregir factores que alteran el equilibrio entre la carga del sistema respiratorio y la capacidad de trabajo respiratorio. Tanto la TQ como la VNI pueden facilitar el destete ventilatorio o ser soluciones para ventilación a largo plazo.
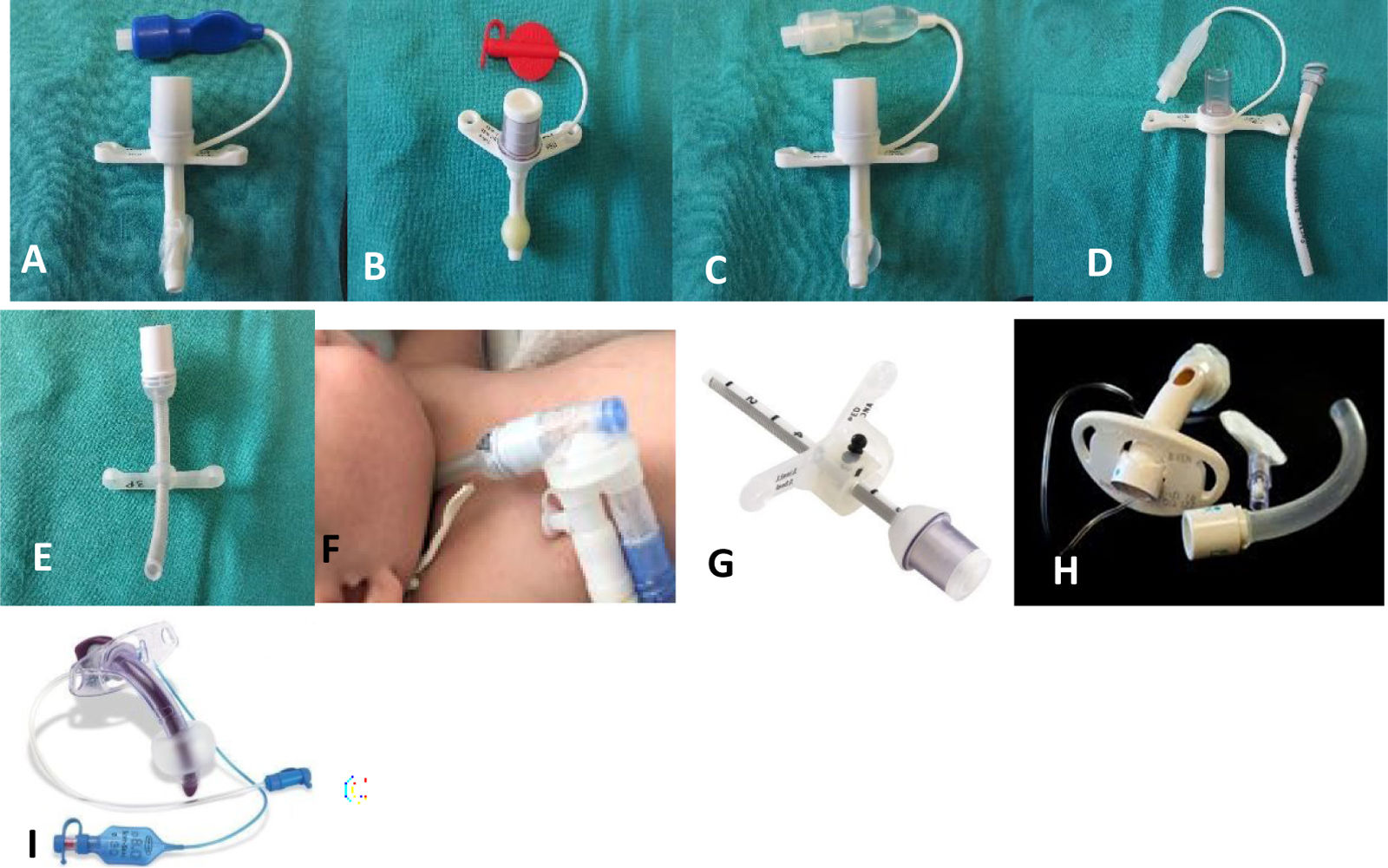
No existe un momento óptimo definido para realizar una TQ en niños; esta decisión debe ser individualizada valorando riesgo-beneficio de cada alternativa. En niños la TQ suele demorarse mucho más que en adultos. En pediatría se utilizan cánulas de una sola pieza; además, si existe estabilidad clínica y posibilidad de conexión a respirador domiciliario, se deben priorizar las cánulas sin balón, por su mejor tolerancia y seguridad.
La ventilación domiciliaria permite el retorno al entorno familiar, mejorando la calidad de vida y favoreciendo el neurodesarrollo. Sin embargo, la ayuda institucional puede ser insuficiente para afrontar la alta responsabilidad y carga asumidas por las familias.
Prolonged mechanical ventilation (PMV) in paediatric intensive care (PICU) is increasing due to health advances and ethical criteria favouring the survival of chronically ill children. These patients require resources, generate high family demand and present a high risk of complications and mortality. Among the most frequent underlying pathologies are chronic respiratory diseases, neuromuscular diseases, prematurity, bronchopulmonary dysplasia and heart disease, with oncological pathology emerging in recent years.
In PICU, PMV is mainly performed by invasive MV with an endotracheal or tracheostomy tube (TQ), with non-invasive ventilation (NIV) being less frequent. Successful weaning from MV requires strategies aimed at identifying and correcting factors that alter the balance between respiratory system load and respiratory work capacity. Both TQ and NIV can facilitate ventilatory weaning or be solutions for long-term ventilation. There is no defined optimal time to perform TQ in children; this decision should be individualised on a risk-benefit basis. TQ tends to be delayed in children much longer than in adults. One-piece cannulae are used in paediatrics; in addition, if there is clinical stability and the possibility of connection to a home ventilator, uncuffed cannulae should be prioritised because of their better tolerance and safety. Home ventilation allows for a return to the home environment, improving quality of life and favouring neurodevelopment. However, institutional support can be insufficient to cope with the high responsibility and burden assumed by families.
Artículo
Diríjase al área de socios de la web de la SEMICYUC (www.semicyuc.org ) y pulse el enlace a la revista.