Evaluar las diferencias observadas en la determinación de los iones y del anión GAP obtenidos por gasometría (POC) y por bioquímica de laboratorio, y analizar los posibles errores en función de los límites de normalidad.
Material y métodosEstudio descriptivo transversal retrospectivo para valorar la concordancia entre dos pruebas diagnósticas de los pacientes ingresados en la Unidad de Reanimación del Complexo Hospitalario Universitario de Ourense, entre julio y noviembre de 2015, con al menos una determinación coincidente de bioquímica y POC. Se excluyeron pacientes menores de 18años.
ResultadosSe analizaron 1.073 muestras. Coeficientes de correlación de concordancia de Lin en sodio, potasio y cloro de 0,87, 0,84 y 0,72, respectivamente. Concordancia kappa de los límites de normalidad para sodio, potasio y cloro de 0,63, 0,74 y 0,32. Pobre correlación del anión GAP y nula concordancia entre el POC y el calculado por la bioquímica, incluido el corregido por albúmina.
ConclusionesConcordancia pobre entre los iones de la bioquímica y la gasometría, por lo que no son intercambiables. Concordancia kappa con los límites de normalidad buena para el sodio y potasio, y débil para el cloro. Posible validez para una orientación en la clasificación dentro de los límites de los iones, excepto para el cloro. Nula concordancia para el anión GAP, incluso el corregido por albúmina.
To evaluate the differences observed in ion and GAP anion determinations obtained by point-of-care (POC) blood gas versus laboratory biochemical testing, and to analyze the possible errors according to the limits of normality.
Material and methodsA descriptive, cross-sectional retrospective study was made to assess concordance between two diagnostic tests in patients admitted to the Critical Care Unit of Ourense University Hospital Complex (Spain), between July and November 2015, involving at least one coinciding biochemical test and POC determination. Patients under 18years of age were excluded.
ResultsA total of 1,073 samples were analyzed. Lin's concordance correlation coefficients for sodium, potassium and chlorine were 0.87, 0.84 and 0.72, respectively. Kappa concordance of the normality limits for sodium, potassium and chlorine was 0.63, 0.74 and 0.32. The results indicated poor correlation of the anion GAP and null concordance between POC and biochemical testing, including the value corrected for albumin.
ConclusionsPoor concordance was observed between the ion values as determined by biochemistry and blood gases; the two methods are therefore not interchangeable. Kappa agreement with normality limits was good for sodium and potassium, and weak for chlorine. Possible validity was noted in orienting the classification within the ion limits, with the exception of chlorine. No agreement was recorded in relation to the anion GAP, even that corrected for albumin.
En las UCI europeas, la extracción diaria de sangre con fines diagnósticos se sitúa entre los 40 y los 80ml1,2, esto es, se extrae el equivalente a un concentrado de hematíes cada 7-10días. Para intentar reducir estas pérdidas y disminuir los tiempos de espera, es usual el empleo de muestras gasométricas que, en menos tiempo y con menos cantidad de sangre, nos ofrecen el equilibrio ácido-base, la cifra de hemoglobina y los iones básicos del paciente.
El empleo de métodos de diagnóstico rápido, como la gasometría a pie de cama (point-of-care [POC]), presenta ventajas en cuanto a la disponibilidad y al acortamiento de tiempo, ya que el procesamiento completo de las muestras por el laboratorio central puede alargar la disponibilidad de resultados 60-90min3 en situaciones urgentes, mientras que el uso de muestras gasométricas acorta la fase analítica a unos escasos minutos. Además del tiempo, minimiza el procesamiento preanalítico y el volumen de sangre necesaria para el análisis4.
La determinación de hemoglobina y de iones en la gasometría puede llevar a la toma de decisiones erróneas. Hay múltiples estudios que demuestran diferencias clínicas entre el POC y el laboratorio central tanto en la hemoglobina5 como en los iones6-9, aunque también hay estudios que no encuentran tales discrepancias10.
Nuestra hipótesis de trabajo fue que hay diferencias en las determinaciones de los iones obtenidos mediante gasometría y los obtenidos mediante el laboratorio central, y que dichas diferencias se aprecian también en el anión GAP. Nuestra hipótesis nula fue que no hubo dichas diferencias, existiendo concordancia entre los dos métodos de medición. Por ello, nos propusimos evaluar las diferencias observadas en ellos y analizar los posibles errores en función de los puntos de corte de normalidad.
En caso de tener una buena concordancia, nos permitiría evitar pruebas innecesarias, disminuyendo no solo el volumen de sangre a utilizar, sino los gastos y los riesgos derivados del proceso de extracción sanguínea.
Pacientes y métodosSe diseñó un estudio descriptivo transversal para valorar la concordancia entre dos pruebas diagnósticas en las determinaciones de los iones obtenidos mediante gasometría y los obtenidos mediante laboratorio central. Se planteó realizarlo de manera retrospectiva en los pacientes ingresados en la Unidad de Reanimación del Complexo Hospitalario Universitario de Ourense. Con el código 2016/408 se registró el protocolo de investigación en el Comité de Ética de la Investigación de Pontevedra-Vigo-Ourense, siendo aprobado por el mismo. Tras esto, fue aceptado para su realización por la Dirección Gerencia del citado Complexo Hospitalario.
Se seleccionaron los pacientes ingresados en la Unidad de Reanimación del Complexo Hospitalario Universitario de Ourense entre julio y noviembre de 2015. Se incluyeron aquellos en los que se constató que tenían al menos una determinación simultánea de iones en gasometría y bioquímica. Se excluyeron los pacientes menores de 18años. Las muestras fueron extraídas en la Unidad de Reanimación y enviadas al laboratorio central a través de un sistema de transporte de tubo neumático.
Los objetos de medida fueron los iones determinados por POC y por bioquímica convencional. Para ello se recogieron los resultados de las muestras de gasometría arterial y bioquímica, que se analizaron de forma simultánea mediante envío al laboratorio central por un sistema de transporte neumático.
El dispositivo utilizado para la medición de las muestras de gasometría fue el Siemens Rapidlab 1265 (Siemens Healthcare GmbH, Henkestr. 127, 91052 Erlangen, Alemania), mientras que el equipo utilizado para determinar la bioquímica fue Roche cobas 6000, compuesto por cobas c501 y Roche cobas e601 (Roche Diagnostics International Ltd, CH-6343 Rotkreuz, Suiza).
Se recogieron las siguientes variables: edad, sexo, motivo de ingreso (traumático o no), APACHEII, iones en la gasometría arterial (sodio [Na], potasio [K], cloro [Cl], HCO3, anión GAP), iones en la bioquímica (Na, K, Cl) y albúmina.
Los informes de laboratorio documentados como muestra inadecuada, coagulada, volumen insuficiente… fueron descartados de la evaluación como error en la fase preanalítica. Si el paciente evaluado no tenía ninguna analítica válida, los datos recogidos referentes al mismo fueron eliminados del estudio.
Para el anión GAP calculado se utilizó la fórmula con potasio, que es la misma que emplea la máquina de gases11, siendo obtenido a partir de los iones de la bioquímica y del bicarbonato de la gasometría.
Para el anión GAP corregido por albúmina se utilizó la siguiente fórmula:
Anión GAP corregido=anión GAP+0,25×(44−[albúmina (g/l)])
Los valores de referencia proporcionados por el informe de laboratorio para la bioquímica fueron: Na, 136-147; K, 3,5-5,1, y Cl, 98-110. Para la máquina de gases fueron: Na, 135-145; K, 3,3-4,6, y Cl, 96-111.
Para los análisis de concordancia se utilizó el coeficiente de correlación de concordancia de Lin y el método gráfico de Bland y Altman. También se obtuvieron los coeficientes kappa para la concordancia en los puntos de corte de normalidad. Para el cálculo del tamaño muestral, según el método de Bland-Altman, hemos utilizado el potasio por considerar el que menos margen de error nos permite. Nos fijamos un error tipoI del 0,01 y una potencia del 80%, asumimos12 una diferencia media de −0,3, una desviación estándar de 0,14 y permitimos una diferencia máxima de 0,6 entre ambos métodos, por lo que se necesitaron 1.026 muestras. Asumimos posibles errores por no cumplimentación en la recogida de datos del 5%, resultando 1.077 muestras a recoger. Previo a la realización de los exámenes estadísticos se comprobó la distribución normal de la muestra de cada uno de los parámetros a estudiar. Los datos fueron analizados con Libreoffice Calc para Linux 5.1.2.2, SPSS 15 para Windows y MedCalc 17.9 para Windows.
ResultadosSe recogieron un total de 1.077 muestras, de las cuales se eliminaron 4, quedando en total 1.073. La muestra sobre la que se realizó el estudio consta de 152 ingresos (102 hombres y 50 mujeres), 22 fallecimientos, un APACHEII medio de 15,53±6,99 y una edad media de 69,29±15,33, siendo 38 de origen traumático y 114 no traumático.
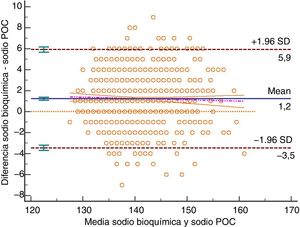
El método gráfico de Bland y Altman nos presenta un bias o error sistemático en todos los parámetros analizados. Se observan los análisis gráficos, en las figuras 1 a 5, para sodio, potasio, cloro, anión GAP y anión GAP corregido por albúmina, respectivamente. En la tabla 1 se exponen los resultados de los estudios de concordancia realizados.
Método gráfico de Bland y Altman para sodio bioquímica frente a sodio POC. Unidad de medición mmol/l. Desviación estándar 2,39, diferencia media 1,22 (1,08-1,36), límite superior concordancia 5,90 (5,65; 6,15), límite inferior concordancia −3,46 (−3,71; −3,21). Análisis en %: diferencia media 0,87% (0,77%; 0,97%), límite superior concordancia 4,20% (4,02%; 4,37%), límite inferior concordancia −2,46% (−2,63%; −2,28%). Intervalos de confianza del 95%. Se incluye la recta de regresión.
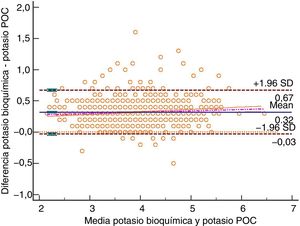
Método gráfico de Bland y Altman para potasio bioquímica frente a potasio POC. Unidad de medición mmol/l. Desviación estándar 0,18, diferencia media 0,32 (0,31; 0,33), límite superior concordancia 0,67 (0,65; 0,69), límite inferior concordancia −0,03 (−0,05; −0,01). Análisis en %: diferencia media 8,45% (8,16%; 8,74%), límite superior concordancia 17,91% (17,41%; 18,41%), límite inferior concordancia −1,01% (−1,51%; −0,51%). Intervalos de confianza del 95%. Se incluye la recta de regresión.
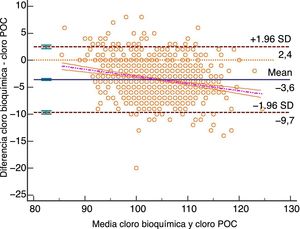
Método gráfico de Bland y Altman para cloro bioquímica frente a cloro POC. Unidad de medición mmol/l. Desviación estándar 3,09, diferencia media −3,61 (−3,80; −3,43), límite superior concordancia 2,45 (2,13; 2,77), límite inferior concordancia −9,67 (−9,99; −9,35). Análisis en %: diferencia media −3,43% (−3,61%; −3,26%), límite superior concordancia 2,37% (2,07%; 2,68%), límite inferior concordancia −9,24% (−9,55%; −8,93%). Intervalos de confianza del 95%. Se incluye la recta de regresión.
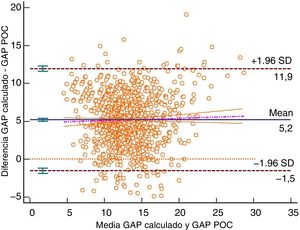
Método gráfico de Bland y Altman para el anión GAP calculado por bioquímica frente al anión GAP POC. Unidad de medición mmol/l. Desviación estándar 3,43, diferencia media 5,20 (4,99; 5,40), límite superior concordancia 11,92 (11,57; 12,28), límite inferior concordancia −1,53 (−1,89; −1,17). Análisis en %: diferencia media 42,93% (40,91%; 44,95%), límite superior concordancia 108,81% (105,31%; 112,31%), límite inferior concordancia −22,95% (−26,45%; −19,46%). Intervalos de confianza del 95%. Se incluye la recta de regresión.
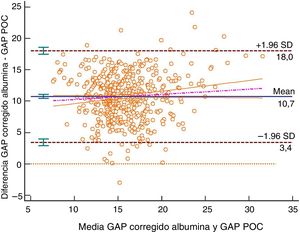
Método gráfico de Bland y Altman para el anión GAP calculado por bioquímica y corregido por albúmina frente al anión GAP POC. Unidad de medición mmol/l. Desviación estándar 3,72, diferencia media 10,72 (10,40; 11,04), límite superior concordancia 18,01 (17,46; 18,57), límite inferior concordancia 3,43 (2,87; 3,98). Análisis en %: diferencia media 71,30% (68,65%; 84,63%), límite superior concordancia 131,49% (126,91%; 136,08%), límite inferior concordancia 11,10% (6,52%; 15,68%). Intervalos de confianza del 95%. Se incluye la recta de regresión.
Datos de los estudios de concordancia entre los iones de gasometría y de bioquímica. Entre paréntesis, los intervalos de confianza del 95%
| Sodio (mmol/l) | Potasio (mmol/l) | Cloro (mmol/l) | GAP (mmol/l) | GAP corregido albúmina (mmol/l) | |
|---|---|---|---|---|---|
| N pares | 1.073 | 1.073 | 1.073 | 1.068 | 520 |
| Media gasómetro | 139,88 (139,56; 140,19) | 3,70 (3,66; 3,73) | 106,08 (105,71; 106,45) | 10,52 (10,30; 10,75) | 10,38 (10,06; 10,70) |
| Media bioquímica | 141,10 (140,79; 141,41) | 4,02 (3,98; 4,05) | 102,47 (102,14; 102,80) | 15,72 (15,49; 15,95) | 21,10 (20,78; 21,44) |
| Concordancia Lin | 0,87 (0,86; 0,89) | 0,84 (0,83; 0,85) | 0,72 (0,70; 0,75) | 0,30 (0,27; 0,33) | 0,11 (0,09; 0,13) |
Las tablas de contingencia según los límites de normalidad se muestran en las tablas 2 a 6 para sodio, potasio, cloro, GAP y GAP corregido por albúmina, respectivamente. El coeficiente kappa de Cohen13, para los límites establecidos, es bueno para el sodio y el potasio, débil para el cloro, y pobre tanto para el GAP como con el GAP corregido por albúmina.
Tabla de concordancia de los valores del potasio determinado por bioquímica vs POC. Índice kappa 0,74 (0,70; 0,79), con un intervalo de confianza del 95%
| Potasio Bioq\Gases (mmol/l) | Bajo (< 3,3) | Normal (3,3-4,6) | Alto (> 4,6) |
|---|---|---|---|
| Bajo (< 3,5) | 170 | 9 | 0 |
| Normal (3,5-5,1) | 72 | 752 | 22 |
| Alto (> 5,1) | 0 | 6 | 42 |
Tabla de concordancia de los valores del anión GAP bioquímica corregido por albúmina vs POC. Índice kappa −0,07 (−0,12; −0,03), con un intervalo de confianza del 95%
| GAP Bioq Alb\POC (mmol/l) | Bajo (< 10) | Normal (10-20) | Alto (> 20) |
|---|---|---|---|
| Bajo (< 10) | 0 | 0 | 0 |
| Normal (10-20) | 140 | 90 | 0 |
| Alto (> 20) | 106 | 182 | 2 |
Lo ideal hubiese sido realizar un estudio prospectivo con más mediciones de control para poder identificar errores, pero creemos que la metodología empleada y el número de muestras evitan el error de introducir el sesgo de evaluación en el análisis, pareciéndose más a un entorno de trabajo real. Hay muchos factores que no se pueden controlar cuando se realizan de forma retrospectiva, pero nos permiten tener una visión real de los resultados del proceso.
Trabajar con múltiples determinaciones por sujeto14, o con un número de determinaciones por sujeto no homogéneo15, puede llevar a un sesgo en la interpretación de los resultados (sobre todo en base a la desviación estándar y los límites de confianza). Nosotros consideramos que el sujeto varía durante su estancia en críticos, bien por mejoría o por empeoramiento, por lo que no podemos asumir que la varianza intrasujeto sea constante, siendo requisito para la utilización de los métodos corregidos de Bland y Altman, motivo por el cual no hemos usado dicho método de análisis.
A nivel de concordancia, los resultados son pobres para los tres iones, pues el coeficiente de correlación de concordancia de Lin es pobre16. Examinando el análisis de Bland y Altman, el intervalo de confianza de las medias de las diferencias no incluye al valor cero, por lo que pueden existir diferencias estadísticamente significativas entre ambas mediciones, siendo los resultados de los equipos no intercambiables, existiendo un error sistemático constante y proporcional entre ambos métodos diagnósticos17.
Otra cuestión es la aplicación práctica de los resultados. El análisis de Bland y Altman solo define los intervalos de acuerdo, no dice si esos límites son clínicamente aceptables o no18. Si asumimos una discrepancia máxima de las muestras de ±5%, teniendo que puede no ser válida en todos los pacientes y/o en todas las situaciones19, los resultados mostrados nos informan que los valores del sodio podrían ser utilizados de forma indistinta por ambos métodos, mientras que los valores del potasio o del cloro no deberían ser utilizados indistintamente para dicho nivel de discrepancia.
Muchas veces nos interesa saber si los iones están en rango de normalidad o no. En cuanto a las anomalías para los puntos de corte de normalidad, la concordancia de la medición con las máquinas de gasometría es buena para el sodio y el potasio, mientras que el cloro presenta un nivel de concordancia débil. Por tanto, nos valdría para orientación de valores en los dos primeros.
Para el anión GAP tenemos una baja concordancia, aunque no esperábamos que el índice kappa fuese negativo, lo que indica que es más fiable el azar que la relación entre ambas pruebas. Las diferencias en su interpretación pueden complicar la orientación diagnóstica, pero dicho análisis queda fuera de los límites del presente estudio. La correlación entre el anión GAP del POC y el anión GAP corregido por albúmina arrojó peores resultados que con el GAP normal. En el presente estudio no hemos realizado otro tipo de correlaciones, como el anión GAP corregido por albúmina y fosfato, ni con otros métodos de aproximación al equilibrio ácido-base. Los resultados del anión GAP por uno y otro método concuerdan con lo recogido en la literatura20.
La utilización del tubo neumático puede llevar a un grado mayor de hemólisis, sobre todo en el potasio21. En nuestro caso, el potasio no fue la peor concordancia encontrada, y aunque la misma fue pobre, no encontramos alteraciones sugestivas de hemólisis.
Aunque se conoce que los cambios en el tipo de jeringa con heparina pueden alterar la validez de las muestras6,22, no tuvimos constancia de cambio de material, utilizándose jeringas de heparina seca. Aunque la heparina eléctricamente balanceada puede introducir un error sistemático en la medición de los iones positivos23, este no parece que sea el error sistemático en nuestro caso, pues el peor resultado de todos es con un ion negativo, el cloro.
Además, la extracción de muestras no fue protocolizada, y aunque gran parte de las analíticas recogidas corresponden a la primera hora de la mañana, hay también analíticas de otras horas del día. Esto también puede generar discrepancias en los resultados, tanto por la disponibilidad de personal como por el momento horario del día. Sin embargo, a pesar de que pueda interpretarse como una limitación, creemos que puede ser una fortaleza al cubrir más horario y personal que en condiciones ideales.
Gran parte de los pacientes poseían una línea arterial, realizándose la extracción de forma simultánea. Sin embargo, esto no ocurre en todos los casos, bien por falta del catéter arterial o por malfuncionamiento de este. El punto y la forma de extracción de las muestras no quedan reflejados en el informe de laboratorio. Este podría ser uno de los puntos a analizar, pero no deberíamos poner solamente el foco en la extracción, pues estudios reglados10,24 también presentan resultados dispares.
Debemos tener en cuenta que los analizadores de gases presentan, además de la rapidez, otra serie de ventajas. No se afectan por los niveles de proteína sérica en sus mediciones de electrólitos25, siendo recomendables en casos de hipoalbuminemia25-29. No consideramos que la hipoalbuminemia presente en los pacientes críticos pueda explicar por sí sola los pobres resultados de concordancia obtenidos. El ion sodio es el más estudiado en la literatura en este aspecto, con una diferencia mayor en casos de hipoalbuminemia25,29 que la obtenida en nuestro estudio.
En conclusión, obtuvimos una concordancia pobre, por lo que ambas pruebas, en nuestro caso, no son intercambiables. Sin embargo, atendiendo a los límites de normalidad, la concordancia fue buena para el sodio y el potasio, y débil para el cloro. Ello nos anima a utilizar dichos resultados para una orientación dentro de los límites de los iones, excepto para el cloro, aunque no para el valor per se. Nula concordancia entre el anión GAP del POC con el calculado a partir de la bioquímica.
Contribución de los autoresAngel López: concepción y diseño del estudio, adquisición de datos, análisis e interpretación de los datos, borrador del artículo, aprobación definitiva.
Beatriz García: adquisición de datos, revisión crítica del contenido intelectual, aprobación definitiva de la versión que se presenta.
Ana Gómez: adquisición de datos, revisión crítica del contenido intelectual, aprobación definitiva de la versión que se presenta.
Laura González: adquisición de datos, revisión crítica del contenido intelectual, aprobación definitiva de la versión que se presenta.
Nerea González: adquisición de datos, revisión crítica del contenido intelectual, aprobación definitiva de la versión que se presenta.
Luis Martín: adquisición de datos, revisión crítica del contenido intelectual, aprobación definitiva de la versión que se presenta.
Gabriel Jaime: concepción del estudio, análisis e interpretación de los datos, revisión crítica del contenido intelectual, aprobación definitiva de la versión que se presenta.
Conflicto de interesesNo se declaran conflictos de intereses.
Se agradece a los integrantes del grupo de investigación «Anestesia y Cuidados Críticos» la ayuda prestada.