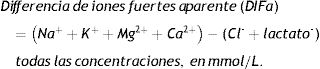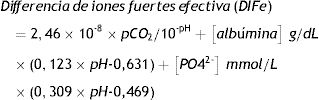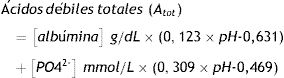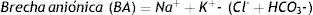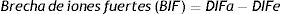Evaluar el impacto de la infusión de lactato de sodio 0,5M sobre variables del medio interno y sobre la presión intracraneana en pacientes críticos.
DiseñoEstudio prospectivo experimental de cohorte única.
ÁmbitoUnidad de cuidados intensivos de un hospital universitario.
PacientesPacientes con shock y neurocríticos con hipertensión intracraneana.
IntervencionesSe infundió una carga de 500 cc de infusión de lactato de sodio 0,5M en 15 min y se midió el nivel plasmático de sodio, potasio, magnesio, calcio, cloro, lactato, bicarbonato, PaCO2 arterial, pH, fosfato y albúmina en 3 tiempos: T0 preinfusión; T1 a los 30 min y T2 a los 60 min postinfusión. Se midieron la presión arterial media y presión intracraneana en T0 y T2.
ResultadosRecibieron el fluido N=41: n=19 como osmoagente y 22 como expansor. Se constató alcalosis metabólica: T0 vs. T1 (p=0,007); T1 vs. T2 (p=0,003). La natremia aumentó en los 3 tiempos (T0 vs. T1; p<0,0001; T1 vs. T2; p=0,0001). Se demostró un descenso de la presión intracraneana (T0: 24,83±5,4 vs. T2: 15,06±5,8; p <0,001). El lactato aumentó inicialmente (T1) con un rápido descenso (T2) (p <0,0001), incluso en aquellos pacientes con hiperlactatemia basal (p=0,002).
ConclusionesLa infusión de lactato de sodio 0,5M genera alcalosis metabólica, hipernatremia, disminución de la cloremia y un cambio bifásico del lactato, y muestra eficacia en el descenso de la presión intracraneana en pacientes con daño encefálico agudo.
To evaluate the impact of the infusion of sodium lactate 500ml upon different biochemical variables and intracranial pressure in patients admitted to the intensive care unit.
DesignA prospective experimental single cohort study was carried out.
ScopePolyvalent intensive care unit of a university hospital.
PatientsCritical patients with shock and intracranial hypertension.
ProcedureA 500ml sodium lactate bolus was infused in 15min. Plasma levels of sodium, potassium, magnesium, calcium, chloride, lactate, bicarbonate, PaCO2, pH, phosphate and albumin were recorded at 3timepoints: T0 pre-infusion; T1 at 30minutes, and T2 at 60minutes post-infusion. Mean arterial pressure and intracranial pressure were measured at T0 and T2.
ResultsForty-one patients received sodium lactate: 19 as an osmotically active agent and 22 as a volume expander. Metabolic alkalosis was observed: T0 vs. T1 (P=0.007); T1 vs. T2 (P=0.003). Sodium increased at the 3time points (T0 vs. T1, P<0.0001; T1 vs. T2, P=0.0001). In addition, sodium lactate decreased intracranial pressure (T0: 24.83±5.4 vs. T2: 15.06±5.8; P<0.001). Likewise, plasma lactate showed a biphasic effect, with a rapid decrease at T2 (P<0.0001), including in those with previous hyperlactatemia (P=0.002).
ConclusionsThe infusion of sodium lactate is associated to metabolic alkalosis, hypernatremia, reduced chloremia, and a biphasic change in plasma lactate levels. Moreover, a decrease in intracranial pressure was observed in patients with acute brain injury.
La fluidoterapia es parte fundamental del manejo terapéutico del paciente crítico. Sus objetivos principales son: la optimización de la perfusión tisular, la reposición de pérdidas insensibles y el mantenimiento de la homeostasis del medio interno1,2. La administración de un fluido actúa sobre el volumen y el contenido de los diferentes compartimentos corporales, variando la composición hidroelectrolítica, la tonicidad y el estado ácido-base. La fluidoterapia debe ser concebida como la administración de cualquier otro fármaco, considerando no solo sus efectos terapéuticos sino también sus efectos secundarios y los potenciales efectos adversos3.
En los últimos años ha emergido un volumen creciente de evidencia que muestra los efectos perjudiciales de la fluidoterapia, en particular, el impacto del aporte de soluciones no balanceadas (aquellas soluciones con una diferencia de iones fuertes in vivo de cero) que condicionan el desarrollo de hipercloremia4. Esto se ha observado en caso de aportes importantes y repetidos de solución salina normal (suero fisiológico) pero, con más frecuencia, en forma más precoz y con mayor severidad con el uso de soluciones salinas hipertónicas (3%; 7,5%; 10%, etc.), las cuales actualmente forman parte de la rutina como forma inicial de control de la hipertensión intracraneana y también en la corrección de la hiponatremia asociada a síndromes perdedores de sal5.
En modelos de experimentación animal se ha demostrado que la presencia de hipercloremia secundaria a fluidoterapia genera un efecto proinflamatorio6,7, así como alteraciones de la hemodinamia intrarrenal, con vasoconstricción y caída del filtrado glomerular8. Por su parte, diversos estudios clínicos observacionales permiten establecer una asociación entre la hipercloremia y el desarrollo de daño renal9, así como un aumento significativo de la mortalidad en diferentes grupos de pacientes críticos10-12. Esta alteración de la función renal generada por la hipercloremia estaría en la base de la retención hidrosalina, del balance hídrico positivo13 y de la expansión del espacio extracelular, que es la regla de los pacientes en la unidad de cuidados intensivos (UCI) y que ha sido señalada también como un factor pronóstico en diversos estudios observacionales14,15.
Debido a estos problemas, se han explorado nuevas soluciones hidroelectrolíticas a los efectos de minimizar el desarrollo de hipercloremia, así como de limitar el balance positivo de fluidos en el paciente crítico. Con este marco, aparece en escena la solución de lactato de sodio hipertónico (LSH) en diversos modelos experimentales16-19 y en ensayos clínicos sobre poblaciones heterogéneas de pacientes críticos, entre los cuales se destacan el postoperatorio de cirugía cardíaca20-22, el shock séptico, la falla cardíaca aguda23 y grandes quemaduras24. Un lugar especial le cabe al LSH para el paciente neurocrítico agudo, en virtud de sus efectos como osmoagente25,26 así como por su capacidad para ser utilizado como sustrato energético para el encéfalo dañado27-29.
Sin embargo, debido a su composición hidroelectrolítica y osmolaridad, el LSH 0,5M (tabla 1) dista mucho de ser una solución balanceada: es capaz de alterar de modo significativo diversas variables del medio interno.
El objetivo primario del presente estudio ha sido evaluar el impacto de la infusión de una dosis de 500 cc de LSH 0,5M sobre diferentes variables bioquímicas del medio interno en una población heterogénea de pacientes críticos. El objetivo secundario fue evaluar el impacto de la administración del LSH sobre la presión intracraneana en la subpoblación de pacientes con daño neural e hipertensión intracraneana.
Pacientes y métodosEs un estudio clínico experimental, prospectivo, unicéntrico, realizado en el Centro de Tratamiento Intensivo del Hospital de Clínicas de la Facultad de Medicina (Universidad de la República del Uruguay), entre los meses de marzo del año 2017 y setiembre de 2018. La UCI de adultos del Hospital de Clínicas de Montevideo se localiza en un hospital de tercer nivel y cuenta con 11 camas polivalentes.
Los criterios de inclusión fueron: ser paciente adulto (mayor de 18 años), requerir carga de fluido con 2objetivos: para el grupo 1, como expansor de la volemia en presencia de hipotensión arterial (presión arterial media [PAM] <65mmHg) y de clínica sugestiva de hipovolemia e hipoperfusión y con elementos predictores de respuesta a una «carga» de fluidos; para el grupo 2, como osmoagente en presencia de daño encefálico agudo de causa traumática, vascular o postoperatoria con hipertensión intracraneana (presión intracraneana [PIC]>20mmHg o> de 15mmHg en aquellos con lesión masa temporal, cisternas basales disminuidas o craniectomía descompresiva previa), una vez que fueron efectuadas las medidas inespecíficas para el control de la hipertensión intracraneana y con indicación de osmoterapia.
Para la administración de fluidos en el grupo 1 se establecieron 2 condiciones necesarias asociadas a la presencia de hipotensión arterial: a) elementos predictores de respuesta favorable a fluidos utilizando variables dinámicas (variación de la presión de pulso>13%; variación del volumen sistólico>10%; índice de distensibilidad de la vena cava inferior>15%) y b) elementos de hipoperfusión (lactato>2 mmol/L o saturación de O2 de la vía venosa central <70% o diuresis <0,5ml/kg por hora o tiempo de relleno capilar>3 segundos).
El tratamiento de la hipertensión intracraneana se encuentra protocolizado en nuestro servicio. Este consta de medidas inespecíficas (asistencia respiratoria mecánica, sedación y analgesia, correcta alineación y posicionamiento del paciente, tratamiento de la hipertermia, prevención de actividad epiléptica, control de la glucemia, estabilidad hemodinámica) y específicas, que se desarrollan en 3niveles. El primer nivel: drenaje de líquido cefalorraquídeo, uso de bloquentes neuromusculares, osmoterapia con LSH 0,5M en este caso, hiperventilación moderada (PaCO2 de 30mmHg); el segundo nivel: infusión de indometacina, hiperventilación intensa transitoria puntualmente para reducir un aumento de PIC (PaCO2 de 25mmHg) y tercer nivel: coma anestésico (propofol), hipotermia controlada moderada a 32-33°C, craniectomía descompresiva o drenaje lumbar. Todas estas medidas se suman en forma progresiva y escalonada hasta lograr un objetivo de PIC menor de 20mmHg (o 15mmHg en caso de descompresiva o lesión focal temporal no evacuada).
Los criterios de exclusión fueron: a) edad menor de 18 años; b) embarazo; c) daño renal agudo según los criterios Kidney Disease: Improving Global Outcomes (KDIGO)30; d) insuficiencia hepatocítica; e) hiponatremia (Na <135 mmol/L) y f) hipernatremia (Na> 155 mmol/L).
Protocolo de estudioLos pacientes elegibles recibieron la infusión intravenosa de una carga de LSH 0,5M (Laboratorio Fármaco Uruguayo, Uruguay) de 500 cc en 15 min, la cual fue administrada mediante un catéter venoso central. Las características bioquímicas de este cristaloide se resumen en la tabla 1.
Inmediatamente antes de la infusión del cristaloide (T0), se extrajo una muestra 5 cc de sangre de vía arterial, la cual fue utilizada para el análisis de gases en sangre (PaCO2, PaO2, pH, exceso de bases), así como para la medida de osmolalidad plasmática, iones (lactato, Cl-Na+, Ca2+ iónico, fosfato [PO42−], magnesio [Mg2+] y bicarbonato [HCO3−]) y albúmina. Una vez finalizada la infusión de LSH 0,5M, se realizaron nuevamente las mismas determinaciones a los 30 min (T1) y a los 60 min (T2) postinfusión. Antes de la infusión de LSH 0,5M (T0) y 60 min después (T2), fueron registrados los valores de PAM, así como las cifras de PIC y de presión de perfusión cerebral (PPC) en todos aquellos pacientes en los cuales el LSH 0,5M fue utilizado como osmoagente. Antes de su inclusión en el protocolo, los pacientes recibieron cloruro de sodio al 0,9% y cloruro de potasio como fluido de mantenimiento ajustado según balance hídrico y ionograma diario.
Procedimiento de análisis de las muestrasLos iones en sangre se procesaron de manera inmediata por el método de electrodos selectivos para iones Na+, K+, Ca2+ y Cl- a través del Analizador ABL Flex 835 (Radiometer). A partir de la misma muestra se obtuvieron los valores correspondientes a pO2, pCO2, pH, HCO3-, exceso de bases y lactato.
Se obtuvieron muestras en tubo de heparina de litio para analizar los valores de albúmina, PO42- y Mg2+. Fueron remitidas de forma inmediata al Laboratorio Central y centrifugadas dentro del plazo de 4 h de su extracción para obtener el plasma heparinizado; las muestras fueron procesadas con el Analizador Cobas C 311 (Roche Diangnostics).
A partir de la muestra de plasma heparinizado se realizó la medición de la osmolalidad a través del analizador Osmometer 3250 (Advanced Instruments), que utiliza método de descenso del punto de congelación.
Para el análisis fisicoquímico cuantitativo de los resultados se utilizó el enfoque fisicoquímico de Stewart modificado por Figge31, considerando los efectos de las proteínas plasmáticas. Las fórmulas utilizadas para los diferentes cálculos derivados fueron las siguientes:
Consideraciones éticasEl estudio se ha desarrollado siguiendo las recomendaciones de la Declaración de Helsinki sobre principios éticos para las investigaciones médicas en seres humanos.
Todos los registros fueron preservados por el investigador principal del estudio.
El protocolo de estudio fue aprobado por el Comité de Ética del Hospital de Clínicas de la Universida de la República y los consentimientos informados fueron completados por familiares antes de incluir a los pacientes en el estudio.
Análisis estadísticoLas variables cualitativas son expresadas como número absoluto y porcentaje. Las variables cuantitativas se expresan como media±desviación estándar (DE) o como mediana y rango intercuartílico (RIQ), según corresponda.
Las variables cuantitativas con distribución normal se compararon utilizando el test de t de Student para muestras dependientes en caso de 2medidas y el análisis de la varianza (test ANOVA) para medidas repetidas para las variables con más de 2medidas. En las que no se cumplieron los supuestos de normalidad, se aplicaron test no paramétricos: Wilcoxon para 2muestras y Friedman para más de 2. Se trabajó con una confianza estadística de 95% para un error αde 5%. Una p <0,05 fue considerada estadísticamente significativa.
ResultadosSe enrolaron 41 pacientes críticos, de los cuales 19 (46,3%) recibieron LSH 0,5M como osmoagente y 22 (53,7%) como expansor de la volemia. Fueron hombres 24 (58,5%). La media de edad fue de 50,9±3,1 años. La mediana de score APACHE II al ingreso a UCI fue 23 (17-26) y la mortalidad en UCI del 46,3%. La estancia en UCI fue de 18,3±3,2 días, en tanto que el tiempo de ventilación mecánica fue de 16,9±3,1 días. De los 19 pacientes que recibieron LSH por hipertensión craneal, 10 ingresaron por traumatismo craneoencefálico grave (CGS <8), de los cuales 3 requirieron craniectomía descompresiva, con una clasificación tomográfica (Traumatic Coma Data Bank) de II (4 pacientes), III (2 pacientes) y IV (4 pacientes). Un total de 12 pacientes ingresaron por sepsis; 4 pacientes ingresaron por politraumatismos graves, con un Injury Severity Score de 27,75±3,9. Las principales características demográficas y basales de los pacientes ingresados en el estudio se muestran en la tabla 2. Ningún paciente recibió cristaloides hipertónicos ni coloides antes de la realización del estudio. Aquellos pacientes que recibieron LSH 0,5M como agente osmótico lo hicieron a las 22,8±13,2 h del ingreso a la unidad, mientras que aquellos que lo recibieron como expansor lo hicieron a las 14,5±8,2 h del ingreso.
Características demográficas y basales de los pacientes previas a la intervención
| Características | |
| Hombres, n (%) | 17 (41,5) |
| Mujeres, n (%) | 24 (58,5) |
| Edad, media ± DE | 50,9±3,2 |
| APACHE II al ingreso a UCI | 23 (17-26) |
| ARM n (%) | 41 (100) |
| Estancia en UCI, media ± DE | 18,3±3,2 |
| Días de ARM, media ± DE | 16,9±3,1 |
| Mortalidad en UCI, n (%) | 19 (46,3) |
| Diagnóstico al ingreso n (%) | |
| Neurocríticos | 19 (46,3) |
| TECG | 10 (24,4) |
| HSA aneurismática | 3 (7,3) |
| Infarto cerebral | 3 (7,3) |
| Postoperatorio neuroquirúrgico (PEIC cirugía de coordinación) | 3 (7,3) |
| Sepsis | 12 (29,3) |
| Sepsis biliar | 2 (4,9) |
| Sepsis peritoneal | 9 (22) |
| Sepsis respiratoria (neumonía aguda comunitaria) | 1 (2,4) |
| Politraumatismos graves | 4 (9,7) |
| Posoperatorios complicados | 4 (9,7) |
| Posoperatorio de cirugía de aorta abdominal | 2 (4,9) |
| Cirugía ORL | 1 (2,4) |
| Esofagectomía | 1 (2,4) |
| Otros | 2 (4,9) |
| EPOC descompensada | 1 (2,4) |
| Intoxicación por metanol | 1 (2,4) |
| LSH 0,5M como osmoagente | 19 (46,3) |
| LSH 0,5M como expansor | 22 (53,7) |
Valores informados como números absolutos (n) y porcentaje (%).
Media±desviación estándar y mediana en rango intercuartílico.
ORL: cirugía otorrinolaringológica; PEIC: proceso expansivo intracraneano; UCI: unidad de cuidados intensivos
El efecto de la infusión del LSH 0,5M sobre el estado ácido-base mostró una alcalosis metabólica inmediata moderada, dado un ascenso del valor de pH (7,41±0,11 en T0 vs. 7,46±0,07 en T1; p=0,007 vs. 7,47±0,06 en T2; p=0,003), de la DIFa (34,00±5,61 en T0 vs. 37,72±4,08 en T1; p <0,0001 vs. 39,11±5,20 en T2; p <0,0001) (fig. 1). Por su parte, se constató un descenso de los Atot en T0 (6,15±3,58 vs. 5,628±3,85; p=0,032), que se mantiene en T1 (5,479±3,98; p=0,032) sin diferencia significativa entre T1 y T2. No se apreciaron modificaciones en el nivel de CO2 en sangre arterial.
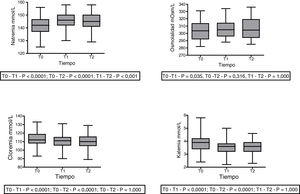
Con relación al impacto sobre los iones en sangre, se apreció una variación en el nivel de natremia en los 3 tiempos: 141,7±6,6 (T0) vs. 145,8±6,5 mmol/L (T1) con p <0,0001; 141,7±6,6 mmol/L (T0) vs. 145,1±6,9 mmol/L (T2) con p<0,0001; 145,8±6,5 mmol/L (T1) vs. 145,1±6,9 mmol/L (T2) con p=0,001. Por su parte, la osmolalidad mostró un aumento a los 30 min de la infusión (302,6±12,0 vs. 306,7; p=0,035), el cual se mantuvo sin diferencias entre los 30 y los 60 min (306,7±12 vs. 305,6±12,7; p=0,31) (fig. 2).
Se observó un descenso leve, estadísticamente significativo, del nivel de Cl- (113,3±8,5 vs. 110,5±7,8 vs. 110,225±7,859 mmol/L) y del catión K+ (3,84±0,6 vs. 3,54±0,5 vs. 3,54±0,5 mmol/L) en T1, que se mantuvo sin cambios en T2 (fig. 2). Los cambios en las variables bioquímicas se resumen en la tabla 3.
Curso evolutivo de los diferentes parámetros bioquímicos durante la observación del estudio
| T0 | T1 | T2 | p (T0 vs. T1) | p (T0 vs. T2) | p (T1 vs. T2) | |
|---|---|---|---|---|---|---|
| Sodio (mmol/L) | 141,7±6,5 | 145,7±6,5 | 145,1±6,8 | <0,0001 | <0,0001 | 0,001 |
| Potasio (mmol/L) | 3,8±0,6 | 3,5±0,5 | 3,5±0,5 | <0,0001 | <0,0001 | 1,00 |
| Mg2+ (mmol/L) | 0,51±0,11 | 0,48±0,12 | 0,49±0,10 | 0,195 | 0,582 | 0,723 |
| Ca2+ (mmol/l) | 1,07±0,17 | 0,99±0,14 | 1,01±0,19 | <0,0001 | 0,0002 | 0,473 |
| Cloro (mmol/L) | 113,3±8,5 | 110,5±7,8 | 110,2±7,8 | <0,0001 | <0,0001 | 1,00 |
| Lactato (mmol/L) | 1,5±1,4 | 4,5±2,5 | 3,07±2,18 | <0,0001 | <0,0001 | <0,0001 |
| Albúmina (g/dL) | 2,85±0,12 | 2,65±0,12 | 2,72±0,12 | 0,012 | 0,197 | 0,143 |
| PO42− (mmol/L) | 0,79±0,25 | 0,66±0,25 | 0,62±0,28 | 0,001 | 0,001 | 0,37 |
| Osmol (mOsm/L) | 302,6±12,0 | 306,7±12 | 305,6±12,7 | 0,035 | 0,316 | 1,00 |
| pH | 7,41±0,11 | 7,46±0,07 | 7,47±0,06 | 0,007 | 0,003 | 1,00 |
| HCO3 (mmol/L)a | 25,40±5,4 | 30,43±5,7 | 30,6±5,64 | <0,0001 | <0,0001 | 1,00 |
| pCO2 (mmHg) | 41,3±10,3 | 42,4±10,1 | 42,2±9,8 | 0,156 | 0,156 | 0,156 |
| BA (mmol/L) | 7,7±4,3 | 9,5±4,1 | 9,1±5,4 | 0,215 | 0,647 | 1,00 |
| DIFa (mmol/L) | 34,0±5,6 | 37,7±4,1 | 39,1±5,2 | <0,0001 | <0,0001 | 0,092 |
| Dife (mmol/L) | 32,0±6,16 | 36,0±5,45 | 36,1±5,9 | <0,0001 | <0,0001 | 1,000 |
| Atot (mmol/L) | 6,15±3,6 | 5,63±3,8 | 5,48±4,0 | 0,032 | 0,032 | 0,032 |
| BIF (mmol/L) | 1,95±4,6 | 1,77±4,4 | 3,04±6,18 | 1,00 | 0,394 | 0,215 |
Los datos se expresan como media±DE. Se realizó ANOVA para medidas repetidas en preinfusión (T0); a los 30 minutos de la infusión (T1), a los 60 minutos de la infusión (T2) en todas las variables excepto en lactato, PCO2 y Atot (test de Friedman).
Atot: ácidos totales débiles; BA: brecha aniónica; BIF: brecha de iones fuertes; DIFa: diferencia de iones fuertes aparente; Dife: diferencia de iones fuertes efectiva.
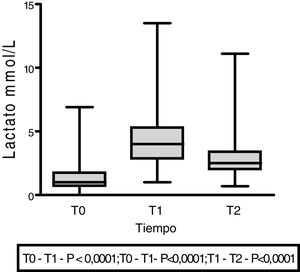
La variación en los niveles de lactato frente a su aporte como carga exógena mostró un ascenso inicial (1,5±1,4 en T0 vs. 4,5±2,5 en T1; p <0,001), con un descenso a los 60 min (3,07±2,18; p< 0,0001) (fig. 3).
Por otra parte, en 9 pacientes que tenían previamente a la infusión de LSH 0,5M una lactatemia>2 mmol/L, se comprobó un aumento del lactato plasmático de 3,67±0,53 (T0) vs. 7,23±1,13 mmol/L (T1) (p <0,015), con un descenso a los 60 min de 5,54±1,01 mmol/L (T2) (p=0,002) después de su infusión. En este mismo grupo se comprobó un aumento del pH arterial: 7,36±0,03 (T0) vs. 7,41±0,032 (T1) con p=0,108 y a 7,43±0,028 (T2) con p=0,01. El comportamiento del lactato y del pH en este grupo especial de pacientes son ilustrados en la figura 4. Los datos de pH, HCO3, brecha aniónica, PCO2, lactato y DIFa de este subgrupo se resumen en la tabla 4.
Evolución de parámetros del equilibrio ácido-base en pacientes con hiperlactatemia (lactato>2 mmol/L) previo a la infusión de LSH 0,5M
| T0 | T1 | T2 | p (T0 vs. T1) | p (T0 vs. T2) | p (T1 vs. T2) | |
|---|---|---|---|---|---|---|
| Lactato (mmol/L) | 3,66±1,61 | 7,29±3,40 | 5,55±3,04 | 0,015 | 0,230 | 0,002 |
| pH | 7,36±0,03 | 7,41±0,03 | 7,43±0,03 | 0,108 | 0,010 | 0,961 |
| PaCO2 mmHg | 39,1±6,3 | 42,4±11,1 | 41,8±8,2 | 0,361 | 0,254 | 1,000 |
| HCO3 mEq/L | 21,7±3,8 | 26,5±4,8 | 27,3±5,2 | 0,003 | 0,003 | 0,492 |
| Brecha aniónica | 11,4±5,8 | 14,0±6,1 | 12,6±7,5 | 0,500 | 1,000 | 0,173 |
| DIFa | 30,5±5,4 | 34,3±3,7 | 35,3±4,0 | 0,028 | 0,006 | 0,058 |
Los datos se expresan como media±desviación estándar.
El test ANOVA para medidas repetidas en varios momentos.
DIFa: diferencia de iones fuertes aparente; T0: valor preinfusión; T1: valor a los 30 minutos de la infusión; T2: valor a los 60 minutos de la infusión.
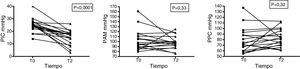
Las variaciones de la PIC mostraron un descenso significativo de los valores: 24,83±5,4 (T0) vs. 15,06±5,8 (T2) con p <0,001; por el contrario, no se apreciaron cambios en la hemodinamia sistémica de acuerdo con las variaciones de la PAM (88,4±20,7 en T0 vs. 90,3±14,4mmHg en T2; p=0,506) en la muestra total de pacientes ni en aquellos que recibieron LSH como osmoagente (103,2±20,7 vs. 98,4±13,0mmHg; p=0,33) (fig. 5). Los datos de PIC, PAM y PPC de los 19 pacientes que recibieron LSH como osmoagente pueden verse en la tabla 5.
Evolución de los valores de PAM, PIC, PPC en 19 pacientes que recibieron LSH 0,5M como osmoagente
| Preinfusión (T0) | Postinfusión (T2) | p | |
|---|---|---|---|
| PAM (mmHg) | 88,4±20,7 | 90,3±14,4 | 0,505 |
| PIC (mmHg) | 24,8±5,4 | 15,06±5,8 | <0,001 |
| PPC (mmHg) | 78,3±21,9 | 88,33±15,7 | 0,327 |
Los datos se ilustran como media±desviación estándar. Se realizó test de t para contraste de medias.
PAM: presión arterial media; PIC: presión intracraneana; PPC: presión de perfusión cerebral; T0: valor preinfusión; T2: valor a los 60 minutos postinfusión.
En el presente estudio hemos demostrado que la infusión de LSH 0,5M es capaz de modificar diferentes variables bioquímicas del medio interno, en especial, del equilibrio ácido-base y los iones en sangre. Respecto del estado ácido-base, el desarrollo de una alcalosis metabólica inmediata es la alteración característica. Esta puede ser explicada de acuerdo con la teoría fisicoquímica de Stewart, la cual se rige por los principios de electroneutralidad y conservación de masas32. De acuerdo con dicha teoría, el pH está regulado por 3 variables independientes: la diferencia de iones fuerte aparente (DIFa), la concentración de ácidos débiles totales (Atot) y la PaCO2 en sangre arterial31,32. Luego de la infusión del LSH 0,5M, este se disocia en sus 2iones fuertes principales, que son el sodio (catión) y el lactato (anión). El lactato ingresa rápidamente a la célula, donde es utilizado como sustrato energético, mientras que la carga de sodio permanece en el compartimento extracelular, lo cual determina un aumento de la DIFa. Este hecho, sumado al efecto dilutorio sobre los Atot encontrado en nuestro estudio, determina una disminución de la disociación del agua plasmática (fuente primaria de protones). Esta disminución de la concentración de hidrogeniones [H+] genera una alcalosis metabólica inicial y transitoria. La alcalosis metabólica secundaria a la infusión de LSH 0,5M podría tener efectos beneficiosos, en especial, sobre la contractilidad miocárdica y, en forma indirecta, sobre el volumen sistólico y el gasto cardíaco. En tal sentido, Nalos et al.23 encontraron una mejoría de la función cardíaca en pacientes con falla cardíaca con disfunción sistólica lo cual ha sido atribuido, al menos en parte, a los efectos de la alcalosis metabólica sobre la producción de catecolaminas endógenas23. Sin embargo, esta alcalosis metabólica podría tener efectos fisiológicamente negativos; por ejemplo, el desplazamiento a la izquierda de la curva de disociación de la hemoglobina, alterando de esta forma la liberación de oxígeno a nivel tisular.
Por otra parte, la administración del LSH 0,5M generó hipernatremia e hipocalemia, hallazgos que son concordantes con datos encontrados en estudios previos20,21,33. El incremento de la natremia es secundario a la carga de sodio administrada, lo cual provoca un aumento significativo de la osmolalidad plasmática; este hallazgo se explica porque el sodio es el esqueleto osmótico del compartimento extracelular y, por consiguiente, el principal determinante de la osmolalidad plasmática.
En nuestra serie, 19 pacientes con daño neural e hipertensión intracraneana recibieron LSH 0,5M, con una reducción significativa de la PIC a los 60 min de la infusión. Es importante aclarar que corresponde a una población de pacientes con daño neural de causa variada. Por otro lado, un porcentaje menor (n=3) presentaba una PIC menor a 20mmHg antes de la administración del LSH. Esta acción terapéutica puede ser considerada controversial. Un hecho que destacar en nuestra serie es que en 5 de los 19 pacientes se produjo un descenso de la PAM y, aunque concomitantemente también hubo un descenso de la PIC, este fue de una magnitud menor, lo que determinó que finalmente se produjera un descenso de la PPC. Estos cambios, algunos de los cuales son de gran magnitud, inciden claramente en que se pierda la significación estadística entre la administración de LSH y el eventual aumento de la PPC. Este hecho podría estar vinculado a un fenómeno de desactivación de la respuesta de Cushing (respuesta hiperadrenérgica secundaria a valores elevados de PIC> 30 y 40mmHg). Es lo que algunos autores han denominado Cushing en reversa y estaría asociado a reducciones rápidas y sustanciales de PIC. Nuestros resultados, junto a los reportados por Ichai et al.25, demuestran la efectividad de este cristaloide como osmoagente y sientan las bases para el desarrollo de futuros ensayos clínicos a mayor escala.
En nuestro estudio, el lactato mostró un comportamiento bifásico, con un ascenso significativo a los 30 min de la infusión, para luego descender a niveles preinfusión a los 60 min; este comportamiento podría ser secundario al desvío del lactato hacia el compartimento intracelular, donde sería utilizado como sustrato energético. Esto fue también observado en aquellos pacientes con hiperlactatemia (>2 mmol/l) previa a la infusión. Es interesante constatar que, si bien la lactatemia aumentó aún más en este grupo, la acidosis metabólica se redujo. El fenómeno podría ser considerado paradójico bajo una concepción clásica del metabolismo ácido-base. Pero la administración exógena de lactato bajo forma de lactato de sodio, su rápida captación celular y el consecuente incremento de la DIFa explican la alcalosis metabólica y dan sustento al enfoque de Stewart de metabolismo ácido-base.
Con relación al impacto sobre el cloro plasmático, la administración de LSH 0,5M produjo hipocloremia en nuestro estudio. La cloremia, de inicio elevada (como testimonio de reposiciones previas con soluciones con alto nivel de cloro) descendió levemente (casi un 3%) a los 30min y se mantuvo descendida a la hora, con un efecto hipocloremiante de la infusión. Resultados similares se observaron en trabajos en los cuales el LSH fue administrado en bolos25. Sin embargo, cuando el LSH se administra en infusiones prolongadas (24-48 h), parece que tiene un patrón bifásico respecto al nivel plasmático de cloro, con un descenso inicial y un aumento progresivo hasta alcanzar el nivel basal. No obstante, en la comparación con otros fluidos utilizados en dichos estudios (cloruro de sodio, lactato de Ringer), los niveles de cloro fueron significativamente menores23,26,33. Esta normalización de la cloremia después de una infusión mantenida prácticamente sin aporte de cloro sustenta la hipótesis de una fuente endógena de cloro determinada por la salida del anión desde el espacio intracelular buscando mantener la electroneutralidad después del ingreso de lactato a la célula34. A partir de este trascendental hallazgo, se ha planteado un mecanismo adicional del LSH como osmoagente en el control de la PIC, el cual sería consecuencia del aumento de la tonicidad plasmática secundario a un aumento de la natremia y al eflujo transcelular de cloro, que genera un «efecto arrastre» con disminución del agua y del volumen intracelular y, en consecuencia, el control de la PIC25,26.
La ausencia de desarrollo de hipercloremia durante la infusión de LSH podría ser clínicamente ventajosa, considerando que la hipercloremia ha demostrado ser perjudicial, en particular, en los pacientes neurocríticos en los que el uso de suero salino hipertónico ha surgido como la piedra angular del tratamiento de la hipertensión intracraneana35. Sin embargo, dado su alto nivel de cloro, produce hipercloremia rápidamente en su uso repetido. En este sentido, un número creciente de estudios observacionales han demostrado el efecto de la hipercloremia sobre la mortalidad de los pacientes neurocríticos, tal cual fue recientemente observado por Riha et al.36. Por su parte, Huang et al. señalaron la asociación entre la hipercloremia y el riesgo de muerte a los 30 días en pacientes con ataque cerebral isquémico y hemorragia intracraneana37. Asimismo, Sadan et al. reportaron una asociación entre el uso de suero salino hipertónico, hipercloremia y riesgo de fallo renal agudo en pacientes con hemorragia subaracnoidea38.
El presente es un estudio piloto que analiza una serie de casos, por lo cual presenta limitaciones. Es un estudio unicéntrico, con una población reducida de 2grupos heterogéneos de pacientes críticos, sin seguimiento temporal extendido, lo cual podría ayudar a una mejor comprensión y definición de la farmacocinética del LSH. Por lo mismo, no se observó la variación más alejada de la cloremia y del trastorno ácido-base. Finalmente, no hubo una monitorización hemodinámica y del metabolismo cerebral, lo cual habría brindado información con relación a los efectos del LSH 0,5M sobre el gasto cardíaco y el metabolismo cerebral.
ConclusionesEn pacientes con daño neural y shock, la infusión de LSH 0,5M se asoció al desarrollo de alcalosis metabólica mediante el aumento de la DIFa y la disminución de los Atot. Este efecto fue transitorio y estuvo vinculado a la aparición de hipernatremia, hiperosmolalidad e hipocloremia. El incremento significativo de la osmolalidad plasmática generó una disminución de la PIC, por lo que este fluido se comporta como un osmoagente efectivo. Sin embargo, dicho descenso, no se asoció a un aumento de la PPC. El nivel de lactato sigue un curso temporal bifásico con un descenso luego de un incremento inicial. Este comportamiento también fue observado en aquellos pacientes con hiperlactatemia previa a la infusión.
Creemos que, en el futuro próximo, se impone la realización de ensayos clínicos aleatorizados de fase III bien diseñados y con fuerza estadística suficiente, que utilicen al LSH 0,5M en diferentes grupos de pacientes críticos, y que es de particular interés el análisis comparativo con el cloruro de sodio hipertónico.
FinanciaciónEl estudio no ha recibido financiación.
Autoría/colaboraciónDr. Ignacio Aramendi: concepción y diseño del estudio, análisis e la interpretación de los datos, redacción del artículo y aprobación definitiva del manuscrito.
Dra. Alejandra Stolovas: adquisición de datos, análisis e interpretación de los datos, redacción del artículo y aprobación definitiva del manuscrito.
Dr. Sebastián Mendaña: adquisición de datos, análisis e interpretación de los datos, redacción del artículo y aprobación definitiva del manuscrito.
Dra. Anna Barindelli: concepción y diseño del estudio, revisión crítica del contenido intelectual y aprobación definitiva del manuscrito.
Dr. William Manzanares: concepción y diseño del estudio, análisis e interpretación de los datos, redacción del artículo y aprobación definitiva del manuscrito.
Dr. Alberto Biestro: concepción y diseño del estudio, análisis e interpretación de los datos, redacción del artículo y aprobación definitiva del manuscrito.
Conflicto de interesesLos autores declaran no tener conflicto de interés.