La parada cardiaca constituye uno de los mayores retos actuales, tanto por sus elevadas incidencia y mortalidad, como por ser causa de disfunción cerebral grave en más de la mitad de los supervivientes.
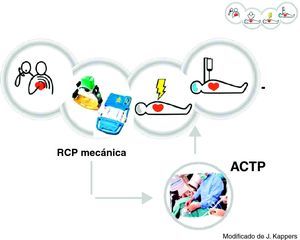
A partir de las líneas sugeridas por las Recomendaciones Internacionales en Resucitación (2005, 2010), se presenta como procedimiento integrado el Código Puente de origen coronario que, de acuerdo con unos estrictos criterios predictivos, permite: (1) Seleccionar a los pacientes en RCP refractaria con alta o muy alta presunción de causa coronaria, (2) Evacuar al paciente utilizando compresores torácicos mecánicos [LucasTM, Autopulse®] manteniendo las presiones de perfusión coronaria y cerebral, para (3) Conseguir acceso a la revascularización coronaria durante las maniobras de Resucitación (ACTP durante la RCP), así como (4) Inducir hipotermia precoz y (5) Cuidados intensivos postparada.
En caso de fracaso terapéutico, la calidad del soporte hemodinámico permite tender un segundo puente a la donación a corazón parado.
Cardiac arrest is one of the major current challenges, due to both its high incidence and mortality and the fact that it leads to severe brain dysfunction in over half of the survivors.
The so-called coronary origin Bridge Code is presented, based on the international resuscitation recommendations (2005, 2010). In accordance with a series of strict predictive criteria, this code makes it possible to: (1) select refractory CPR patients with a high or very high presumption of underlying coronary cause; (2) evacuate the patient using mechanical chest compressors [LucasTM, Autopulse®], maintaining coronary and brain perfusion pressures; (3) allow coronary revascularization access during resuscitation maneuvering (PTCA during ongoing CPR); (4) induce early hypothermia; and (5) facilitate post-cardiac arrest intensive care.
In the case of treatment failure, the quality of hemodynamic support makes it possible to establish a second bridge to non-heart beating organ donation.
La parada cardiaca (PC) en el medio extrahospitalario constituye uno de los mayores retos en el mundo occidental, estimando entre 400.000 y 700.0001 las muertes súbitas (MS) anuales en la Unión Europea y por encima de 350-450.000 en EE. UU. El 80% tienen lugar en domicilio, con una mortalidad próxima al 90% y grados variables de disfunción cerebral grave en más de la mitad de los supervivientes2. Para una incidencia de MS sobre 53/100.000 habitantes2, unos 40-50.000 pacientes sufren una PC extrahospitalaria en España.
A pesar de los nuevos avances, los porcentajes de supervivencia apenas han cambiado. En cuanto a pronóstico final, la variabilidad es la norma, publicando datos a menudo no comparables. Los datos más favorables para la supervivencia inicial oscilan entre 40 y 60%, con un rango de 5 a 20% de alta de hospital, con diferencias significativas en relación con modelos de asistencia y técnicas empleados3,4.
Compresiones torácicas externas: manteniendo la circulaciónDescrita la primera secuencia A-B-C (Airway, Breathing, Chest compressions) en la primera conferencia en Resucitación CardioPulmonar (RCP) en mayo de 1966, en las Recomendaciones 20055, International Liaison Committee on Resuscitation (ILCOR), American Heart Association (AHA) y European Resuscitation Council (ERC) sientan datos para sospechar que las interrupciones en las compresiones torácicas externas en la RCP podrían tener un efecto negativo en la supervivencia final. El verdadero respaldo de esta idea ha llegado en las Recomendaciones de 2010 que, en su versión AHA incluyen como clave del cambio el paso del A-B-C a la nueva secuencia C-A-B en el soporte vital básico tanto de adultos como de niños (excluidos neonatos)6.
Entre muchos datos que apoyan esta línea, un reciente metaanálisis7 describe cómo la RCP del testigo guiada por teléfono tiene una supervivencia del 14% [211/1.500] cuando solo se realizan compresiones vs. 12% [178/1.531] en el grupo convencional risk ratio RR 1, 22, 95%, IC 1,01-1,46], con un incremento absoluto en la supervivencia del 2-4% (95% IC 0,1-4,9), y un number needed to treat (NNT) de 41 (95%, IC 20-1.250).
Nuevas estrategias prácticas en RCPEn las Recomendaciones ILCOR 20055 y en las de 20106,8–10 se planteaba la posibilidad de prolongar la RCP teniendo en cuenta el estado previo del paciente, la causa de la PC -presenciada o no-, los tiempos «sin flujo», su calidad y la precocidad en iniciar tratamiento extracorpóreo en causas potencialmente reversibles (clase IIb), así como la existencia de circunstancias especiales: ahogamiento en agua helada, intoxicaciones, etc.11.
En los últimos años se han ensayado diferentes alternativas en las estrategias de RCP, entre ellas:
- 1.
La Resucitación Cardiocerebral (RCC), que evita la interrupción en la compresiones torácicas mejorando la supervivencia en PC extrahospitalarias12,13.
- 2.
Una variante, la Resucitación Cardiaca Mínimamente Interrumpida (RCMI)14 minimiza las interrupciones en las compresiones cardiacas registrando un aumento de la supervivencia de 1,8 a 5,4%.
- 3.
Un método de abordaje integral por objetivos descrito por Sunde et al.15,16 basado en hipotermia terapéutica, angioplastia coronaria transluminal percutánea (ACTP) urgente, soporte hemodinámico, control de glucemia, ventilación y convulsiones, que permite doblar la supervivencia (56 vs. 26%, Odds ajustada 4,47)15.
Tras décadas de experiencia, se vio necesario extender la cadena a los cuidados hospitalarios (quinto eslabón)16, elaborando el documento de consenso sobre el manejo del síndrome postparada cardiaca17,18 con especial atención a un enfoque global19–23 capaz de realizar un tratamiento etiológico de la causa que produjo la PC6 en especial, las técnicas de revascularización coronaria24–26.
Evidencias recientes confirman la importancia de la intensidad y profundidad de las compresiones torácicas, su frecuencia, liberación de la presión entre compresiones minimizando las interrupciones durante la RCP, la necesidad de evitar pausas antes y después de la desfibrilación evitando, igualmente, la hiperventilación del paciente al objeto de garantizar la eficacia optima de la resucitación10,21.
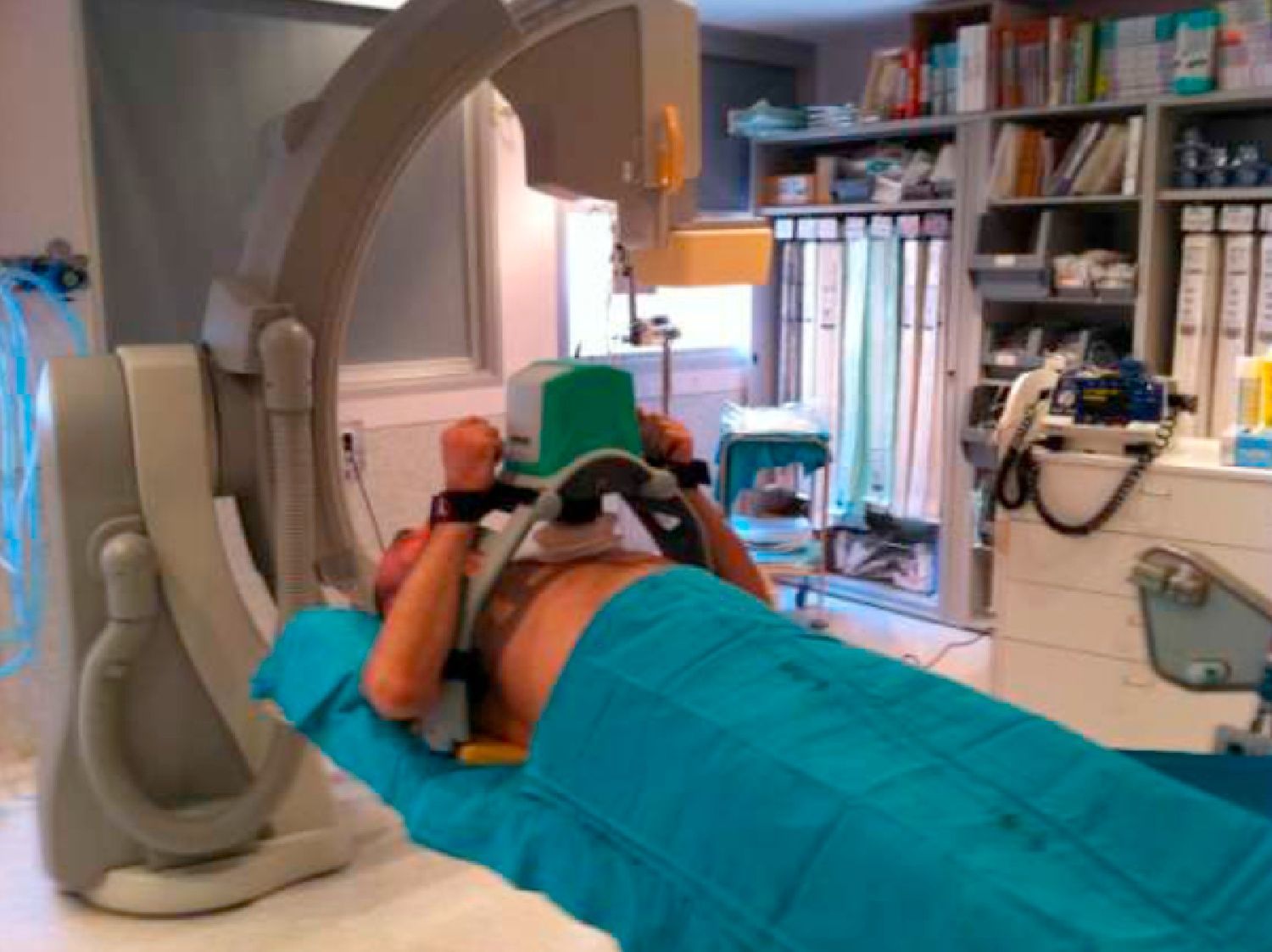
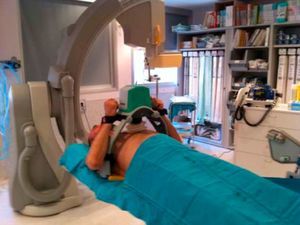
Los modernos compresores torácicos mecánicos (CTM) (fig. 1) presentan unas características mejoradas10,27 que se apoyan en series controladas con resultados más que aceptables en cuanto a eficacia clínica21 en ausencia de complicaciones y/o efectos secundarios de gravedad10. Tanto Autopulse® (Load-distributing LifeBand® -Zoll, Chelsmford, MA-) como Lucas™ 1 (Lund University Cardiac Arrest System) y Lucas™ 2 generan compresiones torácicas de forma continua y sin interrupciones, manteniendo tanto la presión de perfusión cerebral (fase de compresión) como, especialmente, la presión de perfusión coronaria (PPC) (fase de descompresión), principal factor determinante de la Recuperación de la Circulación Espontánea (RCE)21.
En el momento actual, el uso de CTM no se recomienda de rutina10, aunque su uso puede ser inestimable cuando la RCP manual resulta ineficaz: en la unidad de hemodinámica (UH), escáner, trasplante de órganos, traslado en camilla o en ambulancia/helicóptero (clase IIb, LOE C)28, etc.
Consideraciones sobre cardiología intervencionistaConsideraciones generales. Datos epidemiológicosEn ocasiones se olvida que los Síndromes Coronarios Agudos (SCA) no solo incluyen el Infarto Agudo de Miocardio (IAM) -con o sin elevación del segmento ST- y la angina inestable (AI), sino también la MS. Nuestro conocimiento actual sobre el substrato anatomopatológico de la lesión responsable del infarto de miocardio (ruptura vs erosión de placa aterosclerótica con trombosis asociada) proviene del estudio de pacientes que han presentado una MS. Por su frecuencia y gravedad, resulta fundamental descartar la afectación coronaria subyacente. La coronariografía urgente permite ofrecer una ACTP primaria que puede salvar la vida a pacientes comatosos tras una RCP prolongada que habitualmente presentan datos clínicos y electrocardiográficos no concluyentes29.
Para ilustrar esta idea, Dumas recoge en París los resultados de una cohorte de 714 pacientes recuperados tras PC30 en los que, tras descartar otras causas evidentes, 435 (61%) pacientes lo fueron de causa cardiaca. De ellos, 134 pacientes tenían elevación del ST, demostrada en el 96% por enfermedad coronaria de uno o más vasos, mientras de los restantes 301 pacientes, con otras alteraciones electrocardiográficas, de forma sorprendente, el 56% presentaba enfermedad de uno o más vasos, lo que igualmente justifica un manejo hemodinámico de este último grupo. En su estudio, la prevalencia global de enfermedad coronaria para los 435 pacientes es del 69,9%.
Si, como parece, la mayor parte de pacientes en PC lo son de causa coronaria, la reperfusión coronaria tendrá beneficios evidentes. Tanto en el documento de consenso de 200817,31 como en el estudio de Sunde15, hasta el 80% de los pacientes evacuados tras RCP acaban pasando por una UH en las primeras 24-72h26.
En nuestro país, la ACTP primaria ha crecido de forma espectacular en los últimos años27, aumentando el número de laboratorios que ofrecen ACTP primaria 24 horas al día, 7 días a la semana, realizada por equipos experimentados y dentro de unos tiempos puerta-balón aceptados por las actuales guías de práctica clínica27, a lo que ha contribuido la obligada coordinación con los Servicios de Emergencia Médica Extrahospitalaria, Urgencia Hospitalaria y Unidades Coronarias y de Cuidados Intensivos.
Sin embargo, todavía existen diferencias importantes en el número de ACTP primarias por millón de habitantes entre nuestras diferentes comunidades autónomas (rango 104 a 448, media española 302)27. Por este motivo, en coordinación con la Sociedad Europea de Cardiología, la Sociedad Española de Cardiología ha impulsado la estrategia stent for life27. A falta de datos fiables, se estima que el número total de Síndromes Coronarios Agudos con Elevación del Segmento ST (SCACEST) en España, se aproxima a los 45.00027, por lo que la actual estrategia de reperfusión tan solo llegaría al 20% de todos ellos, frente al 70% de pacientes que el programa stent for life se ha propuesto27.
El beneficio de la ACTP primaria sobre la fibrinólisis es todavía superior en pacientes de alto riesgo, en especial aquellos en shock cardiogénico y los que han sufrido una PC27. La RCP prolongada sería una contraindicación relativa para la trombolisis.
Contextos anatómicos especiales: enfermedad del tronco y afectación multivasoUna de las formas más graves en el seno del SCACEST, la enfermedad severa del tronco coronario izquierdo (TCI) puede ser la causa subyacente de IAM muy extensos con marcado compromiso hemodinámico que, a menudo, debutan como una PC y requieren RCP prolongada y medidas de soporte hemodinámico.
Hasta hace poco tiempo, el tratamiento del TCI no protegido se consideraba una indicación exclusivamente quirúrgica y electiva. En los últimos años, los avances en el intervencionismo coronario y la disponibilidad de stents farmacoactivos han condicionado que muchos pacientes con enfermedad del TCI se puedan beneficiar de una ACTP electiva32,33. En nuestro país, el intervencionismo en el TCI común no protegido ha experimentado un fuerte incremento, con 1.973 intervenciones en este contexto, lo que representa un incremento del 19% sobre el año anterior (2009 vs. 2008)27, con resultados similares a la cirugía coronaria32,33. De hecho, en el momento actual la estrategia de revascularización más frecuente en España para el TCI no protegido ya no es la cirugía coronaria sino la ACTP (Registro RENACIMIENTO, datos 2011 no publicados). Por otro lado, el tratamiento urgente de un SCACEST con un TCI pasa, de forma sistemática, por realizar una ACTP primaria, a pesar de su alto riesgo y necesidad de un adecuado soporte hemodinámico, En nuestro medio, la mortalidad de la ACTP de emergencia sobre el TCI es alta, especialmente en pacientes en situación de IAM y shock cardiogénico y en aquellos con enfermedad multivaso (EM) en los que no se logra una revascularización completa.
Por otra parte, más de la mitad de los pacientes con SCACEST tratados con ACTP primaria tienen EM severa34, porcentaje todavía mayor en pacientes con colapso o inestabilidad hemodinámica y en aquellos que presentan PC o arritmias ventriculares graves y recurrentes. A pesar del atractivo de tratar otras lesiones severas sobre otros territorios, una vez tratada con éxito la lesión culpable durante la ACTP primaria, múltiples estudios desaconsejan esta estrategia y sugieren el beneficio de adoptar una actitud conservadora34. Así, se recomienda obtener la revascularización completa en un procedimiento diferente, diferido de la fase aguda, bien durante el ingreso hospitalario o incluso de forma programada tras el alta hospitalaria34. La situación es radicalmente diferente en el contexto de un IAM con inestabilidad hemodinámica tras el tratamiento de la lesión culpable. Aunque la evidencia disponible todavía no es concluyente, en estos pacientes se recomienda valorar el tratamiento de otras lesiones coronarias severas en un intento de aliviar la isquemia asociada que podría desempeñar un papel relevante el deterioro hemodinámico del paciente35,36.
En pacientes con inestabilidad hemodinámica severa, arritmias persistentes y refractarias e, incluso en los primeros momentos, una actividad eléctrica sin pulso (AESP), una vez descartadas otras causas, el tratamiento de lesiones severas que afectan a territorios miocárdicos remotos, asociado a medidas de soporte hemodinámico y vital, puede ser la única esperanza de revertir un círculo vicioso que de otro modo será necesariamente fatal35,36.
Además, la estrategia de revascularización para conseguir de forma electiva una revascularización completa está siendo actualmente revisada34. Clásicamente, en pacientes estables postinfarto -tratados o no con fibrinolisis- se consideraba que la cirugía coronaria representaba la mejor opción terapéutica si existía enfermedad de 3 vasos y/o tronco con disfunción ventricular severa34. Con la generalización de la ACTP primaria, la lesión culpable del infarto ya ha sido tratada con éxito en la mayoría de los pacientes. En estos casos el tratamiento percutáneo electivo del resto de las lesiones (bien en la fase hospitalaria o bien de forma programada tras el alta) nos permite conseguir una revascularización completa34.
Inestabilidad hemodinámica y arrítmicaLos pacientes con IAM que tienen PC y precisan RCP, frecuentemente presentan una marcada inestabilidad hemodinámica y/o arrítmica.
El estudio SHOCK aleatorizó 302 pacientes con IAM a una estrategia de revascularización precoz (percutánea o quirúrgica) o a un tratamiento inicial agresivo médico para intentar estabilizar el cuadro clínico. A los 30 días la mortalidad por cualquier causa (objetivo primario) fue inferior (47 vs 56%) en el brazo asignado a revascularización precoz35, siendo estas diferencias favorables mantenidas hasta los 6 años35,36.
Por otra parte, el estudio SHOCK sugirió que el beneficio del intervencionismo se extendía más allá de 12 horas del comienzo del infarto aunque la precocidad de la intervención determinaba el pronóstico. Este estudio se realizó en un contexto histórico con muy baja utilización de stents y de inhibidores IIb/IIIa plaquetarios35,36 y no demostró beneficio en los pacientes mayores de 75 años, aunque sus resultados se siguen extrapolando a la práctica clínica actual.
Datos observacionales de nuestro país sugieren que, en comparación con series históricas, la ACTP primaria en el shock cardiogénico (balón de contrapulsación en el 79% de los pacientes, stents en el 76%, y ACTP multivaso en el 54%) permite mejorar los resultados de series históricas, con una supervivencia hospitalaria del 58%34.
Por otra parte, las arritmias ventriculares malignas representan la causa más frecuente de PC y posterior necesidad de RCP avanzada en el SCACEST37,38. Algunos estudios iniciales sugerían que, durante una ACTP primaria, tanto la incidencia como el pronóstico de estas arritmias sería mejor que el reportado en pacientes tratados con fibrinólisis. En el estudio PAMI la incidencia de Taquicardia Ventricular/Fibrilación Ventricular (TV/FV) fue de tan solo el 4,3%37. Estas arritmias se presentaron más frecuentemente en pacientes que no recibían betabloqueantes. Curiosamente, aunque los pacientes con TV/FV también tenían una mayor incidencia de bradiarritmias, hipotensión, necesidad de RCP y de intubación endotraqueal en el laboratorio de hemodinámica, en este estudio su presencia no afectó al pronóstico final37. El estudio APEX-AMI, analizó de una forma más completa y sistematizada, la presencia de arritmias ventriculares sostenidas malignas (TV/FV) antes, durante o después de la ACTP primaria en un total de 5.745 pacientes38. En este estudio la incidencia de arritmias ventriculares malignas fue del 5,7% que, en su mayoría (64%), tenían lugar antes de finalizar la intervención. La presencia de estas arritmias constituía un predictor independiente de mortalidad y su pronóstico era todavía peor en los pacientes que presentaban las arritmias ventriculares tardíamente (una vez terminada la intervención). La aparición de estas arritmias se asociaba directamente con el tamaño del infarto, el flujo coronario y, sobre todo, con la presión sistólica de los pacientes38.
En pacientes en shock cardiogénico, el soporte hemodinámico es fundamental para mejorar la hemodinámica general, la perfusión tisular, descargar el ventrículo izquierdo y mejorar el flujo coronario35,36. Tanto el clásico balón de contrapulsación -ampliamente disponible- como el dispositivo Impella® se utilizan en el laboratorio de hemodinámica durante el tratamiento de estos pacientes. Su empleo «profiláctico» en pacientes estables en los que se plantean intervenciones de alto riesgo (TCI no protegido o equivalente y enfermedad severa de 3 vasos en presencia de disfunción ventricular izquierda) es también controvertido.
El estudio PROTECT-II que comparaba de forma aleatorizada el valor del uso profiláctico del balón de contrapulsación intraaórtico o del nuevo Impella (Impella Recover®LP 2.5) en pacientes muy similares, tampoco ha sido concluyente39. Así, aunque el objetivo primario del estudio a los 30 días solo logró mostrar una tendencia favorable al uso del dispositivo Impella® (probablemente por falta de poder del estudio), durante el seguimiento posterior y con el análisis por protocolo, las diferencias fueron significativamente favorables para el grupo tratado con este dispositivo39.
Intervencionismo durante la RCPLas PC secundarias a una arritmia maligna de causa isquémica puntual son relativamente frecuentes en la sala de hemodinámica y se tratan de forma muy eficaz con una simple cardioversión37,38.
Los pacientes con infarto muy extenso frecuentemente secundario a enfermedad de TCI o EM severa con disfunción ventricular tienen mayor riesgo de esta complicación y su pronóstico es radicalmente diferente. En este escenario, los CTM ofrecen una nueva posibilidad para los pacientes con PC mantenida durante una intervención percutánea (Clase IIa, Evidencia C, 2010) en UH40.
La RCP en la UH debe estar protocolizada. El hemodinamista y el intensivista deben pactar sus actuaciones. El cardiólogo intervencionista debe saber respetar los tiempos requeridos para la realización de una RCP correcta en el laboratorio de hemodinámica y ser muy cuidadoso para no inducir una laceración coronaria o una perforación al realizar actuaciones intracoronarias mientras se realizan maniobras externas.
Los dispositivos Lucas™ permiten mayor libertad al hemodinamista para realizar un mayor número de proyecciones40.
Los pacientes que llegan aceptablemente al laboratorio de hemodinámica pero que durante la intervención sufren una PC mantenida tienen una supervivencia mayor del 30%40. Sin embargo, el pronóstico es mucho peor en aquellos pacientes que son traídos al laboratorio de hemodinámica en PC y mantenidos con RCP40. Por dicho motivo, la indicación de intervencionismo en este último grupo debe realizarse de forma muy cuidadosa. En esta situación puede ser conveniente realizar un ecocardiograma urgente para descartar Actividad Eléctrica Sin Pulso (AESP) tanto secundaria a rotura cardiaca como en pacientes que dependen de estimulación eléctrica externa constante. En algunos de estos pacientes, los dispositivos mecánicos puede servir de puente, bien a dispositivos de soporte hemodinámico percutáneo (balón de contrapulsación o Impella®) o, incluso, a maquinas extracorpóreas con oxigenadores de membrana40.
Resultados de la ACTP primaria en pacientes con PCEntre las primeras experiencias en ACTP en pacientes ya resucitados se encuentran los estudios de Spaulding (1997), Bendz (2004) y Azman (2004). En 2005 Nielsen41 presenta el caso de un varón de 62 años que sufre PC en domicilio ingresando en UH en asistolia bajo compresiones manuales, donde recibe un stent farmacoactivo en un tronco común obstruido, e hipotermia inducida. Es alta del hospital a los 19 días con Cerebral Performance Category (CPC) de 1, regresando a sus actividades habituales a los 6 meses.
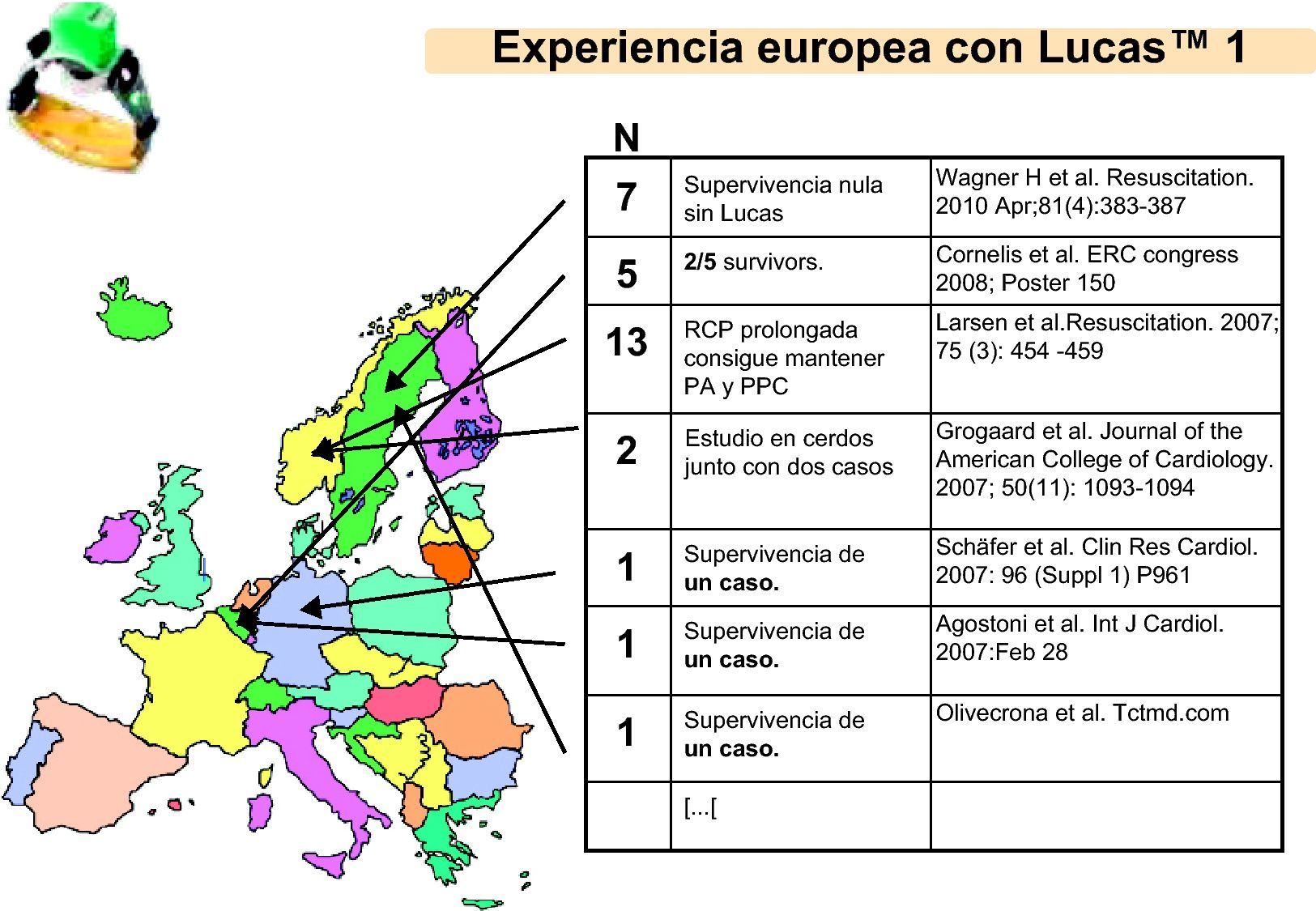
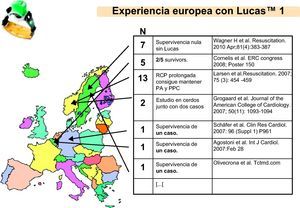
En años posteriores, diferentes países comenzaron a implementar un procedimiento de ACTP durante la RCP con Lucas™ 42–47, datos que se recogen en la figura 2.
También con Lucas™, Wagner et al.48 presentan una cohorte de 3.058 pacientes consecutivos que ingresan en UH para ACTP primaria por IAM, 118 en shock cardiogénico, 81 sufren FV durante el procedimiento y 43 acaban en compresión torácica bajo Lucas™ 1. De estos 43, 17 son alta de UH y 7 fallecen en el hospital por diversas causas relacionadas, siendo alta de hospital 11 pacientes con CPC 1 y 1 con CPC 2. Así descrita, esta serie muestra una supervivencia en ACTP-RCP que llega al 27,90%.
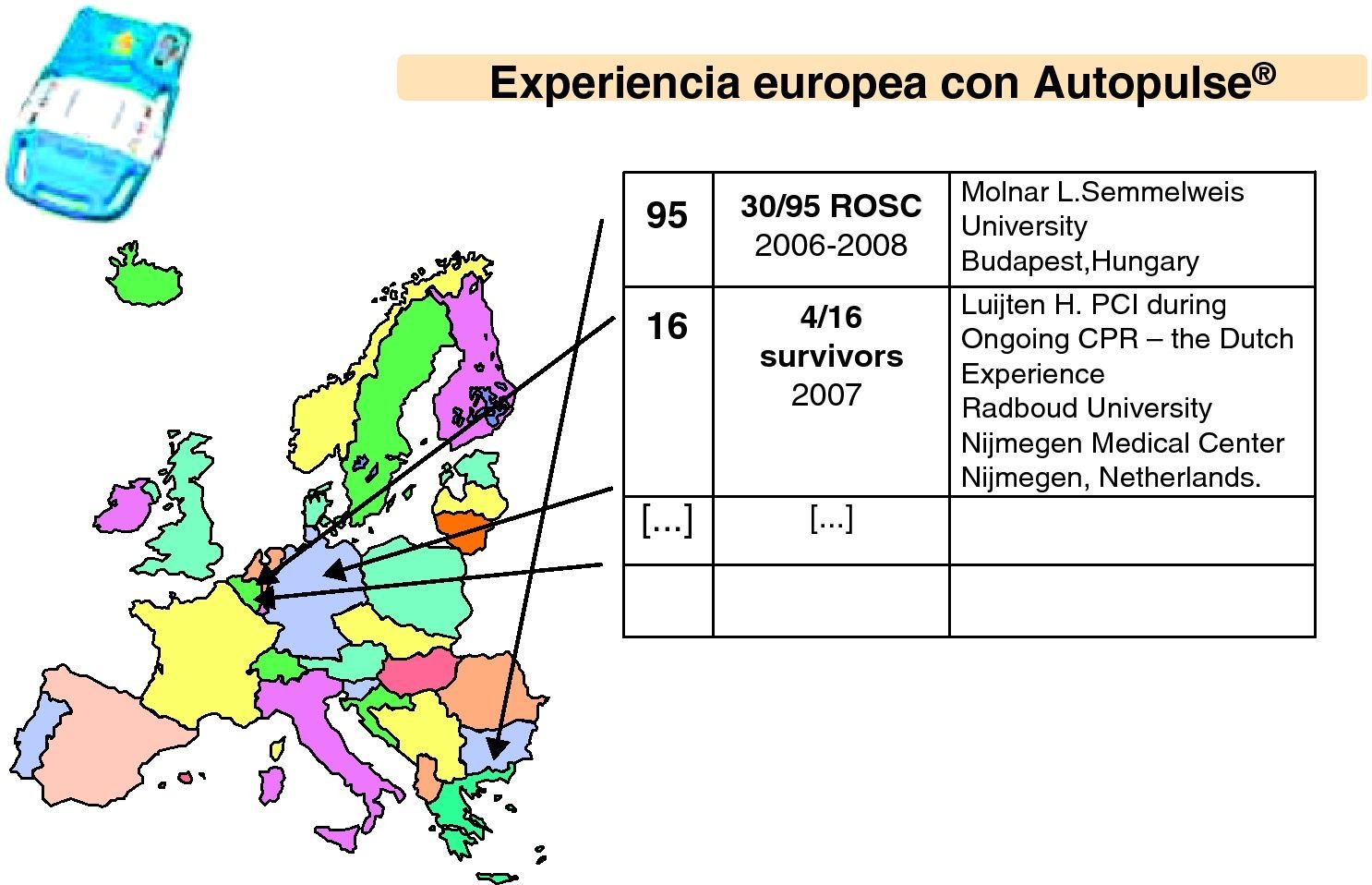
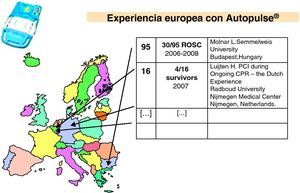
Existen experiencias similares con el dispositivo Autopulse®49,50 (fig. 3).
A modo de comentario, de entre las diferentes series, la mortalidad hospitalaria se incrementa mucho en pacientes tratados con ACTP primaria tras PC, debido fundamentalmente al daño neurológico, renal y pulmonar secundario a una RCP prolongada. Sin embargo, algunos estudios muestran que tras el alta hospitalaria los resultados son similares a los de otros pacientes tratados por un infarto.
Muchos investigadores consideran que los malos resultados de la ACTP primaria en pacientes resucitados tras una PC se deben a la frecuencia presencia de shock cardiogénico. Mager et al.51 excluyeron a los pacientes con shock cardiogénico tras una PC y analizaron los resultados obtenidos en pacientes con infarto aunque hemodinámicamente estables. En este subgrupo, la mortalidad de causa cardiaca no difería de la de otros pacientes tratados con ACTP primaria, aunque la mortalidad de causa no cardiaca era 4 veces mayor51.
Otros estudios se han centrado en analizar los resultados de los pacientes que reciben hipotermia terapéutica para prevenir daños neurológicos. Knafelj et al.52 compararon los resultados de pacientes comatosos supervivientes de un IAM y tratados con ACTP primaria, según se empleara o no hipotermia terapéutica.
El grupo que recibió hipotermia y ACTP primaria mejoró su supervivencia y presentó una mejor recuperación neurológica. Este estudio enfatizaba que, en pacientes con PC y RCP que presentan un SCACEST, era trascendental una correcta RCP y desfibrilación en fase precoz, así como instaurar posteriormente hipotermia terapéutica y conseguir un rápido traslado al hospital para ACTP primaria. Posteriormente, Batista et al.53 demostraron la eficacia de la ACTP primaria en pacientes comatosos tras PC que estaban en hipotermia terapéutica. En esta serie no se detectó aumento de la incidencia de arritmias ventriculares, coagulopatías o infecciones en relación con la intervención. Cuando tanto la hipotermia como la ACTP primaria están indicadas, es muy importante establecer prioridades atendiendo a la condición clínica del paciente ya que la hipotermia puede alargar el tiempo puerta-balón mientras que la intervención puede retrasar la implementación de la hipotermia.
Uno de los firmantes del presente trabajo publica en 2006 un estudio de 63 pacientes tratados en el Hospital Clínico de Madrid con ACTP primaria tras haber sufrido una PC54, con similares incidencia de TV/FV y éxito angiográfico en diferentes grupos, aunque con mayor mortalidad al mes en el grupo sin RCP inmediata, en el que son predictores independientes de mortalidad la existencia de fracaso angiográfico, shock cardiogénico y EM54.
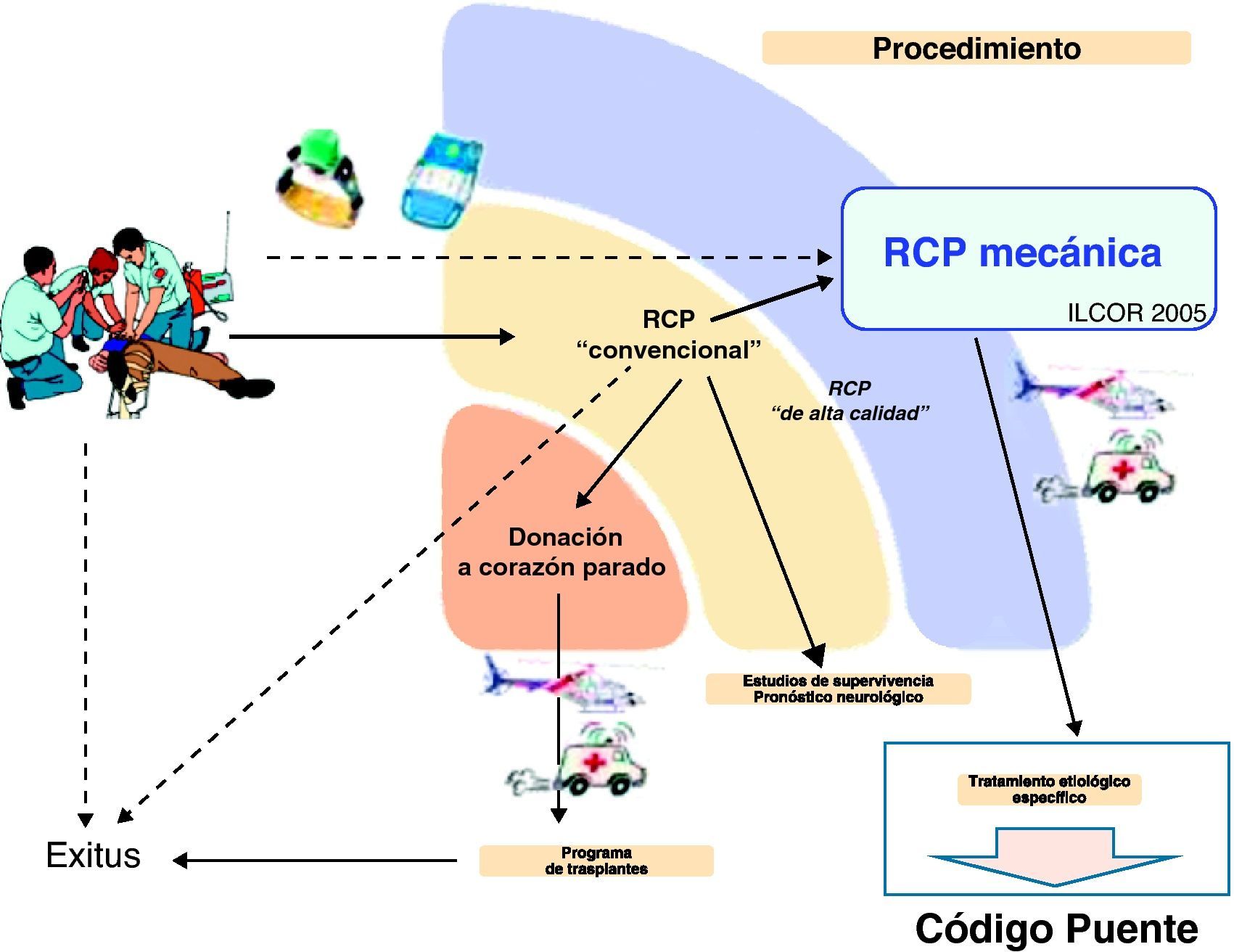
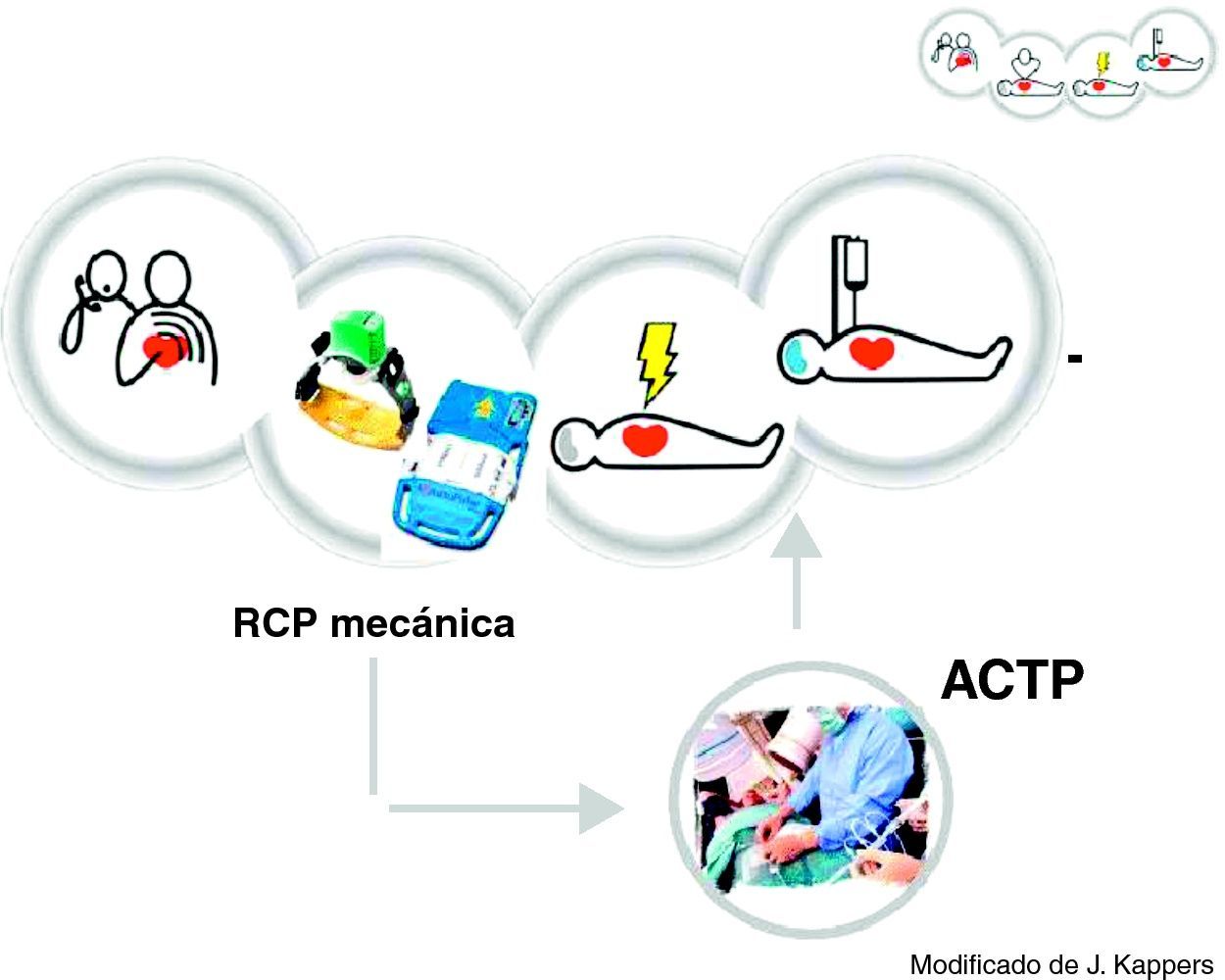
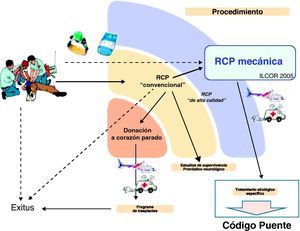
Presentación del código puente de origen coronarioIdentificado el paciente en RCP refractaria de probable causa coronaria, los CTM hacen posible mantener las PPC y cerebral durante el traslado del paciente a la sala de hemodinámica. De esta forma, tanto la RCP mecánica como el uso de dispositivos auxiliares (CardioHelp®)55 sirven a modo de puente56228 para que el paciente pueda recibir su tratamiento etiológico específico: «Código Puente» de origen coronario CPC(fig. 4).
Existen, por otro lado, similares abordajes para pacientes con otras causas de PC. Tanto en el medio prehospitalario como hospitalario, el uso de CTM permitirá: 1) ofrecer a cada paciente el tratamiento etiológico específico para su forma de PC: hipotermia accidental, anafilaxia, embolia masiva de pulmón, etc.56 y 2) hacer posibles técnicas durante la RCP que, en el momento actual, solo podemos ofrecer al paciente en circulación espontánea (ej: hemofiltración, diálisis, gammagrafía de ventilación-perfusión, uso específico de antídotos, tomografía computarizada57, etc.).
Su implicación creciente en programas dependientes de otras técnicas, presentes y futuras permitirá reclutar más pacientes para diferentes programas: bypass fémoro-femoral, soporte vital extracorpóreo (ECLS Extracorporeal Life Support and Resuscitation ECPR), etc. como puente al trasplante cardiaco. Si bien ECPR y ECLS no se aconsejan de rutina (AHA 2010)10, en entornos controlados, con tiempos muy cortos sin flujo y en busca de una causa reversible (Clase IIb, LOE C10) se pueden implicar en escenarios muy similares al CPC.
En última instancia, en caso de fracaso terapéutico de la ACTP y/u otras técnicas, la calidad de PPC y cerebral conseguida por los CTM, tras cumplir los requisitos técnicos, clínicos, éticos y legales, hará posible tender un segundo puente, incluyendo al paciente en el actual programa de Donación a Corazón Parado DCP.
Hipotermia inducidaAunque presentes en las nuevas Recomendaciones AHA e ILCOR 20105,6,8, los programas de hipotermia inducida tras y durante la PC todavía no son de aplicación generalizada en España. En su versión AHA, no solo se recupera la secuencia C-A-B en RCP básica sino que se aconseja tener en cuenta «las 4C de la PC»: Cardiovert/defibrillate, CCR (Cardiocerebral resuscitation), Cooling and Catheterization.
Su aplicación permite reducir y controlar el impacto neurológico en este tipo de pacientes6,8, en función del entorno.
Criterios de inclusión y exclusiónEn este grupo, la sospecha clínica de enfermedad coronaria como causa de PC se convierte en el elemento crítico de selección de pacientes que sigue la ley del todo o nada: el paciente ES o NO ES de origen coronario. Cuando lo es, la supervivencia estadística dependerá del éxito del procedimiento hasta la revascularización. En caso de no serlo, la supervivencia será prácticamente nula, el procedimiento ineficaz.
A fin de beneficiar al paciente de la máxima supervivencia disponible, es necesaria una estricta adherencia al listado de indicaciones y contraindicaciones del procedimiento (v. infra).
Tras 10 minutos de RCP infructuosa -en ausencia de circulación y pulso espontáneos-, haber identificado al paciente como probable o muy probable coronario y eliminado indicaciones de no RCP, procederá a activar el Código Puente (tabla 1). No será candidato al procedimiento cuando presente alguno de los criterios descritos en la tabla 2.
Código Puente de origen coronario. Indicacionesa
| • PCR presenciada con RCP del testigo<10min. o por unidad SVB<15minb. |
| • Acceso a RCP avanzada con aplicación eficaz de compresor torácico mecánicoc. |
| • RCP avanzada refractaria, definida como ausencia de pulso tras 10min. de su inicio. |
| • Sospecha razonada de PCR de etiología coronaria de acuerdo con patrón y criterios clínicos de presentación (ver tabla iii). |
| • Rango de edad comprendido, inicialmente, entre 18 y 70 añosd. |
| • RCP no contraindicada [enfermedad degenerativa y/o terminal, órdenes de no RCP, instrucciones anticipadas, voluntades previas, testamento vital, etc.] |
Para conseguir una mayor supervivencia y adecuación a las recomendaciones, el paciente debe cumplir todos y cada uno de los requisitos enumerados.
Código Puente de origen coronario. Contraindicaciones
| • Ausencia de alguno de los requisitos señalados en la tabla de indicaciones |
| • No es posible activar el procedimiento o, por diferentes motivos, el Centro Coordinador no puede conseguirlo |
| • No es posible mantener la calidad de las compresiones torácicas durante el traslado [ej: evacuación por escaleras, piso a diferente nivel, difícil acceso, rescate complejo, etc.] |
| • Fallo del sistema mecánico de compresión |
| • Otras situaciones que, a juicio del equipo de emergencia, puedan comprometer la eficacia de las compresiones torácicas y/o la viabilidad de la perfusión cerebral del paciente |
Nota técnica: Lucas™ posible desde 16 años y/o tamaño compatible.
Autopulse® posible desde los 18 años. Permite 15 grados de inclinación horizontal.
La identificación del paciente como candidato se basa, en su mayor parte, en criterios clínicos y epidemiológicos, en parte presentados en la tabla 3. Un listado de criterios que, guiado por la evidencia, crecerá, sin duda, en los próximos años26,58.
Factores predictivos de enfermedad coronaria como causa de la PCR
| Patrón epidemiológico |
| • Paciente en grupo de elevada prevalencia para enfermedad coronaria (edad, sexo, etc.) |
| • Existencia previa de enfermedad coronaria documentada (IAM, angina previos, angioplastia, bypass coronario previo, etc.) |
| • Presencia de uno o más factores de alto riesgo para enfermedad coronaria: diabetes mellitus, hipertensión arterial, obesidad, consumo excesivo de tabaco |
| Diagnóstico previo de SCA previo a la PCR [de minutos a horas] |
| Con los siguientes patrones: |
| • Patrón clínico+ECG compatible: |
| - Elevación específica del segmento ST en dos o más derivaciones contiguas: |
| VPP 96%, VPN 42%, S 42%, E 95%30 |
| - Pero también: depresión ST, trastornos de conducción, etc. |
| VPP 56%30 |
| • Marcadores enzimáticos/químicos de SCA: |
| - Troponina T S 96%, E 80% para IAM30 |
| - CK MB S 96% E 73% para IAM30 |
| - Otros |
| Forma de presentación. Historia clínica inmediata previa a la PC |
| • Contexto clínico del paciente |
| Ej1: paciente que cae desplomado con la mano en el pecho o dolor torácico de segundos de duración |
| Ej2: paciente con dolor epigástrico de 24h de evolución que ahora está inconsciente |
| • Forma de presentación y asociación demostrada o sospechada entre SCA y PC |
| a Todos estos factores deben valorarse solos o en asociación, a fin de realizar una estimación del riesgo coronario del paciente |
| b A partir de su valoración se realizará una estratificación de riesgo |
| Ej: factores de alto riesgo para SCACEST37,38. |
| • Troponina cardiaca positiva |
| • Diabetes mellitus |
| • Inestabilidad hemodinámica o rítmica |
| • Desviación del segmento ST en el electrocardiograma |
| Ej: factores de alto riesgo para SCASEST: |
| • Disfunción sistólica del ventrículo izquierdo |
El presente estudio persigue como objetivo fundamental favorecer la supervivencia del grupo de pacientes en PCR refractaria a las medidas convencionales. Una supervivencia que, en el momento actual, es prácticamente nula.
En ausencia de series de casos en PCR de origen prehospitalario (supervivencia de PCR en UH próxima al 27,90%48) la comunicación de casos aislados42–47,49,50 permite sospechar un impacto positivo en supervivencia.
Como objetivos secundarios, los grupos deben ser capaces de:
- 1)
Aplicar criterios que permitan detectar al paciente en PCR de causa coronaria
- 2)
Desarrollar y validar el uso de índices predictivos al respecto
- 3)
Sentar los principios para realizar una RCP de calidad
- 4)
Establecer mecanismos de alerta y coordinación entre niveles
- 5)
Mejorar los procedimientos de recepción y monitorización del paciente
- 6)
Establecer procedimientos para el manejo de estos pacientes en UH
Tras una fase previa de entrenamiento hasta conseguir hacer viable la exploración en ausencia de riesgos añadidos, así como un pilotaje inicial, recogido una serie no inferior a 15-20 pacientes, el programa persigue formar parte de la cartera de servicios de la UH.
La limitación experimental de este tipo de estudios de diseño prospectivo puede controlarse, en parte, gracias a la comparación con el registro histórico de pacientes para los que esta técnica no estaba disponible.
Dada la similitud de requerimientos técnicos y de personal con los actuales programas de Donación a Corazón Parado, la obligada solicitud al Comité de Ética deberá aprovechar parte de la experiencia y trabajo realizados en estos últimos.
Descripción del procedimiento figura 5En su versión completa, el CPC comienza en el medio extrahospitalario a cargo del equipo de emergencias que, tras 10 minutos de RCP avanzada infructuosa, activará el procedimiento iniciando el traslado del paciente según protocolo. Es su responsabilidad proporcionar una información veraz y coherente a familiares y/o allegados -incluso con un modelo escrito que lo describa con palabras claras y sencillas- que los esfuerzos por su vida todavía no se han agotado, siendo igualmente posible: (1) Que el paciente recupere pulso, continuando la evacuación al hospital de referencia -la opción más favorable para el paciente-. (2) Que continúe siendo candidato al CPC y (3) Que, en caso de fracaso del procedimiento, sea necesario solicitar a la familia nuevo permiso para incluir al paciente en un programa de DCP.
Un modelo escrito en formato check-list favorece su aplicación, al tiempo que una hoja de recogida de datos permite cruzar datos clínicos del paciente, situación clínica y entorno de la PCR, así como tiempos de actuación y su correlación con la supervivencia. Diferentes grupos deben compartir similares datos y procedimientos de actuación, así como un esquema de requisitos mínimos que permita estandarizar los datos entre diferentes unidades.
RCP de calidadAparte de evitar interrupciones en las CTM, este concepto intenta optimizar su calidad en fuerza, profundidad y frecuencia, evitando hiperventilar al paciente e integrando las actuales recomendaciones en un esquema organizado. Entre las recomendaciones prácticas, el equipo debe ser capaz de aplicar todos estos principios de acuerdo con el listado que se recoge en la tabla 4.
RCP de calidad: aplicación, monitorización y control
| Durante la RCP |
| A sus recomendaciones de monitorización y cuidados avanzados, incluidos ECG y SpO2 continuas, añadir |
| • Monitorización continua de TECO2, anotando sus valores |
| • Medida inicial de glucemia capilar, lactato y pH venosos mediante dispositivo Point of Care o similar |
| • Como alternativa, extracción de muestras para procesado en hospital, incluidas troponina T y CK-MB |
| • Monitorización continua de la curva de pletismografía transcutánea (visible en pantalla) |
| • Control de temperatura central. |
| Tras activación del Código Puente |
| • Revise secuencia según procedimiento |
| • Confirme destino e información a la familia |
| • Allí donde se dispone, induccción de hipotermia de inicio prehospitalario [ver procedimiento específico] |
| Gestos y actuaciones |
| • Optimización y monitorización hemodinámica de las compresiones torácicas producidas por el CTM |
| Vigile fuerza, profundidad y frecuencia de las CTM. Permita la descompresión completa del tórax entre compresiones |
| Evite hiperventilación e hiperoxigenación |
| • Durante la RCP, no realice pausas para comprobar pulso, monitorizar o desfibrilar |
| • Utilice la información derivada de todos los monitores y dispositivos para adecuar las maniobras de RCP |
| Documente cualquier cambio junto con la hora a la que se produce |
| • Cuidados posrresucitación según recomendaciones y guiados por objetivos (ver procedimiento específico) |
Al no existir estándares unificados, es aconsejable la adherencia las recomendaciones de manejo del síndrome posparada cardiaca, al que añadirá los elementos de su protocolo local
Durante la RCP mecánica puede ser necesario detener las compresiones al objeto de comprobar una posible RCE y/o desfibrilar al paciente. Al objeto de salvar este obstáculo, la tecnología [See-Thru CPR®] permite administrar desfibrilaciones sincronizadas [Autopulse®+Zoll Serie E®] sin necesidad de detener el CTM [Autopulse®].
Recepción del paciente. Manejo en la unidad de hemodinámica figura 6La recepción hospitalaria debe ser completa y exhaustiva, garantizando que la transferencia de paciente y documentación se completa de forma satisfactoria, si es posible mediante una lista de chequeo. El nivel de cuidados y equipamiento requerido será equiparable al del transporte intrahospitalario a prueba diagnóstica/terapéutica de un paciente de máximo riesgo. De forma genérica, de acuerdo con la bibliografía existente42–48, el intervalo máximo disponible colapso-balón no debe superar los 90 minutos.
Por su especial complejidad y necesidad de cuidados especializados, la responsabilidad de asumir el control de las prioridades del paciente en la UH corre a cargo del especialista en Cuidados Intensivos, de presencia física durante todo el procedimiento.
Tras revisar la escasa bibliografía disponible, hemos tenido la oportunidad de probar ambos dispositivos: Lucas™ 2 y Autopulse®, gracias a la cesión de ambos equipos y consentimiento informado por parte de los pacientes. Al ser en su mayor parte radiotransparente, Lucas™ 2 permite una mejor visualización de las estructuras coronarias en diferentes proyecciones, lo que no fue igualmente posible con Autopulse®, utilizando fielmente incluso las modificaciones recomendadas por el fabricante, debido a la existencia en la tabla dorsal de numerosos sistemas metálicos que interferían con la visualización. Una segunda UH en España tuvo similares resultados con Autopulse® en fecha anterior [comunicación personal].
En consecuencia, de acuerdo con nuestra experiencia preliminar, recomendamos el uso de Lucas™ 2 para el procedimiento de revascularización en la UH, utilizando ambos CTM: Lucas™ 2 y Autopulse® de forma equivalente para realizar CTM en el resto de los entornos.
A modo de conclusión, este modelo secuencial de atención del paciente en RCP refractaria se basa en: 1) una adecuada selección de los pacientes en PCR de causa coronaria; 2) una evacuación precoz del paciente utilizando alguno de los actuales compresores torácicos mecánicos; 3) la revascularización coronaria urgente del paciente durante la RCP, y 4) la aplicación de cuidados intensivos posrresucitación, hipotermia incluida.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los autores desean expresar su agradecimiento a Marisa Almarza, Raúl Coto, Camino Bañuelos, Karl Berggren, Luis de Vega-Cabezudo, Gonzalo Díez-Canseco, Robert Engelkes, Jorge Errejón, Salvador Espinosa, José Vicente Esteban, Cristiana Federici, Antonio Fernández, Bonifacio García-Cuenca, Javier García Menéndez, Enrique Hernández, Jürgen Kappers, Sara Lindroth, Bjarne Madsen Hardig, Bela Merkely, Göran Olivecrona, Iván Ortega, Guadalupe Pérez, Ignacio Plaza, Juan Antonio Sinisterra, Dámaso Tomás, y Bas van de Wakker por su inestimable apoyo documental y personal.